本实验通过构建含目标调控序列的荧光素酶报告质粒,转染至细胞后,检测荧光素酶活性,从而评估特定转录因子对目标基因的调控作用,或筛选影响基因表达的化合物。
- 实验流程
(一)转染及荧光素酶活性检测
-
-
-
- 转染体系(每孔)
-
-
试剂
用量
Hieff TransTM试剂
0.45 ul
报告基因载体
0.15ug
VecFOXO3
0.25ul
无血清DMEM
20ul
-
-
-
- 转染程序
-
-
- 转染前一天,将细胞用胰酶消化铺96孔板,控制第二天细胞汇合度约为70~80%
- 将Hieff TransTM、报告基因载体、VecFOXO3、无血清培养基平衡至+15~25℃;
- 对于每孔用10ul无血清培养基稀释0.15ug报告基因载体,用10ul无血清培养基稀释0.45ul Hieff TransTM试剂,并在室温孵育5min;
- 轻轻涡旋载体溶液,并逐滴添加稀释的Hieff TransTM试剂,充分混匀后,室温静置 10~25 min以形成 DNA-Hieff TransTM复合物;
- 对于每孔用3ul无血清培养基稀释0.3ul Hieff TransTM试剂,并在室温孵育5min;
- 轻轻涡旋溶液,并添加0.25ul VecFOXO3,充分混匀后,室温静置 10~25 min以形成 RNA-Hieff TransTM复合物;
- 96孔细胞培养板每孔换成80ul无血清培养基;并将复合物逐滴加入孔中,边加边摇晃;
⑧ 37℃,5% CO2培养箱培养24-48h,直至进行转基因表达分析,无需去掉复合物或更换培养基。但对于脆弱的细胞,可能有必要在6h后更换成完全培养基,不会降低转染活性
(3)荧光素酶检测
① 将荧光检测仪打开,设定参数测定时间为10s,测定间隔为2s;
② 裂解细胞:对于贴壁细胞,96孔板培养板吸尽细胞培养液,加入100ul细胞裂解液,轻轻旋转培养板使裂解液完全覆盖细胞,冰上孵育5 min,充分裂解细胞;
③ 配制萤火虫荧光素酶反应工作液和海肾荧光素酶反应液,即萤火虫荧光素酶底物(50 X)和海肾荧光素酶底物(50 X)分别用对应的缓冲液稀释至1 X 工作液。并孵育至室温;
④ 取20 μL细胞裂解液,加至黑色酶标板中。⑤ 加入100 μL 萤火虫荧光素酶反应液,震板混匀,检测萤火虫荧光素酶的活力,
⑥ 加入100 μL 海肾荧光素酶反应液,震板混匀,静置10min后检测海肾荧光素酶的活力;
检测值比值ratio=萤火虫荧光素酶检测值 / 海肾荧光素酶检测值;
✅ 高灵敏度:生物发光信号无背景干扰,检测下限低至单细胞水平
✅ 高通量:适用于96/384孔板,可快速筛选大量样本或化合物
✅ 动态范围广:发光信号与酶活性呈线性关系,覆盖宽浓度范围
✅ 灵活性高:可结合多种实验设计(如双荧光素酶系统、药物处理等)
- 适用范围
1️⃣ 转录因子活性检测(如NF-κB、STAT3等信号通路研究)
2️⃣ 启动子或增强子功能分析
3️⃣ 药物或小分子化合物对基因表达的调控研究
4️⃣ 基因编辑(CRISPR/Cas9)后调控效应评估
六、代表性实验结果
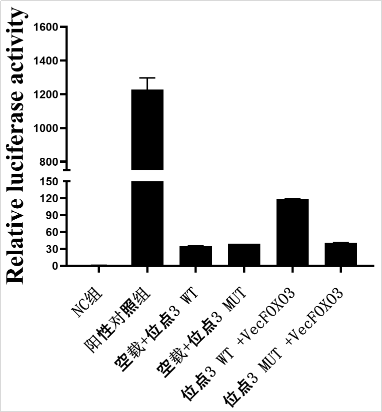
1
细胞类型(贴壁或悬浮细胞),建议提供细胞培养条件
2
实验设计需求(如药物浓度梯度、处理时间、对照设置等)
3
目标序列信息(提供待研究调控元件的DNA序列或GenBank编号)
