对于刚涉足医疗器械领域的新手而言,全面了解医疗器械颇具难度。在日常工作中,各岗位人员各司其职,研发、注册、生产、销售、售后、财务等人员专注于自身业务。然而,工作一段时间后,大家会感觉有条 “绳” 在牵引,这是因为每项工作都有相应流程指引,且需严谨对待。整个项目按策划、输入、输出、验证、确认、转换等步骤推进,产品的整个生命周期都受质量管理体系监督。而这根 “绳” 正是《医疗器械监督管理条例》。接下来,我将依据该条例逐条展开,为医疗器械从业者呈现相对完整的工作框架。
什么是医疗器械?
医疗器械,是指直接或者间接用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相关的物品,包括所需要的计算机软件;其效用主要通过物理等方式获得,不是通过药理学、免疫学或者代谢的方式获得,或者虽然有这些方式参与但是只起辅助作用。
目的:疾病的诊断、预防、监护、治疗或者缓解;损伤的诊断、监护、治疗、缓解或者功能补偿;生理结构或者生理过程的检验、替代、调节或者支持;生命的支持或者维持;妊娠控制;通过对来自人体的样本进行检查,为医疗或者诊断目的提供信息。
《医疗器械监督管理条例》有哪些内容?
总则:国务院药品监督管理部门负责全国医疗器械监督管理工作;遵循风险管理、全程管控、科学监管、社会共治的原则;国家对医疗器械按照风险程度实行分类管理
医疗器械产品注册与备案:
第一类医疗器械实行产品备案管理:第一类医疗器械产品备案,由备案人向所在地设区的市级人民政府负责药品监督管理的部门提交备案资料
第二类、第三类医疗器械实行产品注册管理:需提供的注册申请资料

受理注册申请的药品监督管理部门应当自收到审评意见之日起20个工作日内作出决定。对符合条件的,准予注册并发给医疗器械注册证
注册审评:
补正通知:技术审评过程中需要申请人补正资料的,技术审评机构应当一次告知需要补正的全部内容。申请人应当在收到补正通知1年内,按照补正通知要求一次提供补充资料;技术审评机构收到补充资料后,在规定的时限内完成技术审评
评审不通过:医疗器械注册申请审评期间,对于拟作出不通过的审评结论的,技术审评机构应当告知申请人不通过的理由,申请人可以在15日内向技术审评机构提出异议,异议内容仅限于原申请事项和原申请资料。技术审评机构结合申请人的异议意见进行综合评估并反馈申请人。异议处理时间不计入审评时限。
不予注册的情况:申请人对拟上市销售医疗器械的安全性、有效性、质量可控性进行的研究及其结果无法证明产品安全、有效、质量可控的;质量管理体系核查不通过,以及申请人拒绝接受质量管理体系现场检查的;注册申请资料虚假的;注册申请资料内容混乱、矛盾,注册申请资料内容与申请项目明显不符,不能证明产品安全、有效、质量可控的
附条件品准注册:对用于治疗罕见疾病、严重危及生命且尚无有效治疗手段的疾病和应对公共卫生事件等急需的医疗器械,药品监督管理部门可以作出附条件批准决定,并在医疗器械注册证中载明有效期、上市后需要继续完成的研究工作及完成时限等相关事项;对附条件批准的医疗器械,注册人应当在医疗器械上市后收集受益和风险相关数据,持续对产品的受益和风险开展监测与评估,采取有效措施主动管控风险,并在规定期限内按照要求完成研究并提交相关资料;对附条件批准的医疗器械,注册人逾期未按照要求完成研究或者不能证明其受益大于风险的,注册人应当及时申请办理医疗器械注册证注销手续,药品监督管理部门可以依法注销医疗器械注册证;未列入医疗器械分类目录的可以直接申请第三类医疗器械产品注册
特殊注册程序:创新注册;优先注册;应急注册
变更注册:已注册的第二类、第三类医疗器械产品,其设计、原材料、生产工艺、适用范围、使用方法等发生实质性变化,有可能影响该医疗器械安全、有效的,注册人应当向原注册部门申请办理变更注册手续
延续注册:医疗器械注册证有效期届满需要延续注册的,注册人应当在医疗器械注册证有效期届满6个月前,向原注册部门申请延续注册,并按照相关要求提交申请资料
医疗器械备案:进行医疗器械备案,备案人应当按照《医疗器械监督管理条例》的规定向药品监督管理部门提交备案资料,获取备案编号
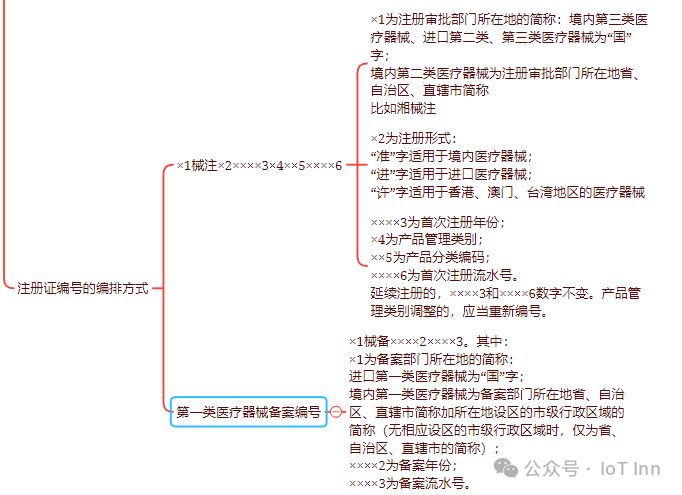
注册证编号的编排方式:
体系资料:
