FDA发布一项关于美敦力消化道产品早期警告。本次警告包括美敦力的Bravo CF Capsule的多种型号输送系统,其预期用途:将pH监测胶囊附着于食管壁,记录pH数据辅助医生诊断胃食管反流病。胶囊在测量食管pH值的同时将数据传输至患者腰间的记录仪,患者可标记症状时间点,供医生比照反流事件与症状关联性。

涉事产品FDA要求美敦力立即停用并下架以下Bravo CF Capsule输送系统。
警告原因
美敦力在生产Bravo CF Capsule输送系统过程中粘合剂使用不当,pH监测胶囊可能无法按预期附着于食管或从输送装置脱离。从而可能引发以下危险:
患者误吸/呛入
食管穿孔
呼吸道阻塞
出血/失血
食管撕裂伤
延误诊断
体内残留异物
目前已经造成33起严重伤害事件,暂无死亡病例。
美敦力初步措施
立即识别并隔离存放所有未使用的涉事批次产品(FGS-0635五只装/FGS-0636单只装)
批号标注位置:FGS-0635外包装标签及FGS-0636单只装产品(核查批号需参照原文链接完整清单)
产品标签示例:
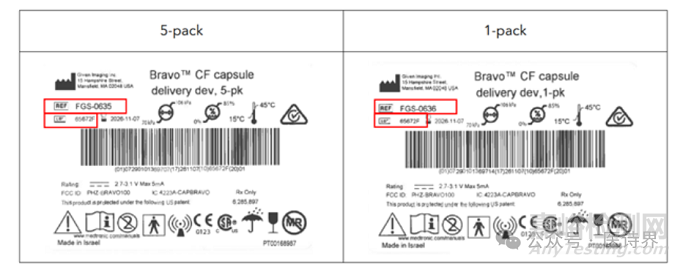
按《客户确认表》要求将未使用的涉事产品退回美敦力换取替代品或退款

