猪输尿管怎么吃智能控制肾盂压力在柔性输尿管镜手术中的流量效应与肾单位保护:基于活体猪模型的研究
在泌尿外科领域,柔性输尿管镜手术(FURS)已成为上尿路结石的主流治疗方式,但高达25%的并发症发生率始终是临床痛点。其中肾盂压力(RPP)的异常升高被公认为导致肾单位损伤、败血症等严重并发症的核心机制。当RPP超过40 mmHg时,可引发肾小球滤过停滞、肾小管基底膜断裂等不可逆损伤,而传统手术中缺乏实时压力监控手段,医生仅能通过经验性调节灌注流量来模糊控制压力,这种"盲操作"模式存在显著安全隐患。
赣州市人民医院的研究团队针对这一临床难题,创新性地开发了智能肾盂压力控制系统(FURS-ICP)。该团队在《BMC Urology》发表的研究中,通过12只雌性小型猪(6对肾脏)的活体实验,系统评估了不同灌注流量(50/100/150 mL/min)下压力控制的效果差异。研究采用特制12/14-Fr测压输尿管通路鞘(UAS),其独特的三通道设计(压力测量/吸引/工作通道)实现了RPP的闭环调控。
关键技术包括:(1)建立活体猪模型,超声引导下肾穿刺获取基线病理;(2)使用PID(比例-积分-微分)控制器自动调节负压吸引;(3)多组对照设计(压力控制组设定-10/0/10 mmHg三梯度,非压力控制组仅调节流量);(4)HE/GMS双重染色评估肾单位超微结构变化。
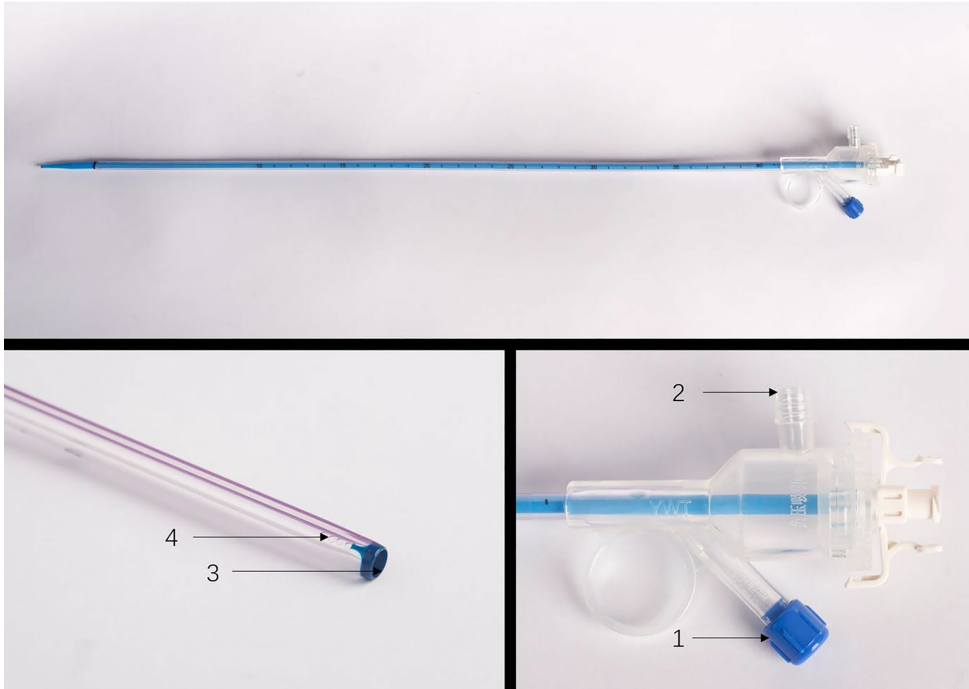
研究创新性地采用可实时测压的UAS装置(图1),其压力测量孔直接连接肾盂出口,通过PID算法动态调节吸引力度。在30分钟持续灌注中,彩色多普勒超声监测肾周液体渗出情况,并在肾上/中/下极分别取材进行病理学分析。
压力调控精度:非压力控制组的RPP与灌注流量呈正相关(50mL/min:8.70±1.02 mmHg;150mL/min:45.97±9.57 mmHg),差异具有统计学意义(P<0.05)。而压力控制组能将实际RPP波动控制在设定值±2 mmHg范围内,各组间无临床显著差异(如10 mmHg设定组实际值为8.77-9.97 mmHg)。
病理学改变:
- 非压力控制组:100 mL/min流量时即出现肾小球囊腔扩张、基底膜变薄(GMS染色显示黑色细线断裂);150 mL/min时可见红细胞渗出、肾小管上皮细胞空泡变性等不可逆损伤(图4c,d;图5c,d)。
- 压力控制组:所有流量条件下肾小球形态完整,肾小管上皮细胞立方形排列整齐,基底膜连续性保持良好(图4b;图5b)。
该研究首次在活体模型中证实:智能压力控制系统能突破Poiseuille定律的流体力学限制,在不同灌注流量下均实现RPP的精准控制。当RPP>40 mmHg时,病理改变与临床观察到的术后肾功能损伤高度吻合,而将压力控制在10 mmHg以下可完全避免结构性损伤。值得注意的是,猪肾脏的疏松被膜结构可能低估了人类病理性肾脏的实际压力值,这提示临床应用中需设置更严格的安全阈值。
研究局限性包括单时间点观察未能评估长期影响,且静态灌注无法完全模拟术中动态压力波动。但该成果为FURS手术提供了重要的设备改进方向,其核心价值在于将经验性操作转化为量化控制,有望显著降低感染性休克等严重并发症的发生率。未来研究可进一步优化PID参数,开发适应临床复杂场景(如出血、碎石粉末堵塞等)的动态调控算法。
相关推荐
- 病床怎么保养福建省妇产医院电梯维保服务(二次)结果公告(采购包1)
- 病床怎么保养有关质量管理工作总结
- 病床怎么保养明日丨“处暑”之后,养生有“三忌”,保你离病床越来越远
- 病床怎么保养彭州市人民医院病床、治疗车等设备维修服务需求调研公告
- 病床怎么保养当你老了,躺在病床上就会明白,晚年最靠得住的,不是儿女
- 病床怎么保养哈尔滨市电梯安全管理条例(最新全文规定)
- 病床怎么保养原创想要夏天远离病床,养生要做到“一不贪”、“二不露”、“三冻”
- 病床怎么保养北京怀柔医院医用车类和病床等维修服务项目中标公告
- 病床怎么保养养生是中老年人的“专利”?98%的年轻人都不知道自己正透支未来的健康
- 病床怎么保养健康面前别说你有钱,别躺在医院的病床上,后悔没有提早养生保健!