一、实验动物及主要试剂
4~6周龄,体重18~20 g的无特定病原体级雄性C57BL/6J野生型(wild type,WT)小鼠(12只)和NRG4全身敲除(gene knockout,KO)小鼠(12只)(上海南方模型生物科技股份有限公司);血糖仪及试纸(美国强生公司);小动物无创血压仪(softronBP98A);链脲佐菌素(streptozocin,STZ)、苏木素(美国Sigma);柠檬酸钠缓冲溶液(北京索莱宝科技有限公司);腺相关病毒绿色荧光蛋白(adeno-associated viral-green fluorescent protein,AAV-GFP)、腺相关病毒NRG4(adeno-associated viral-neuregulin 4,AAV-NRG4)(汉恒生物公司);生化试剂盒(南京建成生物工程研究所);酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)试剂盒(中国Bioswamp);浓缩型正常山羊血清(武汉博士德生物工程有限公司);NRG4抗体(中国Bioss);F4/80抗体(美国CST);甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase,GAPDH)(中国Servicebio);辣根过氧化物酶标记羊抗小鼠二抗、辣根过氧化物酶标记羊抗兔二抗(武汉博士德生物工程有限公司);Trizol(美国Ambion);RNA逆转录试剂盒(中国VAZYME);台式高速离心机(湖南湘仪);透射电子显微镜(日本日立HT78000);酶标仪(中国Rayto);光学显微镜(日本奥林巴斯BX53);实时聚合酶链反应(real-time polymerase chain reaction,RT-PCR)仪(美国ABI 7900/illumine eco)。
二、方法
1.动物造模及干预:所有动物均在华中科技大学同济医学院实验动物中心无特定病原体级环境饲养,实验室内环境温度20~26 ℃,相对湿度(60±5)%,光照时间12 h/d,干燥通风。分笼饲养,自由摄食摄水。根据我们以前报道的方法[10],以STZ建立糖尿病小鼠模型。DN模型小鼠给予高脂饲料(high fat diet,HFD,脂肪41%,碳水化合物42%,蛋白质17%)喂养;对照组给予普通饲料。造模组腹腔注射STZ,剂量为50 mg·kg-1·d-1,连续5 d;对照组腹腔注射等体积柠檬酸缓冲液。9 d后检测各组小鼠连续2 d随机血糖≥13.9 mmol/L为造模成功[11]。继续高脂饮食并检测小鼠尿白蛋白/肌酐比值(urine albumin/creatine ratio,UACR)>30 μg/mg确定DN造模成功。将24只野生(WT)和NRG4敲除(KO)小鼠按照随机数字表法分为:WT非糖尿病对照(WT-CON)组,WT DN+AAV-GFP(D-WT-GFP)组,KO DN+AAV-GFP(D-KO-GFP)组和KO DN+AAV-NRG4(D-KO-NRG4)组,每组6只。D-WT-GFP组和D-KO-GFP组在小鼠肩胛区BAT一次性注射AAV-GFP(1×1011 vp/ml),D-KO-NRG4组注射AAV-NRG4(1×1011 vp/ml)[12]。8周后取D-KO-GFP组与D-KO-NRG4组小鼠的BAT、肝脏、肾脏、骨骼肌及WAT检测NRG4蛋白表达情况进行腺病毒模型验证。
2.一般代谢及血清生化指标检测:实验干预期间每周定期测量小鼠体重,使用小动物无创血压仪测血压和心率,代谢笼测摄食量及粪便排泄量,鼠尾采血法检测血糖。实验结束后腹腔注射1%戊巴比妥钠麻醉小鼠,使用摘除眼球法取血于离心管中,4 ℃过夜后3 000 r/min(离心半径为6 cm)离心10 min,离心后取上层血清保存于-80 ℃。同时称量小鼠肾脏重量和体重,计算肾重比,肾重比=肾脏重量/体重。ELISA试剂盒检测胰岛素、血清NRG4、IL-1β、IL-6、TNF-α。生化试剂盒检测糖化血红蛋白(glycated hemoglobin A1c,HbA1c)、血清甘油三酯(triglyceride,TG)、总胆固醇(total cholesterol,TC)、游离脂肪酸(free fatty acid,FFA)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)等生化指标。
3.葡萄糖耐受试验(glucose tolerance test,GTT)和胰岛素耐受试验(insulin tolerance test,ITT):实验结束前1 d行GTT,小鼠夜间禁食不禁水16 h,称重测血糖后腹腔注射20%葡萄糖(2 g/kg),分别在0、30、60、90、120 min记录血糖浓度,根据结果绘制曲线并计算曲线下面积(area under the cure,AUC)。小鼠禁食4 h后进行ITT,称重测血糖后腹腔注射胰岛素(0.5 U/kg),分别在0、15、30、60、90 min记录血糖浓度,根据结果绘制曲线并计算AUC。
4.UACR的计算:实验结束前3 d,将小鼠放进代谢笼中,收集24 h后尿液,2 000 r/min(离心半径为6 cm)离心5 min,收集上清,免疫比浊法测定尿微量白蛋白,ELISA法检测尿肌酐,计算UACR。
5. Western blotting检测蛋白水平:提取D-KO-NRG4组和D-KO-GFP组小鼠棕色脂肪、白色脂肪、肾脏、肝脏和骨骼肌组织蛋白,用BCA法进行蛋白定量后,十二烷基硫酸钠-聚丙烯酰胺凝胶电泳后转至聚偏二氟乙烯膜,用含5%脱脂奶粉封闭2 h,依次加入相应特异性一抗NRG4(1∶1 000)、GAPDH(1∶2 000)和辣根过氧化物酶标记的二抗(1∶5 000),使用发光试剂进行显色后用Alpha分析胶片灰度值。
6.过碘酸希夫(periodic acid Schiff,PAS)染色:将固定在4%多聚甲醛中的肾脏组织脱水、透明、包埋、切片,PAS染色后光镜下观察肾小球病理变化,并用Image J软件定量分析肾小球面积和肾小球系膜基质指数。
7.透射电子显微镜:取1 mm3大小肾皮质保存于2.5%戊二醛液中固定24 h,然后在1%的四氧化锇中固定1 h。通过梯度乙醇和丙酮脱水并包埋切片后用1%醋酸铀-枸橼酸铅双染色双氧铀双染色后透射电子显微镜成像并观察肾脏足细胞损伤情况。
8.免疫组织化学法(immunohistochemistry,IHC):将固定在4%多聚甲醛中的肾脏组织石蜡包埋,切片脱蜡,抗原修复,3% H2O2室温孵育5~10 min,血清封闭,滴加1∶300稀释的F4/80抗体,4 ℃湿盒过夜,滴加1∶500生物素化二抗孵育40 min,DAB显色,苏木精复染,封片后电子显微镜下观察并拍照,Image-Pro Plus 6.0软件进行半定量分析,检测F4/80阳性表达累积光密度值。
9.实时荧光定量聚合酶链反应(quantitative real-time polymerase chain reaction,qRT-PCR):用Trizol提取肾组织RNA,以GAPDH为内参,逆转录合成cDNA,建立qRT-PCR反应体系于RT-PCR仪按条件进行PCR扩增,95 ℃预变性5 min,95 ℃变性10 s,40个循环;58 ℃退火20 s,40个循环;72 ℃延伸20 s,40个循环。通过循环阈值(Ct)计算2-ΔΔCt,并计算IL-6、IL-1β、TNF-α mRNA相对表达量。引物序列见表1。
采用SPSS 25.0软件进行统计学分析。正态分布的计量资料以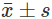 表示,组间差异比较采用单因素方差分析。采用Pearson相关分析法分析血清NRG4水平与血清炎症因子、UACR、肾组织F4/80表达的相关性。以P<0.05为差异有统计学意义。
表示,组间差异比较采用单因素方差分析。采用Pearson相关分析法分析血清NRG4水平与血清炎症因子、UACR、肾组织F4/80表达的相关性。以P<0.05为差异有统计学意义。
与WT-CON组相比,3组DN小鼠的UACR均明显增高,尤其是当NRG4缺乏时,与D-WT-GFP组相比,D-KO-GFP组UACR进一步升高(P<0.01),而当NRG4恢复后,与D-KO-GFP组相比,D-KO-NRG4组UACR水平显著下降(P<0.01,图1)。此外,3组DN小鼠肾重比均明显增高,D-KO-GFP组相较于与D-WT-GFP组小鼠该比值进一步增加(P<0.01),而D-KO-NRG4组相较于D-KO-GFP组肾重比明显降低(P<0.01,表2)。然而,各组小鼠肾功能包括血肌酐和尿素氮结果差异均无统计学意义(P>0.05,表2)。
图1 野生型对照组及各组糖尿病肾病小鼠UACR水平的比较
PAS染色结果显示,DN小鼠肾小球增大,系膜基质增生,系膜区明显增宽(图2A)。与D-WT-GFP组相比,D-KO-GFP组肾小球进一步增加,系膜基质指数增大,而与D-KO-GFP组相比,D-KO-NRG4组肾小球显著减小,系膜基质指数降低(均P<0.01,图2B,2C)。电镜显示,D-KO-GFP组小鼠出现了足细胞足突融合以及肾小球基底膜增厚,而D-KO-NRG4组相较于D-KO-GFP组小鼠足细胞足突融合以及肾小球基底膜增厚的情况得到改善(图3)。
图2 野生型对照组及各组糖尿病肾病小鼠肾脏病理改变。A:过碘酸希夫(PAS)染色观察肾小球病理改变(×400);B:定量分析PAS染色肾小球系膜基质指数;C:定量分析PAS染色肾小球面积
图3 野生型对照组及各组糖尿病肾病小鼠足细胞损伤情况(×8 000)
巨噬细胞免疫组化染色显示,DN小鼠肾组织内可见大量棕褐色颗粒,提示F4/80表达量较非糖尿病小鼠明显增加(图4A)。与D-WT-GFP组相比,D-KO-GFP组F4/80表达进一步升高(P<0.01),而与D-KO-GFP组相比,D-KO-NRG4组F4/80表达明显降低(P<0.01,图4B)。与此同时,D-KO-GFP组相较于D-WT-GFP组小鼠肾组织IL-1β、IL-6、TNF-α mRNA表达增加,而D-KO-NRG4组相较于D-KO-GFP组其表达受到抑制(P<0.05,图5)。此外,血清炎症因子水平的变化与肾脏炎症反应一致(表1)。
图4 野生型对照组及各组糖尿病肾病小鼠肾组织F4/80表达。A:免疫组织化学F4/80染色(×400);B:各组F4/80的累积光密度值
图5 实时荧光定量聚合酶链反应检测各组小鼠肾脏组织IL-1β(A)、IL-6(B)、TNF-α(C)mRNA的相对表达水平
与D-WT-GFP组相比,D-KO-GFP组TG、TC、FFA、LDL-C水平升高,HDL-C水平降低(P<0.01,表1),与D-KO-GFP组相比,D-KO-NRG4组TG、TC、FFA、LDL-C水平降低,HDL-C水平升高(P<0.01)。GTT和ITT结果提示,当NRG4缺乏时,各时相点的血糖、AUC值均升高,胰岛素水平降低(P<0.05),恢复NRG4后则这些代谢异常被明显改善(图6)。此外,与WT-CON相比,3组DN小鼠体重均增加(P<0.01),D-KO-GFP组相较于与D-WT-GFP组体重进一步升高(P<0.01),而D-KO-NRG4组相较于D-KO-GFP组明显降低体重(P<0.01)。各组DN小鼠间血压、心率、摄食量及粪便排泄量差异均无统计意义(P>0.05,表1)。
图6 野生型对照组及各组糖尿病肾病小鼠血糖和胰岛素水平。A:葡萄糖耐量试验;B:葡萄糖耐量试验曲线下面积;C:胰岛素耐量试验;D:胰岛素耐量试验曲线下面积
五、血清NRG4水平与血清炎症因子、UACR、肾组织F4/80表达呈负相关
Pearson相关性分析结果显示,血清NRG4水平与炎症因子(IL-1β、IL-6、TNF-α)均呈负相关(r=-0.548、-0.637、-0.553,P<0.05),与肾组织F4/80表达呈负相关(r=-0.554,P<0.05),与UACR表达也呈负相关(r=-0.503,P<0.05)。
注射AAV-NRG4后在KO小鼠体内可以检测到循环中的NRG4,并持续到1次注射后8周。实验结束后DN小鼠循环NRG4水平降低,D-KO-GFP组与D-KO-NRG4组为全身敲除小鼠,而D-KO-NRG4组注射腺病毒恢复后循环NRG4水平明显升高(P<0.05,表2)。Western blotting结果显示,D-KO-NRG4组小鼠BAT中NRG4蛋白表达水平较高,而肝脏、肾脏、骨骼肌和WAT中NRG4的表达水平较低(P<0.05,图7)。
图7 糖尿病肾病小鼠腺病毒模型各组织NRG4蛋白表达情况。A:2组糖尿病肾病小鼠各组织NRG4蛋白表达的Western blotting条带图;B:基因敲除型糖尿病肾病+腺相关病毒神经调节蛋白4组小鼠各组织NRG4蛋白表达的柱状图
本研究发现,DN小鼠循环NRG4水平降低。当NRG4缺乏时,肾脏炎症反应加重,尿蛋白水平增高,而且肾小球体积增大,系膜基质增生,此外,加重了糖脂代谢紊乱。而当恢复棕色脂肪源性NRG4后,上述变化均得到明显改善。这些结果提示NRG4可以抑制肾脏炎症反应,从而减轻DN肾脏损伤。
NRG4是BAT中表达最为丰富一种脂肪细胞因子。有文献报道,妊娠期糖尿病患者循环NRG4明显降低,并与血糖呈负相关[13];动物实验发现,NRG4抑制肝细胞脂质合成[14]。最近,刘云涛等[15]的一项临床研究发现,早期DN患者血清NRG4水平降低且与UACR负相关,这提示了NRG4可能在DN发生发展中发挥重要作用。然而,NRG4与DN的因果关系目前不清楚。因此,本研究中我们建立HFD/STZ DN小鼠模型,通过NRG4敲除与恢复的方法探讨NRG4与DN之间的因果关系。研究结果提示,敲除NRG4后加重了DN小鼠的尿蛋白水平,肾小球肥大、系膜基质增生及足细胞损伤。而通过病毒转染恢复NRG4后则明显降低DN小鼠尿蛋白和肾小球病理损伤,表明NRG4对DN肾脏损伤有保护作用。
很多研究表明炎症参与了DN的发生发展[16]。炎症因子的异常表达会诱导单核/巨噬细胞在肾小球浸润,形成DN早期肾小球系膜细胞增生和系膜基质增生[17]。因此,抑制炎症是缓解DN的一种潜在的治疗方法。因此,本研究中我们分析了炎症因子和肾组织F4/80表达情况。结果显示,NRG4敲除鼠血清中IL-1β、IL-6、TNF-α水平显著升高,且肾脏内IL-1β、IL-6、TNF-α mRNA表达量也升高,特别是肾组织巨噬细胞浸润增加,而恢复NRG4后则明显抑制了炎症反应并减少巨噬细胞浸润,以上结果表明NRG4通过抑制DN炎症因子反应,保护糖尿病肾损伤。此外,与以往研究结果相似[13],在DN小鼠中NRG4可以改善糖脂代谢,改善胰岛素和葡萄糖耐量,降低体重。
值得注意的是,本研究中DN小鼠循环NRG4水平降低,D-KO-NRG4组浓度低于WT-CON组,但由于NRG4表达量不足,导致实验结果与D-WT-GFP组无明显差异。同时检测各组小鼠肾功能时血肌酐结果显示无明显差异,可能与实验周期过短,DN的发展尚处于早期而导致血肌酐并未发现明显改变有关。
此外,本研究仅在动物水平探讨了棕色脂肪源性NRG4对DN的影响,尚缺乏体外细胞学研究及信号转导研究,需要进一步探讨。
综上,本研究发现棕色脂肪源性NRG4可以降低DN小鼠尿蛋白水平,抑制肾脏炎症反应,保护糖尿病肾损伤。该研究阐明了BAT通过分泌NRG4对肾脏的调控作用,提示BAT有望成为治疗DN的新靶点,而NRG4有望成为防止DN的潜在药物。
参考文献略
作者投稿及专家审稿请登录中华糖尿病杂志官方网站:zhtnbzz.yiigle.com


