转自:IQVIA艾昆纬
导 读
异基因造血干细胞移植是当前根治白血病、骨髓增生异常综合症等多种血液系统疾病的有效手段。巨细胞病毒(Cytomegalovirus, CMV)感染是移植后常见的感染之一,严重影响患者预后,被称为“移植巨魔”。血液移植是极为复杂的系统性工程,CMV感染管理的改进有望优化整体血液移植流程,提升医院管理效率。据此,艾昆纬开展了《中国异基因造血干细胞移植患者巨细胞病毒感染临床管理白皮书》项目,在全国范围内开展定性访谈,并收集了来自91个移植中心150名医生的定量问卷调研结果,结合国内外研究证据编撰《中国异基因造血干细胞移植患者巨细胞病毒感染临床管理白皮书》。本文为白皮书摘要,关注IQVIA智库,近期将发布白皮书全文。
声明:本文信息均来自于公开出版物或调研结果,文中如有错误和疏漏,望各位读者积极指出,不吝赐教。
第一章
我国异基因造血干细胞移植CMV感染管理的迫切性及挑战
巨细胞病毒(Cytomegalovirus, CMV)感染是导致异基因造血干细胞移植(Allogeneic Hematopoietic Stem Cell Transplant, Allo-HSCT)预后不良的主要原因之一。我国主要的移植类型—单倍型移植的CMV感染率高达60%-83%[1]。CMV感染可直接导致CMV疾病(CMV胃肠炎、CMV肺炎等),还会增加机会感染[2]、移植物抗宿主病(Graft versus Host Disease, GvHD)[3]、非复发死亡率以及全因死亡率[4,5]的风险,间接延长患者住院时间,增加临床管理难度。移植后CMV感染管理一直受到临床医生高度重视。
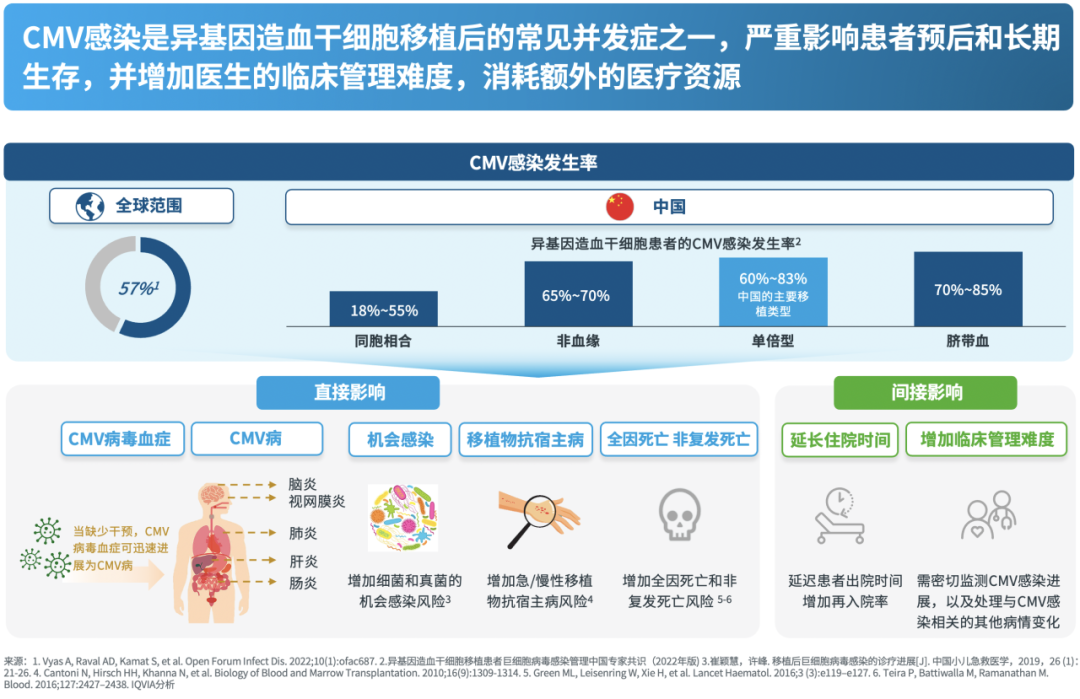
CMV感染最重要的危险因素是移植前受者CMV血清学阳性(R+)[6],此外,还与移植类型(脐带血移植、单倍型移植、非血缘移植感染风险高)、GvHD预防方案、年龄≥40岁等因素有关[7,8]。
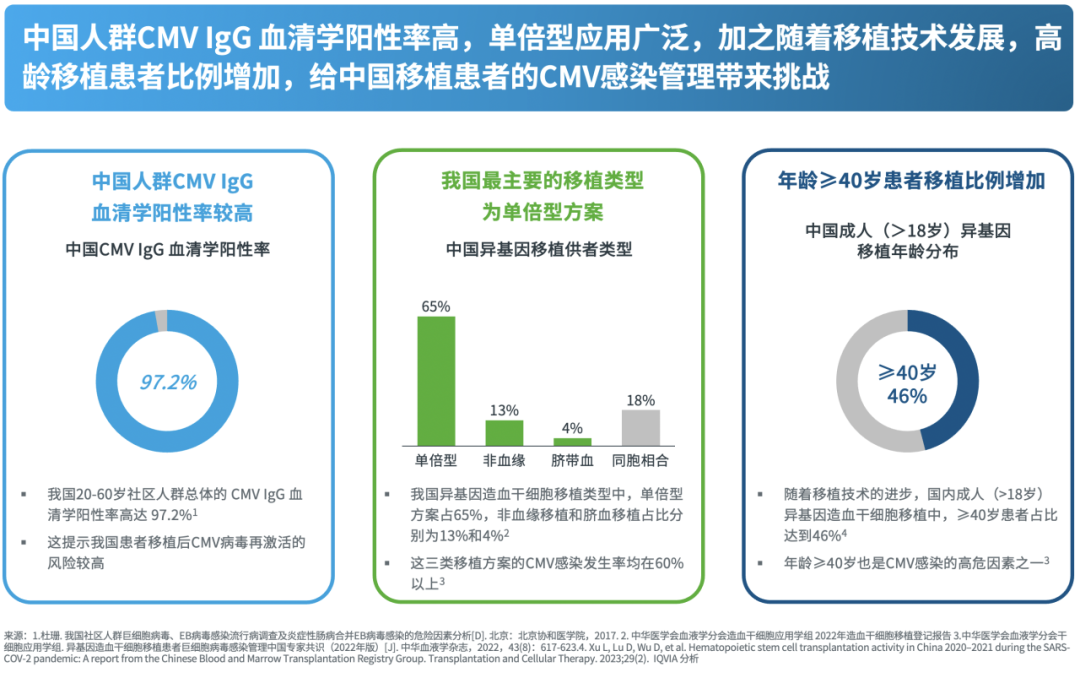
我国人群的CMV IgG血清学阳性率较高[9],主要的移植类型为单倍型方案[10],且近年来随着移植技术进步,年龄≥40岁患者移植比例增加[11],这些因素给我国移植领域CMV感染管理带来挑战。
第二章
我国异基因造血干细胞移植患者CMV感染管理现状
1
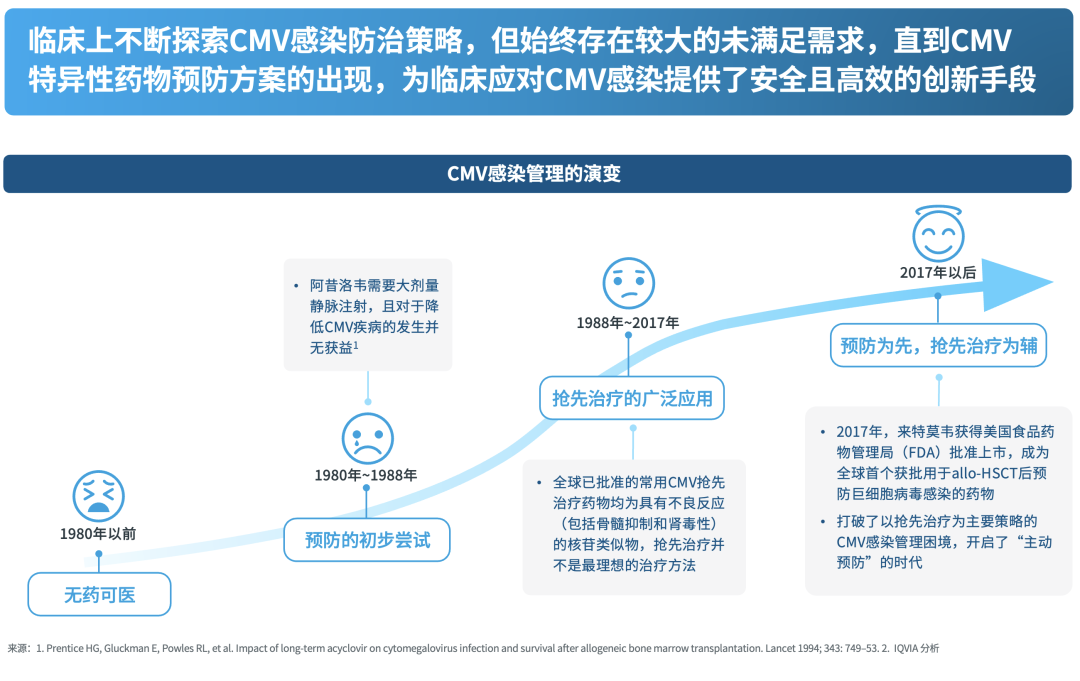
CMV感染管理的演变
异基因造血干细胞移植技术开展以来,临床就在不断探索CMV感染防治策略,但长期缺乏理想的方案。直到CMV特异性预防药物——来特莫韦上市后,开启了“主动预防”的时代。
2
医生对于CMV感染管理的观念
本次调研结果显示,CMV感染“主动预防”观念目前已获得临床广泛认可。CMV特异性预防药物(来特莫韦)的上市与可及性的提高,满足了临床医生长期以来对于移植后患者预防CMV感染的需求。
3
移植后CMV特异性药物预防的应用现状
从临床实际应用来看,CMV特异性药物预防已成为CMV感染管理的主流方案。本次调研结果显示,大部分allo-HSCT成人患者接受过CMV特异性药物预防,但仍存在未按照标准起始时间和疗程用药的情况。
第三章
移植后CMV特异性药物预防带来的临床获益
1
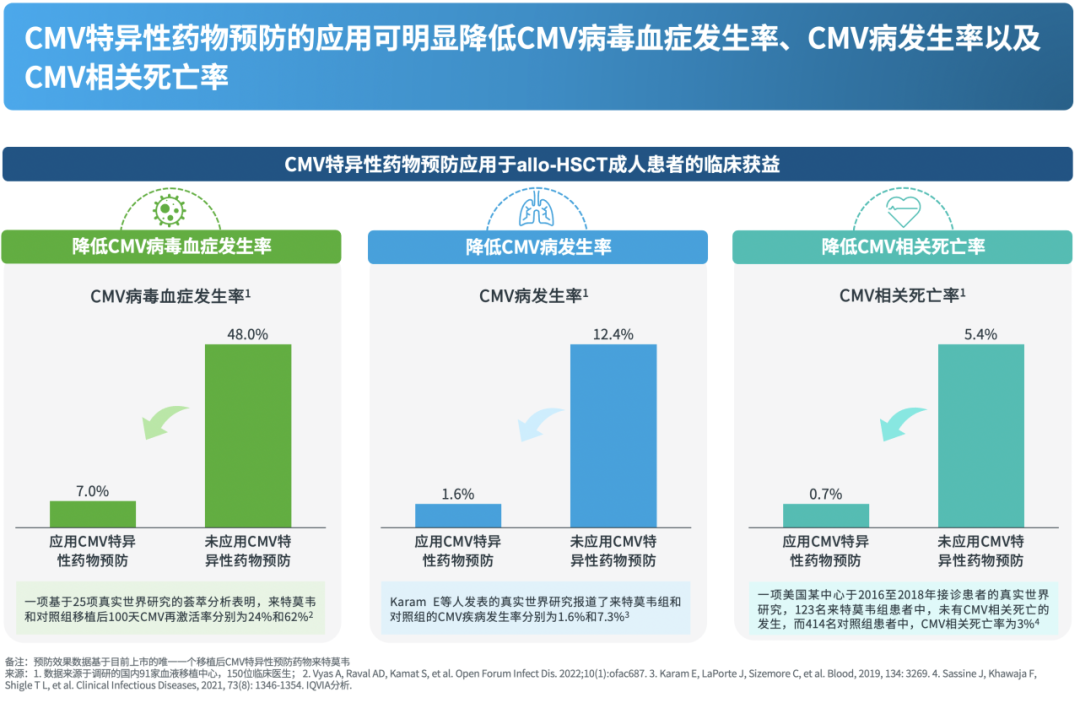
降低CMV病毒血症发生率
应用CMV特异性预防的患者,CMV病毒血症发生率显著低于未应用预防的患者。据调研医生反馈,接受预防与未接受预防的患者CMV病毒血症发生率平均为7%和48%。一项基于25项真实世界研究的荟萃分析表明,来特莫韦和对照组移植后100天CMV再激活率分别为24%和62%[12],同样印证了来特莫韦预防的临床效应。
2
降低疾病发生率
应用CMV特异性药物预防后,CMV疾病发生率降低。据调研医生反馈,应用CMV特异性药物预防的患者CMV疾病发生率为1.6%,是对照组的八分之一。已发表的真实世界研究也显示了类似的结果,Karam E等人报道的来特莫韦组和对照组的CMV疾病发生率分别为1.6%和7.3%[13]。
3
降低CMV相关死亡率
在CMV特异性药物预防下,移植患者的CMV相关死亡率也有所降低。根据调研结果,应用预防的患者CMV相关死亡率低于1%。放眼国际,美国某移植中心的真实世界研究中,123名来特莫韦组患者未有CMV相关死亡的发生,而纳入研究的414名对照组患者的CMV相关死亡率为3%[14]。当然,有关死亡率的分析需要更长的观察期。
4
推迟CMV感染时间
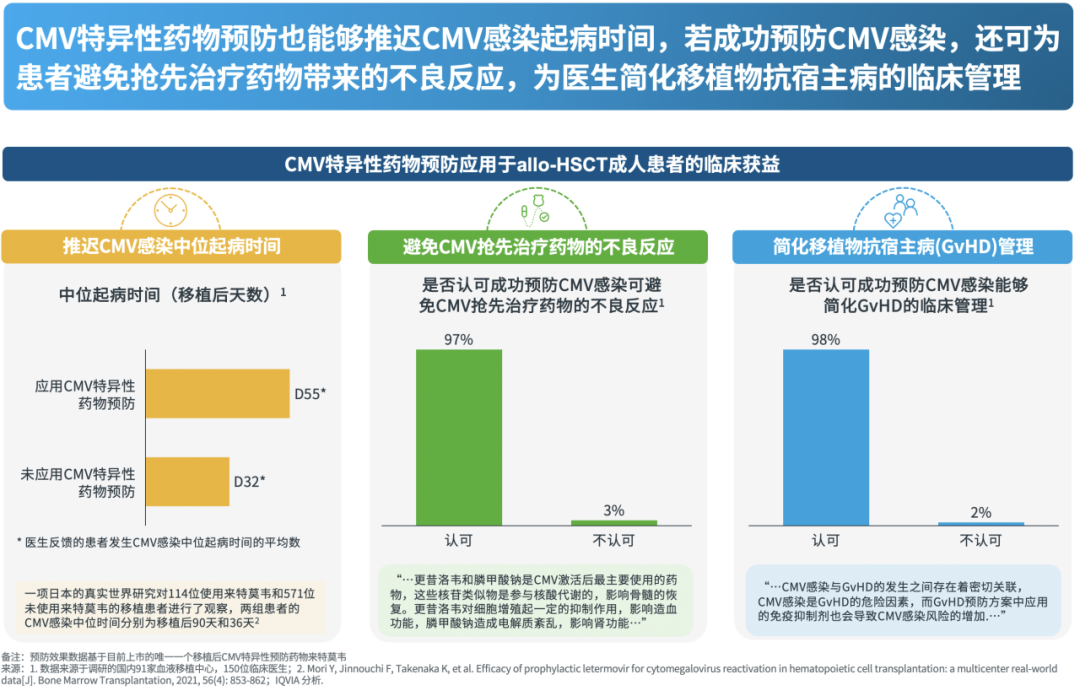
应用CMV特异性药物预防推迟了患者发生CMV感染的时间。本次调研结果显示,应用预防的患者中,发生CMV感染的中位起病时间约为移植后第55天,而未应用预防的患者中,中位起病时间约为移植后第32天。一项日本的真实世界研究报道使用和未使用来特莫韦的两组患者CMV感染中位时间分别为移植后90天和36天[15]。
CMV感染中位时间的推迟对临床管理具有重要意义。据定性访谈中的医生反馈,若在急性GvHD高风险期之后出现CMV感染,感染更易控制,且可减少肠道GvHD和CMV肠炎同时出现的可能性,进而简化临床决策[16]。
5
避免CMV抢先治疗药物的不良反应
调研的临床医生普遍认可成功预防CMV感染可避免CMV治疗药物的不良反应。CMV抢先治疗/治疗常用的一线药物——更昔洛韦和缬更昔洛韦存在骨髓抑制等严重不良反应,膦甲酸钠也易引发肾毒性、电解质紊乱等。成功预防CMV感染可有效避免这些问题产生。
6
简化GvHD管理
成功预防CMV感染能够为GvHD的临床管理带来裨益。98%的调研医生认可“成功预防CMV感染后,医生对于GvHD的管理能够更加方便”。CMV感染的发病机制复杂,包括病毒对人类白细胞抗原表达、细胞因子产生和黏附分子的影响,这可以解释CMV感染与急/慢性GvHD之间的关联[17]。
第四章
移植后CMV特异性药物预防带来的医院管理获益
1
降低CMV感染相关住院率和全因再入院率
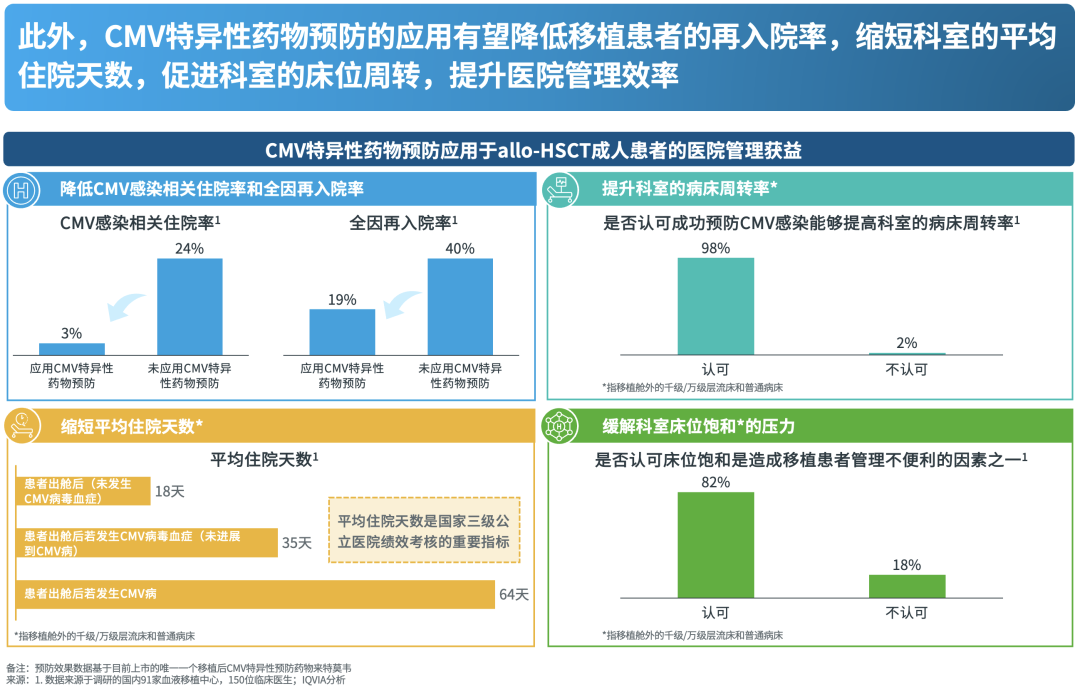
成功预防CMV感染可减少移植患者再入院率。根据调研结果,平均而言,各调研中心使用和未使用来特莫韦的患者中,CMV感染相关住院率分别为3%和24%,全因住院率分别为19%和40%。
2
缩短平均住院天数和提升病床周转率
平均住院天数是医院关注的管理指标之一,降低CMV感染率有望缩短allo-HSCT相关平均住院天数,释放更多住院资源。移植患者出舱后在无CMV感染的情况下平均住院18天;若患者出舱后发生CMV病毒血症,平均住院天数延长至35天;若发生CMV疾病,平均住院天数延长至64天。98%的调研医生认可成功预防CMV感染能够提高科室的病床周转率。
3
缓解科室床位饱和的压力
床位饱和对移植患者管理有所影响,82%的调研医生认可本中心的床位饱和是造成移植患者管理不便利的因素之一。根据定性调研发现,部分中心因普通病床的床位饱和而不能及时让患者出舱,从而也影响了移植舱的使用,另外也会影响血液科其他患者的收治。
4
降低住院患者抗菌药物使用强度(Defined Daily Doses, DDDs)
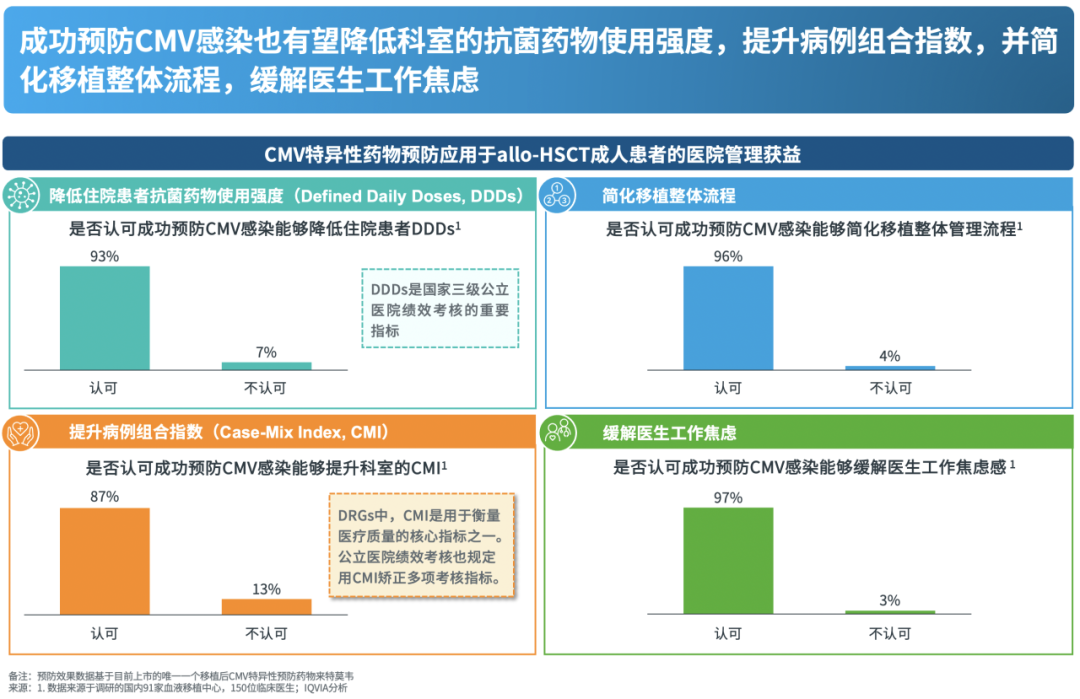
临床医生普遍认可成功预防CMV感染间接降低住院患者DDDs。CMV感染患者继发细菌和真菌感染的风险增加[18,19],进而患者抗菌药物使用也会增加。DDDs是公立医院绩效考核关于医院合理用药的重要考核指标。本次调研中,93%的医生认可成功预防CMV感染能够降低DDDs,提示了CMV感染预防对提升医院DDDs管理的作用。
5
提升病例组合指数(Case-Mix Index, CMI)
临床医生普遍认可成功预防CMV感染间接提升科室的CMI指数。CMI数值越高,代表医疗服务难度系数越高。在本次调研中,87%的医生认可成功预防CMV感染能够提升科室的CMI指数。据定性访谈反馈,医生认为预防CMV感染可以避免医生处理感染而分散精力,以及避免感染患者占用床位,从而可以收治更多疑难杂症患者,提升科室的CMI指数。
6
简化移植流程并缓解医生工作焦虑
成功预防CMV感染将简化移植患者管理的整体流程,缓解医生的工作焦虑感。对于出舱患者,医生往往疲于应对包括急性/慢性GvHD、真菌感染、病毒感染、血液疾病复发在内的各类病情发展变化,工作量接近饱和。根据本次调研反馈,96%的医生认为避免CMV感染能够简化移植整体管理流程,97%的医生认为自身的工作焦虑感能够因此得到缓解。
小结:
CMV特异性药物预防的应用为临床和医院管理带来了多方位的获益。不仅直接影响CMV病毒血症/疾病发生率、CMV相关死亡率等临床结局,改善患者的移植预后,还通过降低再入院率和缩短住院时间、改善DDDs和CMI等绩效考核指标,缓解医院的行政管理压力。
第五章
CMV感染管理上不足与展望
1
当前CMV管理上的不足
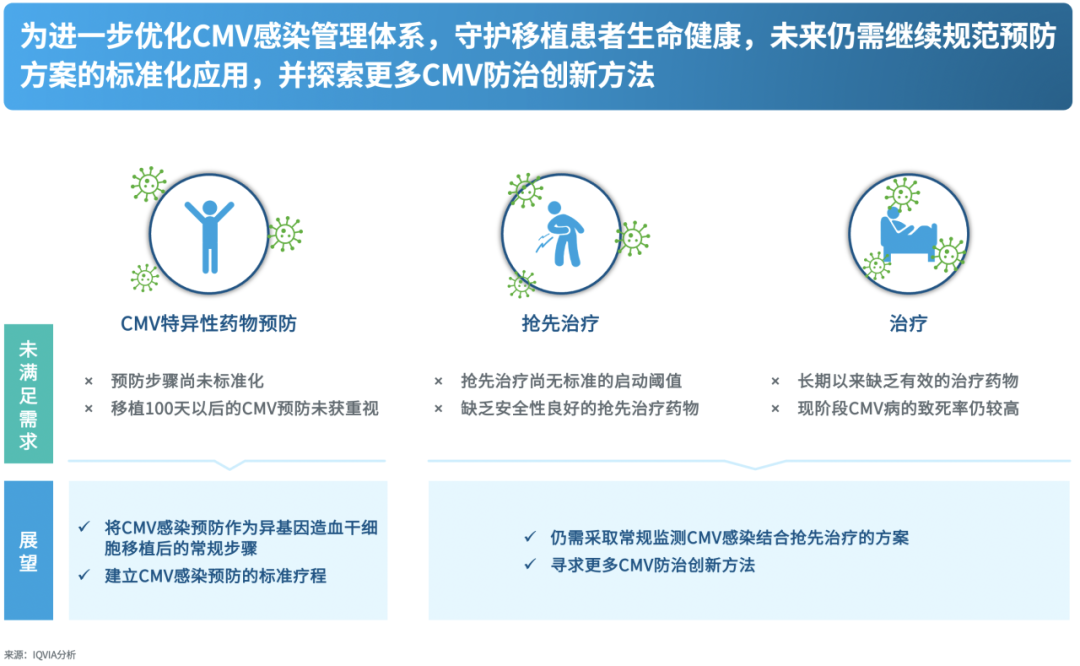
预防策略尚未完全落实,预防步骤尚未完全标准化。部分中心尚未遵照来特莫韦标准预防疗程和起始时间(可在移植当天或不晚于移植后28天开始给药,应持续使用本品至移植后100天),预防效果受到一定影响。即便在移植100天后,仍有发生CMV感染的风险,尤其是急/慢性GvHD患者,但目前这阶段的预防还未受到充分的重视。抢先治疗尚无统一的启动阈值,同时缺乏安全性良好的药物。目前尚无经过验证的统一的病毒载量标准作为启动抢先治疗的阈值,临床上启动抢先治疗的时机依赖于频繁的病毒检测和临床医生的经验,增加了患者的痛苦和经济负担,也增加了临床管理的难度。目前常用的抗CMV药物存在明显的不良反应,疗效或安全性不尽人意。
治疗上长期缺乏有效的药物,疾病致死率高。临床上长期缺乏有效的治疗药物,患者一旦进展到疾病,病死率高达20%~60%[20]。
2
未来CMV感染管理上的展望
优化CMV感染管理体系。一是将CMV感染预防作为allo-HSCT移植后的常规步骤,二是建立CMV感染预防的标准疗程。
探索更多防治CMV的创新方法。例如在研药物马立巴韦、布林西多福韦等,CMV特异性细胞介导免疫治疗、CMV疫苗接种策略、CMV细胞疗法等。
滑动查看注释
[1].中华医学会血液学分会干细胞应用学组. 异基因造血干细胞移植患者巨细胞病毒感染管理中国专家共识(2022年版)[J]. 中华血液学杂志,2022,43(8):617-623. DOI:10.3760/cma.j.issn.0253-2727.2022.08.001.
[2].崔颖慧,许峰. 移植后巨细胞病毒感染的诊疗进展[J]. 中国小儿急救医学,2019,26(1):21-26. DOI:10.3760/cma.j.issn.1673-4912.2019.01.007.
[3].Cantoni N, Hirsch HH, Khanna N, et al. Evidence for a bidirectional relationship between cytomegalovirus replication and acute graft-versus-host disease. Biol Blood Marrow Transplant. 2010;16(9):1309-1314. doi:10.1016/j.bbmt.2010.03.020
[4].Green ML, Leisenring W, Xie H, et al. Cytomegalovirus viral load and mortality after haemopoietic stem cell transplantation in the era of pre-emptive therapy: a retrospective cohort study. Lancet Haematol. 2016;3(3):e119-e127. doi:10.1016/S2352-3026(15)00289-6
[5].Teira P, Battiwalla M, Ramanathan M, et al. Early cytomegalovirus reactivation remains associated with increased transplant-related mortality in the current era: a CIBMTR analysis. Blood. 2016;127(20):2427-2438. doi:10.1182/blood-2015-11-679639
[6].George B, Pati N, Gilroy N, et al. Pre-transplant cytomegalovirus (CMV) serostatus remains the most important determinant of CMV reactivation after allogeneic hematopoietic stem cell transplantation in the era of surveillance and preemptive therapy. Transpl Infect Dis. 2010;12(4):322-329. doi:10.1111/j.1399-3062.2010.00504.x
[7].中华医学会血液学分会干细胞应用学组. 异基因造血干细胞移植患者巨细胞病毒感染管理中国专家共识(2022年版)[J]. 中华血液学杂志,2022,43(8):617-623. DOI:10.3760/cma.j.issn.0253-2727.2022.08.001.
[8].崔颖慧,许峰. 移植后巨细胞病毒感染的诊疗进展[J]. 中国小儿急救医学,2019,26(1):21-26. DOI:10.3760/cma.j.issn.1673-4912.2019.01.007.
[9].杜珊. 我国社区人群巨细胞病毒、EB病毒感染流行病调查及炎症性肠病合并EB病毒感染的危险因素分析[D]. 中国医学科学院,2017. DOI:10.7666/d.Y3514806.
[10].中华医学会血液学分会造血干细胞应用学组 2022年造血干细胞移植登记报告
[11].王昱,黄晓军. 造血干细胞移植在血液疾病中的应用进展[J]. 中华血液学杂志,2019,40(8):704-708. DOI:10.3760/cma.j.issn.0253-2727.2019.08.020.
[12].Vyas A, Raval AD, Kamat S, LaPlante K, Tang Y, Chemaly RF. Real-World Outcomes Associated With Letermovir Use for Cytomegalovirus Primary Prophylaxis in Allogeneic Hematopoietic Cell Transplant Recipients: A Systematic Review and Meta-analysis of Observational Studies. Open Forum Infect Dis. 2022;10(1):ofac687. Published 2022 Dec 22. doi:10.1093/ofid/ofac687
[13].Karam E, LaPorte J, Sizemore C, et al. Real world outcomes of letermovir prophylaxis in unselected high risk CMV seropositive hematopoietic stem cell transplant recipients. Blood, 2019, 134: 3269. Doi: org/10.1182/blood-2019-131365
[14].Sassine J, Khawaja F, Shigle TL, et al. Refractory and Resistant Cytomegalovirus After Hematopoietic Cell Transplant in the Letermovir Primary Prophylaxis Era. Clin Infect Dis. 2021;73(8):1346-1354. doi:10.1093/cid/ciab298
[15].Mori Y, Jinnouchi F, Takenaka K, et al. Efficacy of prophylactic letermovir for cytomegalovirus reactivation in hematopoietic cell transplantation: a multicenter real-world data. Bone Marrow Transplant. 2021;56(4):853-862. doi:10.1038/s41409-020-01082-z
[16].Liu Y, Mo XD, Han TT, et al. Zhonghua Xue Ye Xue Za Zhi. 2016;37(7):597-601. doi:10.3760/cma.j.issn.0253-2727.2016.07.011
[17].Nichols WG, Corey L, Gooley T, Davis C, Boeckh M. High risk of death due to bacterial and fungal infection among cytomegalovirus (CMV)-seronegative recipients of stem cell transplants from seropositive donors: evidence for indirect effects of primary CMV infection. J Infect Dis. 2002;185(3):273-282. doi:10.1086/338624
[18].Nichols WG, Corey L, Gooley T, Davis C, Boeckh M. High risk of death due to bacterial and fungal infection among cytomegalovirus (CMV)-seronegative recipients of stem cell transplants from seropositive donors: evidence for indirect effects of primary CMV infection. J Infect Dis. 2002;185(3):273-282. doi:10.1086/338624
[19].Salzberger B, Bowden RA, Hackman RC, Davis C, Boeckh M. Neutropenia in allogeneic marrow transplant recipients receiving ganciclovir for prevention of cytomegalovirus disease: risk factors and outcome. Blood. 1997;90(6):2502-2508.
[20].中华医学会血液学分会干细胞应用学组. 异基因造血干细胞移植患者巨细胞病毒感染管理中国专家共识(2022年版)[J]. 中华血液学杂志,2022,43(8):617-623. DOI:10.3760/cma.j.issn.0253-2727.2022.08.001.
更多详情,敬请垂询:
杨芳
IQVIA艾昆纬管理咨询执行总监
fang.yang@iqvia.com
白雪
IQVIA艾昆纬管理咨询顾问
xue.bai@iqvia.com
刘孟嘉
IQVIA艾昆纬管理咨询助理顾问
mengjia.liu@iqvia.com
任映宇
IQVIA艾昆纬管理咨询助理顾问
yingyu.ren@iqvia.com
