在过去的几十年里,电子器件、微纳加工和无线技术取得了巨大发展,显著提升了医疗保健和生命科学研究的质量与效果[1–4]。这些创新与先进的生物材料相结合,推动了微型传感器和生物相容性设备的发展,使其可植入人类和动物模型体内 in vivo,实现诊断、预后评估和生物学研究[5–7]。借助众多可植入设备,科学家已在动物模型中阐明内脏器官的慢性疾病,并在真实患者中进行诊断和治疗[6,8–11]。近年来,柔性与可拉伸电子技术被引入并得到验证,为医疗保健、生物科学发现和医学的未来发展展现出广阔前景[2,7,12]。利用微型可植入系统,科学家已评估和研究了脊椎动物身体中一些难以触及的位置,例如深部脑区、血管内区域、心脏内部,甚至单细胞内部等长期具有挑战性的位置[13–16]。
植入式医疗设备(IMD)用于改善医疗保健,帮助或实现某些功能障碍器官的功能,已有多年历史。它们已被广泛应用于诊断、预后和治疗。根据是否需要电源,植入式医疗设备可分为主动和被动设备。如今,从大脑、耳蜗和视网膜到心脏、肺、膝关节甚至血管、食管和膀胱,全身各部位的多种慢性疾病已通过植入式医疗设备得到治疗。根据十年前的统计数据,全球约有300万人使用起搏器,每年新增60万个起搏器植入。此外,超过6万名患者接受了人工耳蜗植入体治疗[17]。近年来,由于人口增长和更完善的医疗体系,这些数字迅速增加。例如,在美国,仅2009[18]年就有超过23万个新的起搏器被植入。这些事实表明,植入式医疗设备在人类生活中的应用正变得越来越广泛。
为了确保正常运行,大多数植入式医疗设备需要依赖持久且充足的电源,因此几十年来人们已广泛研究了多种用于植入式医疗设备的电源。不同的供能方式可以通过产生电能来替代或补充现有的电池供电,从而实现植入式医疗设备的自主运行。目前面临的主要挑战包括尺寸限制、难以接触、需要持续工作以及生物相容性。
自从1972年首个医疗植入物——起搏器——问世并使用电池[19–23],以来,各种类型的电池已被开发并应用于植入式医疗设备(IMDs)[24–33]。其中,锂基(Li)电池因其高体积能量密度以及相对紧凑的尺寸而成为最受欢迎的电源[28,34,35]。此外,它们具有5至10年的长使用寿命,因此适用于长期应用[36]。另外,利用生物催化剂从葡萄糖或淀粉等可再生可降解材料中发电的生物燃料电池也是潜在的电源[30,35]。酶基生物燃料电池能够在温和条件(20–40 °C且接近pH = 7.0)下运行,产生毫瓦级功率,使其适用于大多数植入式医疗设备,如起搏器、心脏除颤器和药物递送系统。另一种类型是核电池,该技术也于1970年代初推出,曾用于将植入式医疗设备的使用寿命延长至10年以上。其工作原理基于放射性同位素释放的粒子所携带的能量[37]。然而,这类电池在20世纪80年代已停止使用。
由于潜在风险以及医生得出的结论,即植入式医疗设备应至少每十年用新技术更新一次[38]。
人们还提出、研究并开发了其他替代方案,通过利用植入物周围潜在的能量源来产生和收集能量。上述生物燃料电池是极具前景的候选方案,因为它们可以利用血液中丰富的葡萄糖和氧气来产生能量[27,39–41]。此外,脊椎动物的身体及其日常活动本身也是良好的能量来源,例如发热(体热)以及呼吸和移动等运动,这些均可被利用来为植入式医疗设备供电,从而替代传统电池。例如,体内部分与皮肤之间的最大温差为8°C,这足以利用热电发电机产生数百微瓦的电能[42–44]。另一方面,压电发电机已被用于通过压电材料将动能转化为电能[45–47]。
尽管它们能够产生相对较高的功率,达到毫瓦级,但压电发电机通常需要大幅度运动,因此不适用于大多数植入位置[48–50]。静电和电磁机制也已被用于利用身体运动收集能量,但由于其尺寸限制和产生的功率较低,限制了其在实际体内应用中的使用[51–54]。
除了利用宿主产生的潜在能源外,还可以通过外部单元向植入式医疗设备(IMD)提供能量,以实现为电池充电或持续为无电池植入物供电。这种方法可以通过光学方式、超声方式或电磁方式进行。光充电方法包括在植入式医疗设备中使用光伏电池,该电池接收来自激光二极管的功率,激光二极管通常在近红外或红外范围工作[55]。近年来,超声波设备由于其相对较高的效率、紧凑的结构以及对电磁辐射的免疫能力而受到越来越多的关注[56–60]。然而,目前通过人体组织进行感应式电力传输是为各种微型植入式医疗设备提供足够电力的唯一可行解决方案[61]。该方法基于一对天线,通过互感耦合链路实现电力传输。因此,天线设计与方向、工作距离和频率,以及指定功率都需要被考虑。所有这些方法及植入式医疗设备的功率范围在图1中进行了总结。
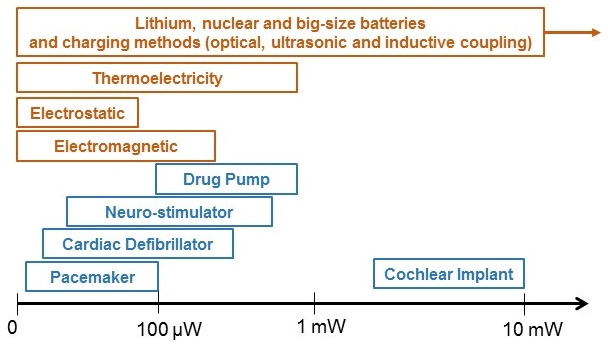
在这篇综述论文中,我们介绍了为有源植入式医疗设备供电的方法,并对每种方法进行了深入的讨论。这些方法分为两大类:(1)可独立工作的植入式医疗设备,无论是否使用一次性电池或可持续供电;(2)可通过外部单元传输电源的植入式医疗设备,这类设备可以是基于电池或无电池的。图2展示了这两类方法。讨论部分首先概述了植入式医疗设备的最终目标,随后深入探讨了最流行的方法,即感应耦合。
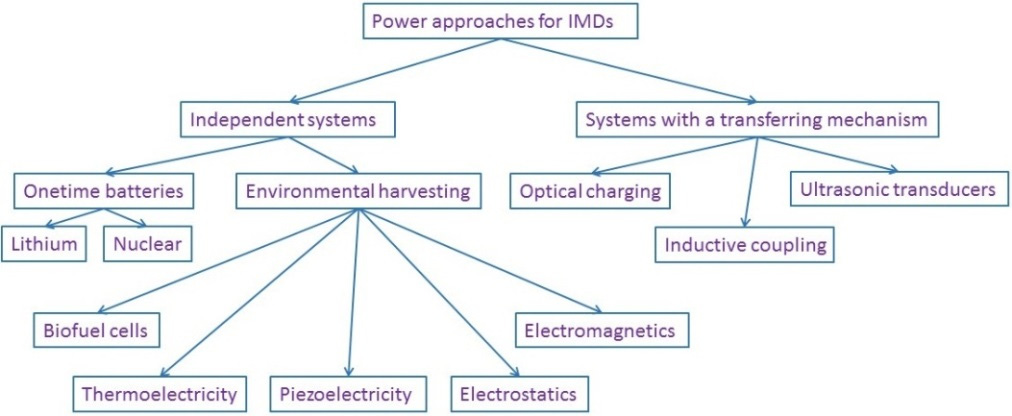
2.1. 独立系统
第一个电池由伏特于1796年发明,自那以后,多种类型的电池被发现并应用于人类生活的各个方面[62]。一般来说,电池以化学物质的形式储存能量,这些化学物质能够产生电能。电池包含阳极、阴极和电解质,使离子能够移动从而形成电流。根据电池性能,电源能力可分为三类(低倍率、中倍率和高倍率)。尽管定义尚不明确,但低倍率电池应能提供100微安的恒定电流,而高倍率电池则能在10秒内提供至少5瓦的脉冲功率。因此,中倍率电池可以填补这一差距。在植入式医疗设备中,起搏器使用低电流,神经刺激器和药物泵需要中倍率电源,而植入式除颤器/转复器(ICDs)则需要极高功率以及更长的使用寿命[32]。
2.1.1. 锂离子电池
通常,锂离子电池采用锂金属阳极与阴极系统组合的形式开发并出现,其中阴极系统包括碘(Li/I2)[2,6,24,63,64], 、二氧化锰(Li/MnO2)[7,12,65,66], 、一氟化碳(Li/CFx)[67–70], 、氧化银钒(Li/SVO)[71–73]或混合阴极(Li/CFx‐SVO)[29,32,64,74,75]。作为人工耳蜗植入体、起搏器、心脏除颤器或药物递送等长期应用的可靠电源,这些锂离子电池已被广泛应用,可根据不同类型植入式医疗设备的需求提供从微安到安培范围内的适当电源水平 [26,29,32]。
其中,锂/碘(Li/I2 )电池已被证明在植入式起搏器应用中比其他电池更安全、更可靠,因此在过去40年中已被大多数制造商采用[27]。锂/碘(Li/I2 )电池的放电电压高达3.6 伏,相当于三倍的
镍基电池产生的电压。其能量密度可达210 瓦时/千克,可为心脏起搏器供电数年。此外,通常情况下,测量Li/I2电池的剩余能量比其他锂基电池更容易,从而为植入式医疗设备[27]更换电池提供了充足的时间。另一方面,由于锂/五氧化二钒电池的能量密度超过300 瓦时/千克,在过去30年中主要被用于植入式心律转复除颤器。金属银的存在也显著提高了电子导电性[76]。
在中等能量范围内,采用亚硫酰氯阴极(Li/SOCl2)的系统已广泛应用于神经刺激器和药物泵。
材料研究的最新进展催生了一类新型锂基电池,即柔性锂或锂聚合物电池[77,78]。尽管其在柔性电子器件和可穿戴消费设备中的优点毋庸置疑,但由于尺寸方面的障碍以及潜在毒性相关问题,其在植入物中的进一步应用仍然受限。
2.1.2. 生物燃料电池
一般来说,生物燃料电池是基于涉及生化途径的电化学反应将生化能转化为电能的设备 [30]。生物学与电之间的联系最早由伽伐尼在1791年通过对青蛙腿的实验发现。他发现当施加电火花时,死青蛙腿部的肌肉会发生抽搐。燃料电池的概念于1839年由格罗夫首次展示,他完全逆转了水的电解过程,成功将氧气和氢气重新结合生成水,并有趣地产生了电流[79]。微生物燃料电池(MFC)的发展始于1911年,当时波特发现,当将铂电极插入大肠杆菌培养物中时,可在0.3–0.5 伏特电压下产生0.2–0.5 毫安的电流[80],这表明利用微生物发电具有潜力。该设想于1931年由科恩实现,他构建的生物燃料电池可提供2 毫安的电流和35 伏特的电压[30,81]。
在燃料电池中,阳极发生氧化反应,阴极发生还原反应。氧化反应释放的电子通过外部电路流向阴极,形成电流[30]。同时,质子通过质子选择性交换膜迁移至阴极(图3)[27]。
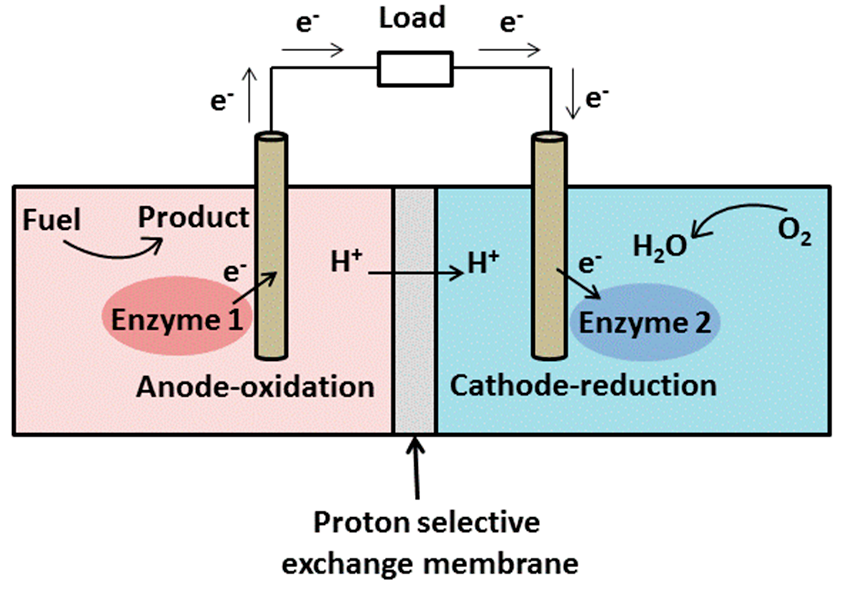
根据所使用的催化剂,生物燃料电池可分为微生物燃料电池(MFC)和酶生物燃料电池(EBC);而根据电子从阳极移动的路径,
阴极,我们可以区分直接或非直接电池[27,30]。例如,燃料可以通过以下反应从血液中的葡萄糖和氧气获取:
At anode: C6H12O6 → C6H10O6+ 2H++ 2e−
At cathode: O2+ 4H++ 4e− → 2H2O
对微生物燃料电池(MFCs)的兴趣始于1960年代,起因是美国航天计划在太空飞行的废物处理系统中寻求可能的电源技术[30]。用于植入式医疗设备(IMDs)的微生物燃料电池最早于1960年代启动,当时使用无细胞酶基燃料电池为可植入人工心脏供电[30,82]。在1970年代,研究人员探索了以葡萄糖为燃料、氧气为氧化剂的酶基生物电池(EBCs),用于为植入式医疗设备供电[27,30] ;自那时以来,已提出多种方法和改进措施,以提升其性能并针对特定应用 [28]。2003年,Mano及其同事报告了一种微型化生物燃料电池,可在葡萄中植入运行。他们能够在0.52伏特电压下产生2.4 μ瓦特的功率,这对于紧凑型植入物的应用而言非常有前景[83]。
生物燃料电池具有多项优点,包括利用自然界中现有的可回收材料、反应所需的适中操作条件,以及生物燃料电池与人体之间的良好生物相容性[31]。然而,仍存在一些挑战。首先,长期维持生物催化剂的活性较为困难,而外科干预显然不是理想的选择。其次,生物燃料电池输出的微瓦级功率限制了其在广泛领域的应用。最后,尽管它们具有高度生物相容性,但不可避免的生物污损仍可能发生,从而损坏设备或危害患者[27]。
2.1.3 核电池
在核电池中,能量通过放射性同位素发射的粒子所携带的能量转化为电能。这一过程可以通过多种方式实现。例如,一些利用放射性同位素发射粒子产生的电势差,一些利用发射的粒子束引起电离所产生的电势,另一些采用荧光材料激发的光电转换,其余的则利用辐射的热能。
核电池的优点在于,其使用寿命(>15年)比其他所有同类产品更长,并且输出能量极为稳定,不受环境因素(温度、压力和电场)影响。例如,美敦力公司(美国明尼苏达州明尼阿波利斯)生产的Betacel,体积为1.8 毫升,高度为1.02 厘米,直径为1.52 厘米,可提供50 μW的电源 [27]。此外,只要保持密封,其安全性已得到证实,但潜在的放射性危险及其高昂的成本仍使其难以被接受[32,33]。
2.1.4. 热电性
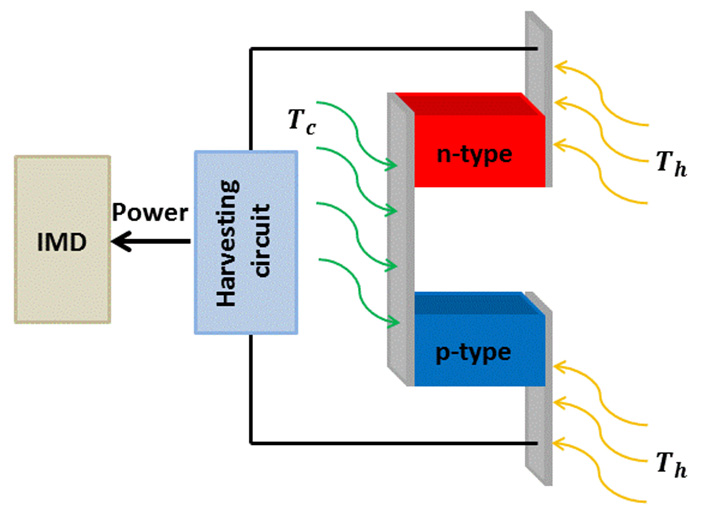
可以利用人体内的温差通过热电效应来获取电能。自然情况下,人体不同位置之间存在温度差异,从而形成温度梯度。当在热电模块上施加温度梯度时,由于塞贝克效应(图4a)[84],材料两端会产生电势差。由于
人体是一个无限的热能来源,因此这些发电机的寿命自然也是无限的[85–88]。然而,人体内的温度梯度相对较小,难以实现显著的功率输出。由于热电发电机是一种热机,其效率与卡诺效率成正比,卡诺效率定义为[89]:
ŋ ൌ 1െ ܶܶ ൌ ܶܶെ ܶ (1)
其中,ŋc为卡诺效率,Th和Tc分别表示热端和冷端的开尔文温度。热电发电机通常由半导体材料制成,最常见的材料是碲化铋(Bi2Te3)和多晶硅锗薄膜(poly‐SiGe)[90]。热电模块通常由n型掺杂和p型掺杂的半导体热电偶组成,这些热电偶在电学上串联,在热学上并联。
1999年,斯塔克和斯托多尔报道了一种尺寸为0.19 cm3的热电发电机,在5 K和10 K的温度梯度下分别可产生1.5 微瓦和5.8 微瓦的输出功率[91]。该设备通过在75 微米厚的聚酰亚胺 (Kapton)(杜邦,威尔明顿,特拉华州,美国)基板上溅射具有热电效应的材料Bi2Te3 ,从而形成热堆结构。最终的集成密度为11.9个热电偶/mm3。到了2004年代,斯特拉斯等人介绍了他们的工作,即使用沉积在多晶硅基板上的多晶硅锗材料开发微加工CMOS热电发电机。他们在5 K的温度梯度下,实现了1 cm2尺寸的发电机输出功率达到1 微瓦[92]。事实上,人体内部与皮肤表面之间的最大温差约为8 K,因此最大输出功率约为180 μ瓦特/cm2[93]。由此可见,热电发电机仅能为需要低微瓦级电源的植入式医疗设备提供足够的电力。为了提高输出功率,需要以适当方式级联大量热电偶,但这将面临尺寸、可靠性和生物相容性等方面的问题[84]。
2.1.5. 压电性
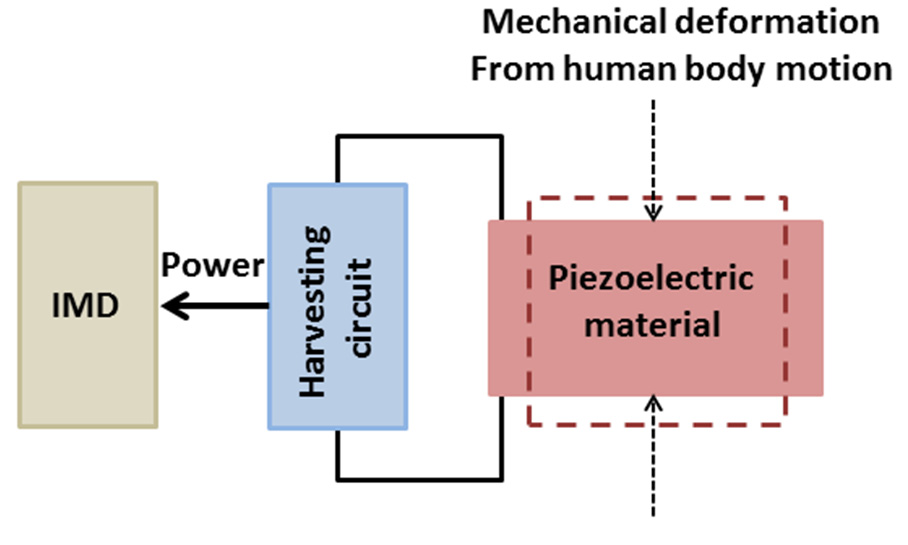
压电现象于1880年由法国物理学家雅克和皮埃尔·居里[94]发现。可以验证,某些材料通过压电效应,在受到施加的机械应力时会产生成比例的电极化。迄今为止,大量压电材料已被用于为各种应用产生能量[95,96]。其背后的物理现象基于以下事实:当某些固体材料中的电荷在受到机械变形时将
被诱发(图4b)。因此,压电换能器可以利用人体运动产生的机械能[45–47]。人体运动可分为两类:连续运动(如人体呼吸和血液流动)和非连续运动(如行走和手部动作)。多个研究团队已探讨了利用非连续人体运动进行压电能量收集的可能性[97–99]。压电换能器可集成于关节、全身质心运动、肌肉抽搐以及鞋子等移动位置[98,100–103]。脚踝、膝盖、臀部、肘部和肩部的运动分别最多可产生69.8 瓦、49.5 瓦、39.2 瓦、2.1 瓦和2.2 瓦的功率[98]。另一方面,从血流或呼吸获得的连续运动所提供的功率相比使用非连续运动的压电能量收集器要低。例如,在血流环境中,一块半径为5.62 毫米、厚度为28 μm的压电板所能产生的最大功率为0.33 μ瓦 [104]。显然,压电收集器是为植入物供电的良好候选方案,但需要显著的运动才能产生可观的功率,因此实际可植入的位置受限(即膝盖、肘部、脚部)。例如,Kymissis等人在1998年的研究中,通过将压电换能器集成于鞋跟实现了1 瓦的输出功率[46]。然而,如何在体内实现并收集此类系统的能量仍是亟待解决的关键问题。此外,小型化和生物相容性问题始终是最主要的挑战。
2.1.6. 静电发电机
静电发电机通过静电感应产生电能,这种感应基于保守的库仑力所产生的静电势能[105]。它们的设计利用机械运动,在换能器的移动部件受到电场作用时诱导出电能。一种常见的静电发电机结构由两个导电板组成,导电板之间通过空气、真空或电介质绝缘体(电容器)实现电隔离,并具有相对可移动性(图5a)[53]。由于人体运动引起的一个可移动电极的移动或振动,导致电容器两电极之间的距离发生变化。
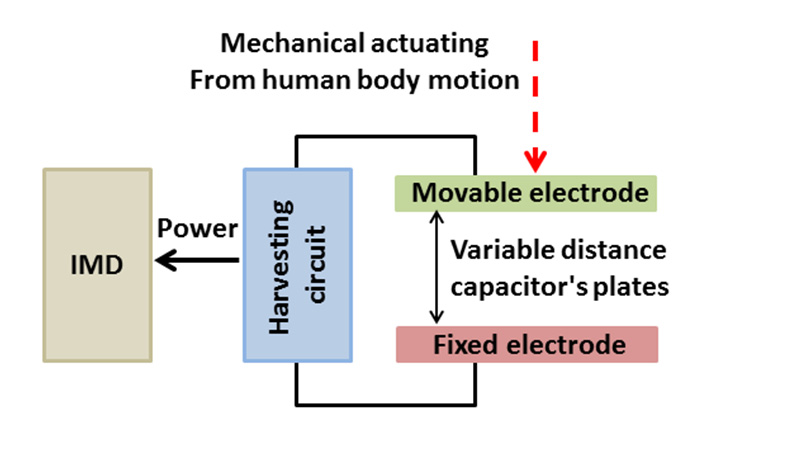
静电能量收集器有两种工作模式:恒定电荷模式和恒定电压模式[106]。极板通过外部电源(如电池)充电。此外,根据驱动方向的不同,静电发电机可分为三种类型:面内间隙闭合、面外闭合和面内重叠[107]。
平面内间隙闭合技术相比其他驱动技术可提供最高的输出功率。静电发电机能量收集系统可通过硅微加工制造技术构建,并且能够很好地与微电子电路及其他技术集成,因此成为植入式医疗设备的理想候选方案。基于微机电系统(MEMS)的技术实现了微型化尺寸,使得这些发电机可植入人体内部[52,108]。最近,已有若干关于利用静电能量收集系统为生物医学设备供电的研究报道。例如,有研究报道了一种利用心室运动和心跳为心脏起搏器供电的静电发电机,分别可产生36 μW和58 μW的功率[54,109]。此外,Meninger et al.开发了一种基于MEMS技术的静电发电系统,能够产生8 微瓦的功率。在该研究中,苗及其同事实现了一种非共振型基于MEMS的静电发电机,从而可在宽范围的激励频率下提供操作灵活性。他们在30 赫兹频率、0.1 米/秒移动条件下获得了80 微瓦的输出功率[108]。总体而言,由于静电发电机具有高输出阻抗和高电压特性,导致可用电流较小,因而不太适合作为电源设备。此外,产生的能量通常较低,且这些发电机通常需要额外电压源来初始充电电容器,这是该技术的主要缺点。
2.1.7. 电磁发电机
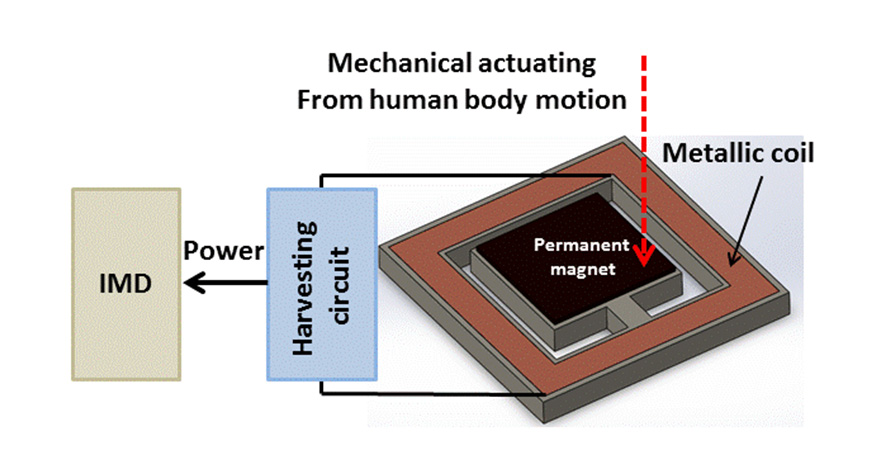
电磁发电机基于法拉第‐诺依曼‐楞次定律来收集能量,该定律指出线圈与永磁体之间的相对运动会产生时变磁通量,从而产生电压。这可以通过两种方式实现:(1)利用相对运动而发电系统保持固定;(2)利用刚体运动,并通过发电机上质量块的惯性力实现[110]。通常,电源是通过磁体和线圈的相对移动,或由于磁场的变化而产生的[51,111]。因此,所产生的电能大小可能是磁场强度、相对运动速度以及线圈匝数的函数。与基于压电或静电换能器的方法类似,电磁发电机利用人体运动来产生电源(图5b)。
人类的低频和不规则运动使得电磁技术适用于为植入式医疗设备供电。例如,心肌以0.5 和2赫兹之间的频率重复收缩,可产生40–200 μ瓦特的功率[112,113]。Roberts等人研究了一种采用MEMS技术的电磁发电机,以在临床试验中增强起搏器电池的电源[114]。腹部在呼吸时以0.3赫兹的频率运动,通过体积为16立方厘米3[115]的电磁发电机可产生约1.1毫瓦的功率。利用人体行走,尺寸为2.6毫米2的电磁发电机可产生 400 μ瓦特[116]的功率。高性能体磁体、多匝线圈和宏观尺度线圈均易于获得;然而,该方法所使用的MEMS制造技术的主要挑战在于平面磁体的较差性能[51]。此外,电磁发电机产生的功率低于压电发电机所获得的功率。
尽管独立系统能够提供带来舒适性并避免复杂性的解决方案,但它们在可靠性、低输出功率(如微生物燃料电池、热电性)以及可能引起毒性且无法实现生物相容性方面表现出不足。随着植入式医疗设备与智能设备之间通信需求的不断增加,带外部单元以持续传输能量的系统因此受到关注。电源可以通过人体组织以光学方式、机械方式或电磁方式进行传输,这些方法将在以下章节中介绍和讨论。
2.2.1. 光充电
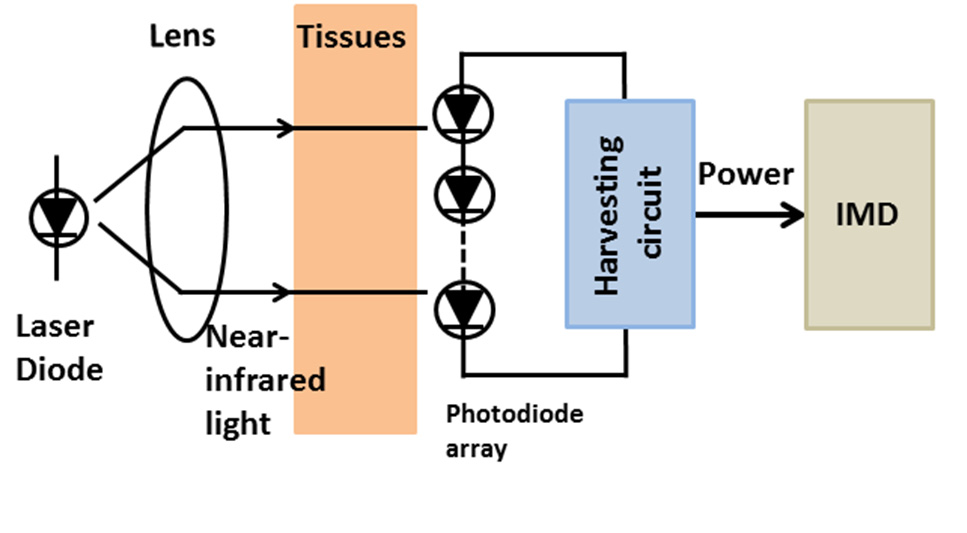
光充电方法利用植入物中集成的光伏电池。电源可以通过近红外(近红外)或红外区域的激光二极管传输,并由光伏电池阵列接收[55,117]。光通常与生物组织的相互作用较弱。根据波长的不同,辐射能够深入生物组织内部。光伏电池阵列将接收到的辐射转换为电流,以对植入式医疗设备进行充电或供电(图6a)。
光充电方法;和 (b) 超声波换能器)
光伏电池由大带隙半导体的 p‐n 结构成。当入射光子形成电子‐空穴对时,该结可被光学方式充电,从而实现电子迁移率。如果连接了负载,自由电子将流经负载,然后返回到电池中空穴所在的位置[118]。这些设备能够产生数百微瓦量级的电源。面积为 2.1 cm2 、以 22 毫瓦/平方厘米的功率密度充电 17 分钟的光伏电池阵列,可产生 20 μA 电流,足以使起搏器运行 24 小时[119]。采用这种方法,不仅可以传输电源,还可以通过光链路传输信息数据[120]。然而,在充电期间,激光照射可能使皮肤温度升高 1.4 °C,这可能会引起副作用[121]。此外,该方法仍存在一些缺点,例如尺寸较大和效率较低。
2.2.2. 超声波换能器
近年来,由于该技术在效率、尺寸以及对电磁辐射的抗干扰性方面相较于其他技术具有优点,因而受到越来越多的关注[56–59]
其他设备[60]。超声波换能器通过外部超声源机械激发,该外部超声源使用可在电容模式或压电模式下工作的超声波换能器[122,123]。植入式超声波发电机从外部单元发射并接收到的声波中产生电源。入射的声波分别通过电容式超声波换能器(CUT)的电容变化或压电式超声波换能器(PUT)的压电效应转换为电压(图6b)。可以利用MEMS技术制造超声波能量收集系统,因此其紧凑性使其适用于植入式医疗设备。然而,由于高电压要求,CUT不适用于 in vivo操作。另一方面,PUT具有前景,因其利用压电材料将接收到的声波转换为电源。1988年,Cochran等人报道了首个植入式超声电源,该电源在外部超声源频率为2.25兆赫、输入电压为10–20伏特的条件下工作,以激发一个5 × 5 × 0.9毫米3压电陶瓷换能器。该设备可产生1.5毫瓦/平方厘米的输出功率2[124]。除了传输电源外,超声系统还可用于向植入式医疗设备发送数据[125]。此外,一种直径为3.5毫米的压电陶瓷换能器被植入活体组织内,并由一个直径为12毫米的外部圆形发射器在2.25兆赫频率下激发,能够产生高达1.5毫瓦/平方厘米的输出功率2 ,足以驱动外周神经微刺激器[126]。总体而言,这种方法的主要优点是易于选择工作波长。长波长超声波可更深入地穿透人体,但会覆盖非期望区域;相反,短波长波可聚焦于期望区域,但无法穿透到所需的深度[127]。尽管有这些优点,超声波电源传输仍面临许多挑战。通常认为使用超声波电源是安全有效的,但在某些情况下,由于空化效应引起的发热导致组织细胞核内的气体受热,会产生灼烧感等身体疼痛,进而引发呼吸困难、头晕、恶心和定向障碍[127]。
光充电方法;和 (b) 超声波换能器)
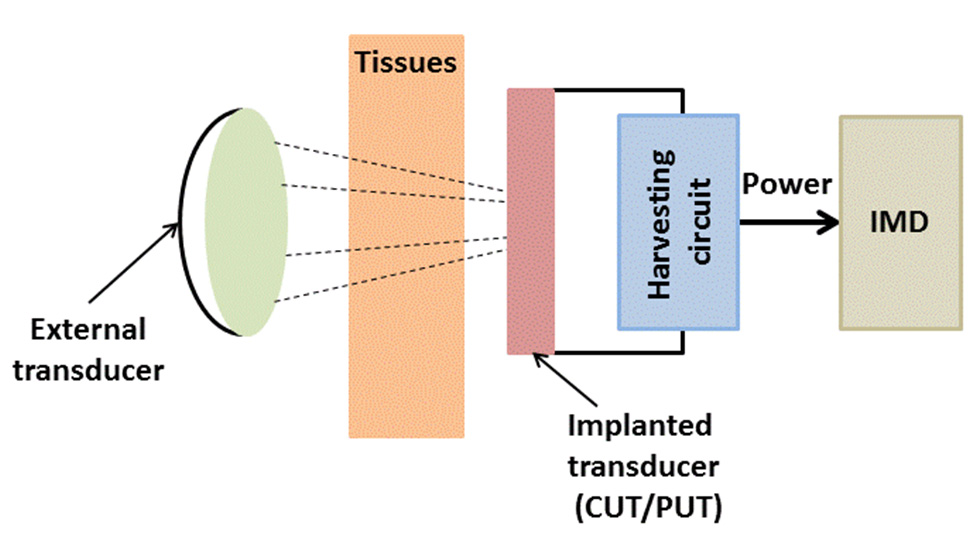
2.2.3. 感应耦合
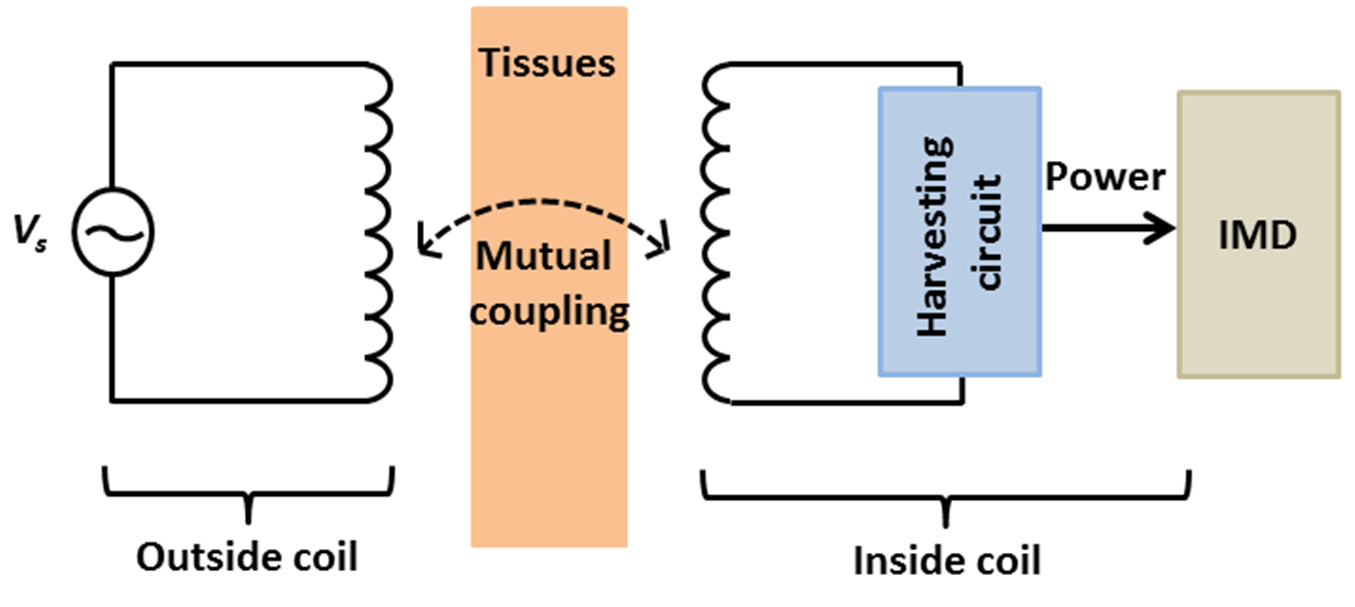
自迈克尔·法拉第发现电源可以通过磁感应在空气中传输以来,已有180多年的历史。1914年,特斯拉[128]首次报告了基于两个环路磁耦合的无线电力和数据传输。近年来,尤其是在过去十年中,感应耦合被广泛研究用于为植入式医疗设备供电。其原理基于两个线圈之间的互感,其中一个位于体外,另一个则集成在植入设备中。当外部天线发射变化的电磁信号时,接收线圈中会产生感应电压(图7)。无线功率效率取决于谐振频率(或工作频率)、距离、对准以及发射器和接收线圈之间的耦合匹配[5,6,129–132]。此外,感应技术还可用于在不使用射频(RF)发射器或接收器的情况下实现体内外双向数据传输,数据速率可达数百千比特每秒[5,6,121,133]。
Parramon等人在其研究中开发了一种感应耦合电源,在10 MHz载波频率下可产生19 毫瓦的功率。该电源用于为植入兔肌肉中的肌电图(EMG)记录微系统供电。内部线圈的直径、外部线圈的直径以及两线圈之间的距离分别为10 毫米、20 毫米和15 毫米[134]。另一个例子是利用感应耦合为无线摄像胶囊提供电源,以非侵入方式检查小肠,载波频率为1 MHz[20]。该电源最高可产生150 毫瓦的功率,两线圈之间的距离为205 毫米。内部线圈的尺寸为10 × 13毫米2。2004年,Catrysse 等人提出了一种感应链路电源系统,在台面实验中可在3 厘米距离上传输50 毫瓦的功率,工作频率为700 千赫[135]。此外,2007年,Ghovanloo和Najafi展示了 一种片上系统(SOC),通过将专用集成电路(ASIC)设计与片外元件(LC谐振电路;滤波器)结合,在5/10 MHz频率下可在5 毫米距离上传输50 毫瓦的功率[136]。
感应耦合方法中存在若干关键因素,例如错位、植入物天线的尺寸、未知的副作用以及由于组织吸收导致的有限载波频率,因此低兆赫范围(0.3–30 MHz)被广泛使用[5]。有关此方法的更多信息,读者可参考讨论部分,其中对感应耦合进行了详细讨论。
3.1. 植入式医疗设备:作用与未来展望
在过去的十年中,随着先进技术的迅速发展,医疗保健在多个方面发生了变革。纳米技术和无线技术已将医学诊断、监测和干预转变为个体化医疗[6,137,138]。自我护理、电子护理、移动医疗和物联网(IOTs)的概念相继出现,改变了医生与患者的传统角色。人们能够利用创新设备每天监测自身健康状况,而远在数千英里之外的医护人员则可对大规模医疗数据进行持续评估和诊断。在许多情况下,设备需要植入体内并安全稳定地停留一段时间;因此,对植入式医疗设备(IMDs)提出了新的期望,即植入物需能够与外部单元通信,以实现实时追踪、感知、诊断和治疗。为实现这一目标,无论设备是主动式还是被动式,充足的电源都成为必不可少的条件。
在这种即将到来的场景中,不仅需要电源来运行植入物,还需要为高功耗的无线通信供电,这将同时耗尽植入式医疗设备的电池,从而缩短设备的寿命。图8描绘了未来植入式医疗设备的概念示意图。根据这些预期,植入式医疗设备(1)可以从外部单元获取电源,例如当植入式医疗设备位于腹部时可使用可穿戴腰带(4),当植入式医疗设备位于大脑/头部时可使用帽子(2)。如果在手臂/手部位置有皮下植入式医疗设备,则可通过腕部设备(3)供电。对于无线通信,植入式医疗设备可以直接将数据发送到智能手机,或通过外部单元传输。可应用算法对数据进行过滤、解释和分类,以供诊断、存储或远程医护人员进行实时检查。需要大数据处理和移动云系统来支持基础设施。我们设想这将是未来医疗保健的模式,能够显著节省时间与成本,为社会提供更高的效率和效益。显然,在这一理想图景中,可靠的微传感器和通信技术、持久的电源和系统,以及智能的算法和设计至关重要。此外,还需改进安全性、实用性、时尚性和舒适性等问题,以便将尖端设备不仅带给患者,也带给公众。
3.2 植入式医疗设备电源方案:优势与局限
尽管仍存在一些尚未解决的挑战和问题,植入式医疗设备(IMD)在医疗监护和诊断等医疗应用中已变得有用且普及。例如,一项2009年开展的调查涉及1,002,664台起搏器和 328,027台植入式心律转复除颤器(ICDs),包括新植入物和更换设备,发现美国数量最多,分别为264,824台起搏器和133,262台ICDs[18]。大多数情况下,IMD使用不可再生的电源,即电池。迄今为止,在确保安全并采用适当封装的前提下,当考虑尺寸、功能和运行时间时,电池仍然是IMD最可靠的电源。与电池相比,生物燃料电池和热电性等独立系统最常见的问题是输出功率较低,而无线供电系统则会带来复杂性并引起不适,且所有可能的方法均无法提供在严格的医疗领域中可接受的可靠性水平。
然而,为慢性或终身植入式医疗设备提供电源的可持续能源仍然备受关注。还有另一类情况是难以接触植入位置(例如血管内应用),因此更倾向于使用可生物降解植入物。近年来在开发创新生物材料方面的新努力[139,140]已经实现了这些,但需要定义一种使用可降解材料的无电池电源解决方案。表1简要总结了用于植入式医疗设备应用的各种供能方式的优缺点及发电情况。
独立系统
带外部单元的系统
在即将到来的移动健康和物联网时代的典型植入式医疗设备中,关键组件将包括高灵敏度生物传感器、低功耗集成电路、低功耗可靠无线通信,以及显然充足的电源。尽管纳米技术和材料方面的最新进展[2]已实现了更小、更灵敏且能耗更低的传感器,以及功耗更低、体积更紧凑的电子器件,但日益增长的与其他设备及可移动云进行通信和交互的需求,使得新一代设备需要更高的功率来运行。因此,目前面临一个尚无绝对解决方案的两难困境。尽管科学家们已投入巨大努力来研究各种方法,无论是利用人体能量还是远程传输电源,所提出的解决方案仍然无法提供足够的能量来驱动体积越来越小、功能越来越多的设备。起搏器中有超过80%的体积被电池占据,这一现象一直是该领域科研人员面临的真正困扰和挑战,更不用说近年来移动健康应用对无线通信的需求了。
最近,人们提出了许多使用DNA[142–144]的新型生物传感机制,这意味着在不久的将来,电子器件与生物元件相融合的混合系统将成为可能。此类系统无疑需要极低的功耗,但能够带来最高水平的灵敏度和生物相容性,因为它们在我们的生物环境中不会被视为异物,更不用说还能最大限度地减少生物污染和炎症反应。然而,由于无线数据通信仍然是必需的,因此棘手的电源问题仍未解决。尽管最近已发明了大量低功耗且更高效的无线通信方法和协议,但其机制并未改变,仍由无线芯片、常规放大电路、滤波器和转换器在某一频率下处理电磁波。这将始终对紧凑型植入式医疗设备造成巨大负担。
除了用于人类的植入式医疗设备外,可植入设备已广泛应用于动物模型的生物学研究和药物筛选。尽管其安全性问题与用于人类的设备不可相提并论,但大多数动物模型(i.e., 小鼠、斑马鱼和大鼠)由于尺寸小得多而带来更大的挑战。因此,在克服动物模型障碍过程中获得的经验可以应用于植入式医疗设备。例如,近期为斑马鱼和新生小鼠开发无线心电图(ECG)监测系统以阐明心脏再生的研究[145,146]可能为用于人类的可植入设备提供解决方案,其中电源采用感应传输,而数据则通过光学方式发送。
3.3. 感应耦合:可能性与挑战
近年来,基于共振的感应链路无线供电因其能够提供充足电源、具备高可靠性以及可与其他电子元件集成等优势,在多种应用中得到了广泛研究。此外,该感应链路还可用于数据传输[5,6,136]。在医疗设备领域,为满足特定应用需求,研究人员提出了众多在设计、材料和电路方面的创新方案。对于植入式医疗设备(IMDs),其工作频率通常位于低兆赫(MHz)或千赫(KHz)范围,以最大限度地减少组织吸收功率,从而避免组织发热和副作用[6,135]。已有大量研究致力于提高常规双线圈系统的能量传输效率(PTE)[20,23,34,147–149],,其中对线圈几何结构、线圈尺寸、匝数和线圈损耗进行了优化分析。近年来,MEMS技术与先进材料的发展使得可在柔性或刚性基板上制造微型线圈,并实现与其他电子元件的单片集成。然而,线圈尺寸减小导致耦合能量降低的问题仍未解决,同时还面临另一挑战:所制备线圈的金属薄膜较薄(通常为<1 μm),会导致品质因数(Q)极低,进而造成PTE低下。本课题组近期提出一种解决方案,采用低温共烧陶瓷(LTCC)技术将螺旋线圈在多层结构中级联(LTCC中最多可达10层),以提升PTE(相关结果即将发表)。利用LTCC技术,性能得以改善,不仅通过级联增加了匝数,而且由于厚金属层(>8微米)实现了更高的Q值。尽管低温共烧陶瓷(LTCC)能够提高功率传输效率(PTE),并具备与电子器件以及芯片实验室应用集成的能力,但其硬质材料和高加工温度限制了其在多种植入式医疗设备中的应用。
在实际场景中,大多数解剖表面高度弯曲,并且大多数器官在日常活动中相对可移动,这就要求植入式医疗设备具备柔性并保持功能。然而,柔性线圈天线的电感会随着机械环境信号的变化而改变,从而导致植入式医疗设备中LC谐振电路的谐振频率发生变化。如果变化显著,功率传输效率(PTE)将大幅降低。因此需要实施自适应机制,以确保两侧的谐振频率相匹配[149–151]。但这可能会增加空间受限的植入式医疗设备的组件数量。另一个实际问题是错位,该问题已被广泛研究[5,35,152]。对于附着在胃等运动器官上的特定植入式医疗设备,位置和角度错位变得尤为关键。最近的研究表明,采用螺旋结构的发射天线能够产生较大的波束尺寸,从而最大限度地减少错位问题[153]。尽管如此,错位问题具有案例依赖性且不可避免,因此在实际使用前需要在模拟环境中进行充分的校准和研究。
与传统的双天线系统不同,多输入多输出(MIMO)系统已被研究[154–156]。显然,由于磁场持续处于激活状态,可同时使用多个植入式医疗设备,但这会导致复杂的情况,因为它会影响任意两个天线之间的互感,进而影响功率传输效率(PTE)。此外,如[157]中所述,放置“中继器”以提高功率传输效率(PTE)和传输距离也较为困难。最有可能带来改善的情况是在一个植入式医疗设备中使用多个发射器和一个接收器[156]。例如,可在躯干周围布置两个或更多的发射器,以增加输送至植入式医疗设备的功率。然而,在用户不可避免地进行日常活动的动态情况下,要实现相长叠加和场优化仍然十分困难。
如果不提及电磁场[41,158]在组织中引起的生物效应,将是不恰当的。尽管已有相关研究,但关注点主要集中在发热产生的急性效应上,而长期健康问题则是阻碍患者和公众接受并使用采用感应耦合的植入式医疗设备的担忧所在。
有限的使用寿命和生物相容性是所有用于植入式医疗设备的供能方式中最严重的问题。为了替代现有的基于电池的系统以驱动植入式医疗设备,研究人员已广泛探索了各种替代方法。为此,本综述旨在实现双重目标:(1)总结用于植入式医疗设备的各种关键供能方式,并突出每种方法的优势与不足;(2)提出关注点,并探讨植入式医疗设备在未来医学和医疗应用中的发展趋势。本文回顾并讨论了利用独立系统以及外部单元获取能量的所有方法。独立系统方法利用体内环境能量(如体温和身体运动)来产生电能,从而为植入式医疗设备供电。这些方法基于热电、压电、电磁和静电效应,可提供无限寿命,但输出功率低以及可植入位置受限是主要挑战。另一方面,使用外部单元的供能方式(如光充电、超声波换能器和感应耦合)能够传输能量和信息数据,并可实现对不同身体位置的植入式医疗设备进行供电。德谟克利特曾说过:“宇宙中存在的一切都是偶然与必然的产物”。受此启发,我们充分理解了每种植入式医疗设备供能方式的重要性和意义,并高度赞赏科学家们为推动社会更美好生活的道路上所做出的宝贵贡献。
