指南共识 l 2020儿童继发性骨质疏松症专家共识:诊断和治疗(全文)**

2020专家共识
儿童继发性骨质疏松症
诊断和治疗
编译:高龙/陈康
CK经典文献翻译组
高龙 译者简介
精华推荐:
由于这些原因,西班牙儿科风湿病学会的成骨不全和儿童骨质疏松症工作组呼吁制定指南以规范这种疾病的临床实践。
结论:
综上,我们根据现有证据和专家临床经验,在此为预防、诊断和治疗继发性儿童骨质疏松症提供指南。我们相信它可以成为该病临床实践标准化的有用工具。预防措施、及早诊断和适宜的治疗不仅对改善儿童和青少年骨骼健康至关重要,而且对他们将来成年的骨骼健康也很重要。
关键词:继发性骨质疏松,儿童,骨密度减低
背景
骨质疏松症是一种以骨量减少和骨组织微观结构改变为特征的疾病,导致骨脆性增加,从而增加骨折风险[1]。目前,骨质疏松症是工业化国家的一个公共健康问题,影响到欧洲约30%的女性和8%的50岁以上男性[2]。虽然通常认为骨质疏松症是一种成人疾病,但越来越清楚的是它可能源于儿童和青少年[3]。骨基质矿化发生在生命的这些时期,因此患者在生长阶段结束时达到峰值骨量。如果峰值不能达到最佳,将促进成年后骨质疏松症发生[3]。
此外,儿童骨质疏松症的发病率增加的原因还有:慢性病患者存活率增加以及可能损害骨骼的药物使用的增加[4]。
2013年,国际临床骨密度学会的官方立场考虑到关于诊断儿童骨质疏松症的两种可能情况[5]:
此外,他们的指南指出,Z值高于-2不能排除骨脆性增加的可能,特别是那些患有易发生继发性骨质疏松症疾病的患者。
目前,在儿科,人们对该病越来越感兴趣。然而,最近对儿童骨质疏松症定义的修订[5,6],以及缺乏关于其诊断和治疗的指南或国家共识,导致该病的治疗方案存在很大差异[7]。
由于这些原因,西班牙儿科风湿病学会成骨不全和儿童骨质疏松症工作组(西班牙语缩写为SERPE)已经呼吁需要制定指南以规范该病的临床实践。
方法
设计:
采用科学证据和共识(基于临床经验及现有科学证据)的定性综合,来制定研究设计。
制订过程:
准备工作由成立一个由11名医生(6名儿科医生和5名风湿病学家)组成的专家小组开始。他们都是SERPE的成员,在儿童继发性骨质疏松症的诊断和治疗方面有经验。
研究协调由其中一名医师承担。
专家小组就文件的核心内容达成了共识,该文件由以下八个部分组成:
-
何时应警惕骨质疏松
-
如何预防
-
实验室筛查
-
影像筛查
-
治疗:钙和维生素D的补充
-
治疗:双膦酸盐(BPs)
-
随访
-
糖皮质激素性骨质疏松症(GIOP)
指定一名或两名专家,在一名风湿病学专家和一名方法学专家的协助下负责每一部分的文献综述。
修订后,负责文献综述的每位专家根据证据(如果有的话)或他们自己的经验,就每一部分提出建议。
随后,小组成员举行会议讨论并起草建议。使用牛津循证医学中心(CEBM)系统确定每一部分的证据水平。为此,风湿病学家和方法论专家提供了指导。对证据水平为四级或五级的建议进行了德尔菲调查。该调查发送给SERPE成员。包括所有一致性高于或等于70%的建议。
结果
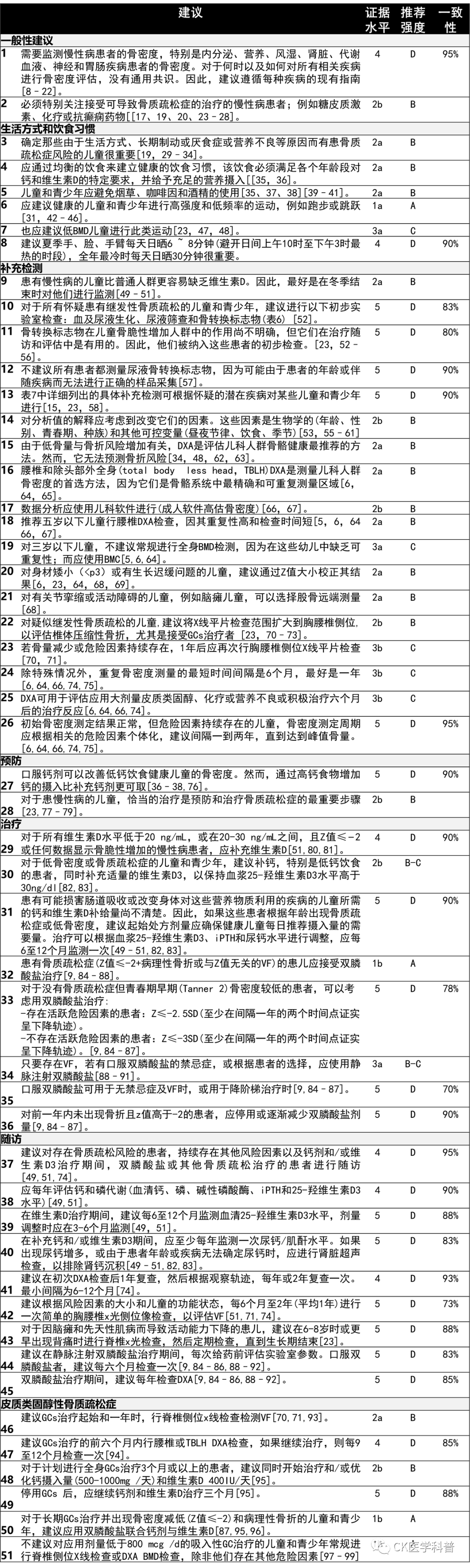
共获得51项建议(表1),分为八个章节。其中24项证据的等级为4或5,因此进行了德尔菲调查。问卷以电子方式提交,收到的回复率为40%。所有提交给德尔菲回合的建议都获得了70%或更高的一致性,从而被接受。
导致儿童和青少年骨质疏松症的因素可能与遗传和生活方式有关。
患慢性病或长期接受损伤骨骼治疗的儿童,几个增加骨吸收和减少骨形成的因素共同导致骨脆性增加[100] [63]。因此,应在随访期间评估骨骼健康,采取适当的预防措施。
表2列出了一些导致继发性骨质疏松的疾病。

对于何时以及如何评估所有相关疾病的骨健康,没有通用共识。然而,有一些针对不同儿科疾病的临床指南(表3)。

DXA双能x线骨密度仪,BMD骨密度,GCs糖皮质激素,MTX甲氨蝶呤,FR危险因素
慢性病患者的BMD应根据每种疾病的现有指南进行监测。此外,必须特别关注患有慢性病并接受可能导致骨质疏松症的治疗的患者;例如,糖皮质激素(GCs)、化疗或抗癫痫药物。
影响儿童骨骼健康的因素有很多。其中许多都是可以改变的,至少在一定程度上是可以的(表4) [35]。

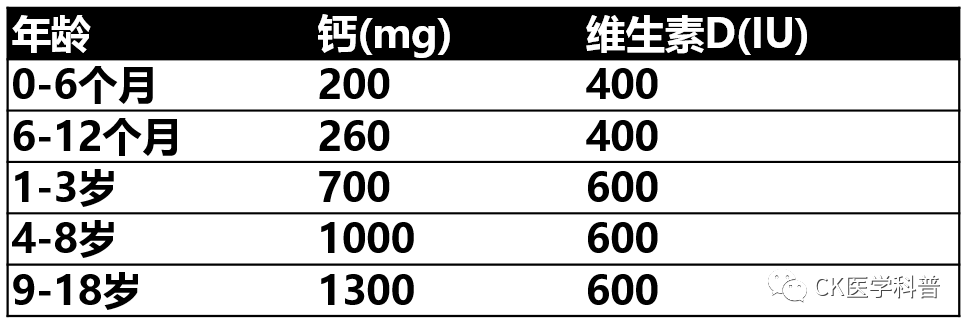
证据较高的对骨骼健康有积极作用的营养因子是钙、磷和维生素D [23]。表5列出了健康儿童的每日营养需求[103],尽管患慢性病或应用改变肠道吸收的药物治疗的儿童可能需要更高的钙和维生素D摄入量[23,35,49,104]。
对于获得最佳钙摄入量而言,富含钙的食物比补剂更可取,不仅因为它们具有更高的生物利用度[23]并且更容易消化,还因为它们的摄入避免了成人可能常见的继发性心血管效应[105],并且有利于从儿童时期就养成良好的营养习惯[23]。因此,不建议在没有骨质疏松或骨密度减低的情况下全身补钙[[106]。只应针对饮食中钙缺乏的患者[42]。
维生素D是钙吸收和利用的重要激素[103]。尽管一般来说,认为血清25-羟维生素D3≥50 nmol/L (20 ng/mL)正常。30-50 nmol/L (12-20ng/mL)为不足,<30nmol/L (12 ng/mL)为缺乏,关于维生素D的最佳水平仍存在一些争议[49]。
为了保持适当的水平,摄取富含维生素D的食物是重要的,同样重要的是,夏季几个月手、脸、手臂日晒6 ~ 8min之间(避开日间最热的时段),全年最冷的几个月日晒时间在30 min 。然而,不暴露于紫外线B对皮肤癌是安全的[49]。
患慢性病的儿童缺乏维生素D的风险增加。因此,建议监测这些患者的血清维生素D水平,尤其是在冬末[104]。
此外,许多其他营养物质在骨代谢中起着重要作用,如蛋白质、钾、镁、铜、铁、磷、锌和维生素A、C和K [23,104]。因此,建议包括水果和蔬菜的多样化饮食是重要的,以确保摄入足够的关键营养素,保持儿童和青少年良好的骨骼健康[23,35,104]。
此外,认为锻炼和有规律的体育活动是儿童期峰值骨量最大化的最有效策略[23,35,42,104]。高强度和低频率的运动——例如跳跃、跑步或阻力训练——有利于儿童骨密度的增加,就骨骼健康而言,比其他运动如游泳或骑自行车更适合[35,43,104]。然而,过强的体育活动会增加骨折风险[44]。
还有其他因素,如吸烟、咖啡因和饮酒,与骨密度降低和骨折风险增加有关[35,37,38,104]。这是儿童和青少年避免摄入它们的原因之一。
保持适当的营养状态也很重要,因为极瘦和肥胖都与骨密度减低和骨折风险增加有关[29,30,35]。
此外,对原发疾病的最佳控制是预防和治疗继发性骨质疏松症的最有效方法[23,35]。
实验室检查
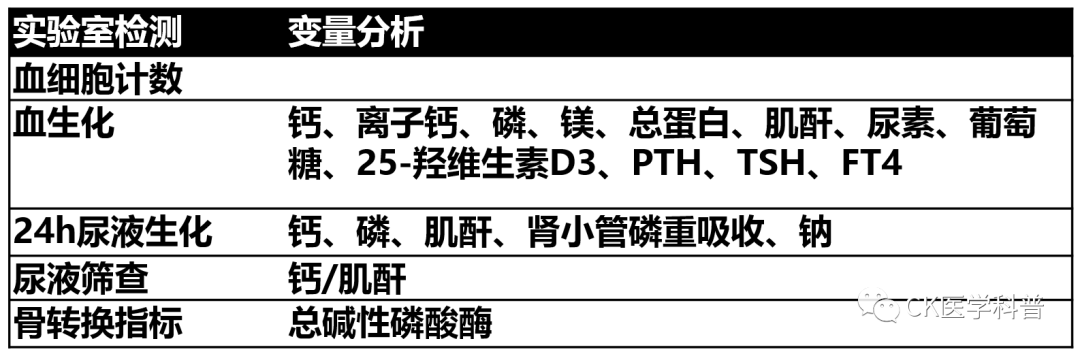
继发性骨质疏松症的诊断通常是在诊断出导致它的潜在疾病后进行的。然而,在某些情况下,它可能是潜在疾病的首发表现。尽管可以通过完整的病史回顾和体格检查来推断出鉴别诊断中包括的大多数疾病,但是一些疾病——如钙磷代谢变化、甲状腺功能减退或某些类型的白血病——可能是缺乏症状的,需要补充化验才能确诊[100]。因此,在评估疑似或确诊为继发性骨质疏松症的儿童时,建议采用表6所列的分析指标。关于表7所示指标,它们仅在临床怀疑的情况下才有理由(应用)。
钙/肌酐:单次尿,最好是早上第一次

应根据年龄、性别、生长速度、营养状况和青春期等因素来解释这些生化指标[52,59]。
骨转换标志物是在骨形成或吸收过程中释放到血液中的某些物质,反映了给定时间的骨代谢活动。虽然数量众多,但应分别用1型前胶原氨基末端前肽 ( P1NP ) 、Ⅰ型胶原羧基端肽 ( CTx )评估骨形成和吸收的参考指标[107,108]。这些可以在血和尿中检测到[109],对儿童来说,最好检测血标本[53,110,111]。已证实它们对成年人骨质疏松症的治疗有监测价值[112]。然而,在儿童,结果解释要复杂得多[54,110,113],尽管它们有助于抗重吸收治疗依从性的监测和有效性评估[100]。
影像学检查
儿童骨质疏松症的诊断主要根据存在脆性骨折。然而,建议采用双能x线吸收法(DXA)来确保对骨骼健康的完整评估[5]。
尽管有许多局限性[100],DXA是测定儿童骨骼健康的首选方法。DXA的首选骨骼部位是腰椎和不包括头部的全身,它们是儿童最精确和可重复的部位。此外,身高在第三百分位以下儿童的Z值应进行校正[5]。
其他用于评估儿科骨质量的技术有外周定量 CT和超声检查。然而,尽管在某些方面优于DXA,但对儿科人群的研究不足以推荐常规使用[100]。
此外,对于怀疑或确诊骨脆性增加的患者,应始终通过简单的全脊椎x线侧位片或DXA椎体骨折评估(如果可以的话)来评估通常为无症状的椎体骨折[39,114]。
钙和维生素D补充
在对健康儿童进行的研究中,没有显示补充钙和维生素D对骨密度有任何显著临床作用[106]。相比之下,一些研究报告称,对脑瘫等易于骨质疏松的慢性病患者有良好的效果。[8] 另一方面,没有副作用的报道[8,40] 。因此,虽然没有研究评估补钙对骨折发生率的影响,但对于骨密度减低或骨质疏松症的儿童和青少年,特别是那些饮食摄入量低的患者,可取的做法是补充钙剂。
同样,为了维持血浆25-羟维生素D3水平高于50 nmol/l (20 ng/dL),建议确保适当摄入维生素D3。
表6列出了健康儿童每日钙和维生素D的推荐摄入量[103]。对于患有可能干扰肠道吸收或改变钙代谢疾病的儿童来说,最佳摄入量仍不清楚 [41]。因此,起始剂量应根据这些建议补充,然后根据血浆25-羟维生素D3、全段甲状旁腺激素(iPTH)和尿钙水平进行调整,这些应每6-12个月监测一次。
双膦酸盐
BPs是焦磷酸盐的合成类似物,可抑制骨骼吸收。它们选择性浓集并增加高重塑率骨骼区域的骨密度[115]。它们是亲水性药物,肠吸收率低(< 1%)和分布容积高,通过尿液排出。因此,剂量应根据肾小球滤过率进行调整。此外,它们的特点是从骨组织中清除非常缓慢,并且治疗后在体内保留数年[115]。
关于这些药物中长期安全性的认识不断加深[100]。因此,一些作者建议只要符合骨质疏松标准就可应用,特别是那些长骨和椎体骨折的患者,以及那些自行恢复能力差的患者(青春期、风险因素持续存在等)[116]。
迄今为止,双膦酸盐仅被规定为二级防治措施。换句话说,一旦发生第一次骨折。它们的应用是为了防止出现新的脆性骨折。目前已知它们对骨密度有正性效应[9,84–87],并且关于它们的长期安全性的认识越来越多[100]。另一方面,如果在生长期结束时达到的峰值骨量不是最佳的,更有可能在生命晚期发生骨质疏松症[3]。基于上述数据,我们的工作组建议临床医生考虑对那些没有骨质疏松症,但青春期早期骨密度减低,Z值低且轨迹下降的患者进行BPs治疗。
在任何情况下,BPs治疗儿童骨质疏松症都是适应症外使用,因此在开处方时必须获得知情同意。
第二代和第三代BPs是儿童最常用的BPs。有些是静脉注射,有些是口服[100]。口服BPs广泛用于成年骨质疏松症,一些研究表明,它们增加成骨不全患者的骨密度,降低骨折风险。然而,与静脉注射BPs相比,它们对VF后重塑的诱导力不足[117],并禁用于有食管炎危险因素者;例如,胃食管反流或食管裂孔疝。小儿骨质疏松症首选静脉注射BPs,口服BPs仅用于因任何原因禁忌静脉内给药且无VF的轻度骨质疏松症患者或在治疗维持阶段[100]。
表8列出了儿科最常用BPs的剂量和给药间隔[100]。
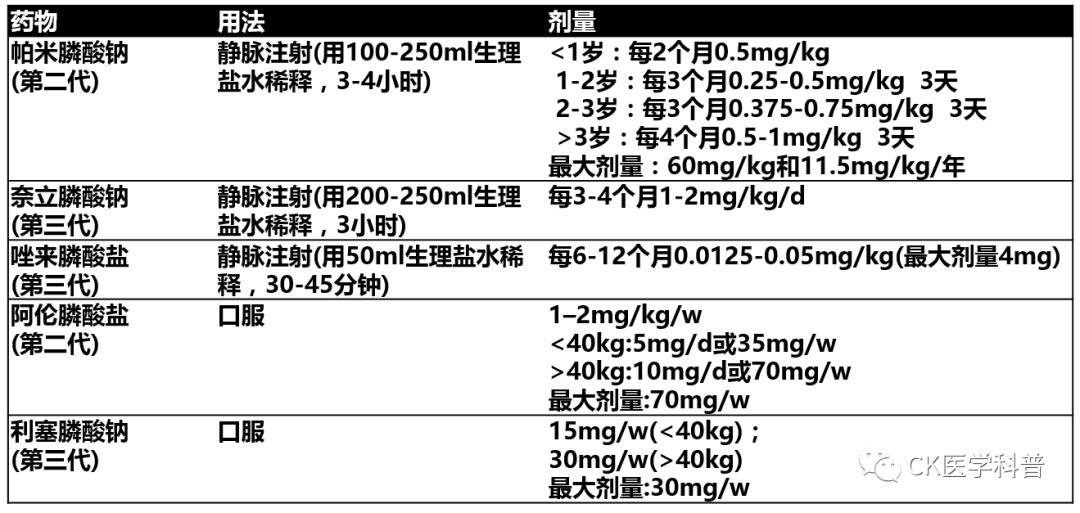
最佳治疗持续时间没有明确规定,目前基于专家建议[116]。我们建议对前一年没有出现骨折且Z值高于-2的患者停用BPs或逐渐减量。
对有骨质疏松风险因素的患者进行随访的目的是确定需要开始或继续有效治疗的患者。对于此类患者和已确诊为骨质疏松症的患者,只要持续存在风险因素,或者使用钙和/或维生素D3、BPs或其他骨质疏松症药物维持治疗,就应继续随访[49,51,74]。
应监测临床、放射和分析参数。评估脆性骨折和疼痛发作的次数很重要。就密度测定而言,Z值变化是相关的。DXA的最佳频率没有明确界定[74]。我们的建议是一年复查DXA,然后根据患者的发展轨迹,每1-2年检查一次,检查之间的最短间隔为6-12个月。
对VF进行放射学评估也很重要,因为它们通常无症状,甚至Z值高于-2的患者也会出现[23]。此外,它们的进展可导致治疗方法的改变[116]。虽然一些作者建议每年或每两年进行一次脊椎侧位x线检查,但没有研究明确界定VF的监测频率[23]。我们建议根据患者的风险因素对其频率进行个体化,最短6个月,最长2年。
此外,没有研究或指南界定评估磷钙代谢的最佳周期。我们的建议是每年进行一次分析测定。
对于补充钙和维生素D的患者,由于不清楚患慢性病的儿童和青少年的最佳摄入量[41],剂量应根据尿钙和25-羟维生素D3和血浆iPTH水平进行调整。监测这些指标的最佳频率尚不清楚[49],尽管一些作者主张每3-12个月进行一次测定[49,51]。我们的工作组建议,25-羟维生素D3的水平应每6-12个月测定一次,或改变剂量后3-6个月测定一次。此外,建议每年测定一次尿钙。如果出现尿钙增多或无法收集尿液,应行肾脏超声检查以排除肾钙质沉着。
对于接受BPs治疗的儿童,没有研究确定分析检查的最佳频率。我们小组建议对接受静脉注射BPs的患者在每次输注前进行监测,对口服BPs的患者每6个月进行监测。
皮质类固醇性骨质疏松症
GCs广泛用于多种儿科疾病,疗效确切。然而,它们有多种副作用,并与骨密度降低和脆性骨折有关[118]。
全身GCs治疗的患者在治疗的前3-6个月骨量减少更明显,主要是骨小梁。[118]。骨量丢失依赖于治疗剂量和持续时间[119,120]。虽然较低剂量比较高剂量的危害小,但似乎没有明确的安全剂量,因为据报道,2.5 mg/d和7.5 mg/d的泼尼松(或同等剂量)的骨折风险持续存在[118]。
因此,可取的做法是与其他有骨质疏松危险因素的患者一样,监测骨密度和VF的发生。本组患者DXA检查最佳时间尚不明确,我们建议在治疗的前6个月进行一次DXA检查,如果继续治疗,每9 ~ 12个月复查一次。
关于VF筛查,有研究报道第一年发病率约为10%,其中近50%无症状[70,71]。因此,建议在治疗初始用成像技术对这些患者进行评估,此后在维持GCs治疗的同时每年评估一次。
西班牙风湿病学会共识[121]认为,所有进行强的松高于5mg /d(或同等剂量)并持续3个月以上治疗的患者,必须尽早开始预防GIOP。预防措施包括处方尽可能低剂量的GCs来控制基础疾病,鼓励体育锻炼,避免有毒产品,如烟草和酒精,并确保均衡的饮食,摄入所需的钙和维生素D[121]。事实上,最近一项系统评价得出结论,作为预防GIOP的措施,所有应用GC的儿童应以健康儿童钙和维生素D推荐量为起始量给予补充,特别是当预期治疗持续3个月以上时[95]。此外,即使停止治疗,GCs对骨骼的影响仍在持续,我们小组建议在停止GCs治疗后的三个月内继续补充钙和维生素D。然而,尚无研究确定最佳补充期。尽管缺乏全面的数据,但该评价还建议将BPs用于预防目的[95]。我们自己的工作组只会在有脆性骨折时考虑全身使用BPs。然而,当发生GIOP时,其有效性得到证明;例如,当病理性骨折明显时[87,95,96]。
大多数研究表明,吸入GCs剂量低于相当于800mcg/d的布地奈德对骨折风险的影响最小,而较大剂量与BMD加速下降和较高的骨折风险相关。尽管有理由对这些患者进行非药物性预防[97,98,122],但不建议常规进行脊椎侧位x线或DXA检查,除非患者有其他风险因素[97–99]。此外,虽然一些小组建议给高危人群补充钙和维生素D,但给吸入GCs患者补充的作用尚未确定,[93]。
总之,我们在此提出了基于现有证据和专家临床经验的继发性儿童骨质疏松症的预防、诊断和治疗指南。我们相信它可以作为一个有用的工具,有助于这种病理临床实践的标准化。预防措施、早期诊断和适当的治疗方法对改善骨骼健康至关重要,不仅对儿童和青少年,而且对他们未来将成为的成人也是如此。
感谢西班牙小儿风湿病学会,Laboratorios Rubió和Alexion Pharma的赞助。
感谢InMusc医疗主任Dra.EstíbalizLoza协助进行文献回顾,确定了证据的推荐水平以及建立了Delphi调查。
RGZ协调了该项目,对儿童继发性骨质疏松症钙和维生素D的补充进行了文献综述,并根据证据提出了建议,是文稿的主要撰写者,阅读并批准了终稿。RBT对儿童继发性骨质疏松症双膦酸盐的应用进行了文献综述,并根据证据提出了建议,是文稿的主要撰写者,阅读并批准了终稿。BML对儿童继发性骨质疏松症筛查中的影像学检查进行了文献综述,根据证据提供了建议,阅读并批准了最终文稿。CMP对何时应怀疑儿童继发性骨质疏松症进行了文献综述,并根据证据提供了建议,阅读并批准了最终文稿。NPF对何时应怀疑儿童继发性骨质疏松症进行了文献综述,并根据证据提出了建议,阅读并批准了最终文稿。BSP对儿童糖皮质激素性骨质疏松症进行了文献综述,根据证据提供了建议,阅读并批准了最终文稿。MMSI对儿童继发性骨质疏松症筛查中的影像学检查进行了文献综述,根据证据提供了建议,阅读并批准了最终文稿。MIGF对儿童继发性骨质疏松症的随访进行了文献综述,根据证据提出了建议,阅读并批准了最终文稿。ARP对儿童继发性骨质疏松症筛查的实验室检查进行了文献综述,根据证据提供了建议,阅读并批准了最终文稿。PAR对儿童继发性骨质疏松症的预防进行了文献综述,并根据证据提出了建议,阅读并批准了最终文稿。JCNG进行了有关儿童继发性骨质疏松症中钙和维生素D补充的文献综述,根据证据提供了建议,阅读并批准了最终文稿。MLC进行了有关儿童继发性骨质疏松症预防的文献综述,根据证据提供了建议,阅读并批准了最终文稿。JGG对儿童继发性骨质疏松症筛查的实验室检查进行了文献综述,根据证据提供了建议,阅读并批准了最终文稿。
参考文献:
1. Peck WA etal.Consensus development conference: diagnosis, prophylaxis, and treatment ofosteoporosis. Am J Med. 1993;94(6):646-50.
2. Wade SW, Strader C,Fitzpatrick LA, Anthony MS, O’Malley CD. Estimating prevalence of osteoporosis:examples from industrialized countries. Arch Osteoporos. 2014;9:182.
3. Yeste D, CarrascosaA. Valoración e interpretación de la masa ósea en la infancia y laadolescencia. Pediatr Integr. 2015;XIX(6):436.e1–9.
4. Galindo Zavala R,Núñez Cuadros E, Díaz Cordovés-Rego G, Urda Cardona AL. Advances in thetreatment of secondary osteoporosis. An Pediatr. 2014; 81(6):399.e1–7.
5. Gordon CM, LeonardMB, Zemel BS. 2013 pediatric position development conference: executive summaryand reflections. J Clin Densitom. 2014;17(2): 219–24.
6. Baim S, Leonard MB,Bianchi ML, Hans DB, Kalkwarf HJ, Langman CB, et al. Official positions of theInternational Society for Clinical Densitometry and executive summary of the2007 ISCD pediatric position development conference. J Clin Densitom.2008;11(1):6–21.
7. Mir-Perelló C,Galindo Zavala R, González Fernández MI, Graña Gil J, Sevilla Pérez B,Magallares López B, et al. Prevention and early diagnosis of childhoodosteoporosis: are we doing the right thing? Rev Osteoporos y Metab Miner.2018;10(1):30–6.
8. Fehlings D, SwitzerL, Agarwal P, Wong C, Sochett E, Stevenson R, et al. Informing evidence-basedclinical practice guidelines for children with cerebral palsy at risk ofosteoporosis: a systematic review. Dev Med Child Neurol. 2012;54(2):106–16.
9. Dwan K, Phillipi CA,Steiner RD, Basel D. Bisphosphonate therapy for osteogenesis imperfecta.Cochrane Database Syst Rev. 2016 Oct 19;10: CD005088.
10. Bhardwaj A, SweKMM, Sinha NK, Osunkwo I. Treatment for osteoporosis in people withß-thalassaemia. In: Swe KMM, editor. Cochrane Database Sys Rev.2016;10(3):CD010429.
11. Birnkrant DJ,Bushby K, Bann CM, Alman BA, Apkon SD, Blackwell A, et al. Diagnosis andmanagement of Duchenne muscular dystrophy, part 2: respiratory, cardiac, bonehealth, and orthopaedic management. Lancet Neurol. 2018;17(4):347–61.
12. Cervera A, Cela E,González A, Berrueco R, Argiles B, Badell I, et al. Guía de práctica clínica dela talasemia mayor e intermedia en pediatría.1ST ed. CEGE; 2015.
13. Fong CY, MallickAA, Burren CP, Patel JS. Evaluation and management of bone health in childrenwith epilepsy on long-term antiepileptic drugs: United Kingdom survey ofpaediatric neurologists. Eur J Paediatr Neurol. 2011;15(5):417–23.
14. Hall CH, Hewitt G,Stevens SL. Assessment and management of bone health in adolescents withanorexia nervosa part one: assessment of bone health in adolescents. J PediatrAdolesc Gynecol. 2008;21(3):155–7.
15. Jefferson A,Leonard H, Siafarikas A, Woodhead H, Fyfe S, Ward LM, et al. Clinicalguidelines for Management of Bone Health in Rett syndrome based on expertconsensus and available evidence. PLoS One. 2016;11(2): e0146824.
16. Tangpricha V, KellyA, Stephenson A, Maguiness K, Enders J, Robinson KA, et al. An update on thescreening, diagnosis, management, and treatment of vitamin D deficiency inindividuals with cystic fibrosis: evidence-based recommendations from theCystic Fibrosis Foundation. J Clin Endocrinol Metab. 2012;97(4):1082–93.
17. Wasilewski-MaskerK, Kaste SC, Hudson MM, Esiashvili N, Mattano LA, Meacham LR. Bone mineraldensity deficits in survivors of childhood cancer: long-term follow-upguidelines and review of the literature. Pediatrics. 2008; 121(3):e705–13.
18. Zhang Y, MilojevicD. Protecting bone health in pediatric rheumatic diseases: pharmacologicalconsiderations. Paediatr Drugs. 2017;19(3): 193–211.
19. Shaw NJ. Managementof osteoporosis in children. Eur J Endocrinol. 2008; 159(Suppl):S33–9.
20. Cassidy JT, HillmanLS. Abnormalities in skeletal growth in children with juvenile rheumatoidarthritis. Rheum Dis Clin N Am. 1997;23(3):499–522.
21. Ma NS, Gordon CM.Pediatric osteoporosis: where are we now? J Pediatr. 2012;161(6):983–90.
22. Paganelli M,Albanese C, Borrelli O, Civitelli F, Canitano N, Viola F, et al. Inflammationis the main determinant of low bone mineral density in pediatric inflammatory boweldisease. Inflamm Bowel Dis. 2007;13(4): 416–23.
23. Ward LM, Konji VN,Ma J. The management of osteoporosis in children. Osteoporos Int.2016;27(7):2147–79.
24. Mandel K, AtkinsonS, Barr RD, Pencharz P. Skeletal morbidity in childhood acute lymphoblasticleukemia. J Clin Oncol. 2004;22(7):1215–21.
25. Cromer BA, BonnyAE, Stager M, Lazebnik R, Rome E, Ziegler J, et al. Bone mineral density inadolescent females using injectable or oral contraceptives: a 24-monthprospective study. Fertil Steril. 2008;90(6):2060–7.
26. Cibula D, SkrenkovaJ, Hill M, Stepan JJ. Low-dose estrogen combined oral contraceptives maynegatively influence physiological bone mineral density acquisition duringadolescence. Eur J Endocrinol. 2012;166(6):1003–11.
27. Lopez LM, Chen M,Mullins S, Curtis KM, Helmerhorst FM. Steroidal contraceptives and bonefractures in women: evidence from observational studies. Cochrane Database SystRev. 2012;15(8):CD009849.
28. Souverein PC, WebbDJ, Weil JG, Van Staa TP, Egberts ACG. Use of antiepileptic drugs and risk offractures: case-control study among patients with epilepsy. Neurology.2006;66(9):1318–24.
29. Soyka LA, Misra M,Frenchman A, Miller KK, Grinspoon S, Schoenfeld DA, et al. Abnormal bonemineral accrual in adolescent girls with anorexia nervosa. J Clin EndocrinolMetab. 2002;87(9):4177–85.
30. Turner JM, BulsaraMK, McDermott BM, Byrne GC, Prince RL, Forbes DA. Predictors of low bonedensity in young adolescent females with anorexia nervosa and other dietingdisorders. Int J Eat Disord. 2001;30(3):245–51.
31. Behringer M,Gruetzner S, McCourt M, Mester J. Effects of weight-bearing activities on bonemineral content and density in children and adolescents: a meta-analysis. JBone Miner Res. 2014;29(2):467–78.
32. Dong Y, Pollock N,Stallmann-Jorgensen IS, Gutin B, Lan L, Chen TC, et al. Low 25-hydroxyvitamin Dlevels in adolescents: race, season, adiposity, physical activity, and fitness.Pediatrics. 2010;125(6):1104–11.
33. Moro M, van derMeulen MC, Kiratli BJ, Marcus R, Bachrach LK, Carter DR. Body mass is theprimary determinant of midfemoral bone acquisition during adolescent growth.Bone. 1996;19(5):519–26.
34. Goulding A, GrantAM, Williams SM. Bone and body composition of children and adolescents withrepeated forearm fractures. J Bone Miner Res. 2005;20(12):2090–6.
35. Golden NH, AbramsSA. Optimizing bone health in children and adolescents. Pediatrics.2014;134(4):e1229–43.
36. Kalkwarf HJ, KhouryJC, Lanphear BP. Milk intake during childhood and adolescence, adult bonedensity, and osteoporotic fractures in US women. Am J Clin Nutr. 2003;77(1):257–65.
37. Watanabe R, InoueD. Smoking and bone. Clin Calcium. 2016;26(10):1445–50.
38. Maurel DB, BoisseauN, Benhamou CL, Jaffre C. Alcohol and bone: review of dose effects andmechanisms. Osteoporos Int. 2012;23(1):1–16.
39. Alqahtani FF,Offiah AC. Diagnosis of osteoporotic vertebral fractures in children. PediatrRadiol. 2019;49(3):283–96.
40. Huncharek M, MuscatJ, Kupelnick B. Impact of dairy products and dietary calcium on bone-mineralcontent in children: results of a meta-analysis. Bone. 2008;43(2):312–21.
41. Uziel Y, Zifman E,Hashkes PJ. Osteoporosis in children: pediatric and pediatric rheumatologyperspective: a review. Pediatr Rheumatol Online J. 2009;7:16.
42. Tan VPS, MacdonaldHM, Kim S, Nettlefold L, Gabel L, Ashe MC, et al. Influence of physicalactivity on bone strength in children and adolescents: a systematic review andnarrative synthesis. J Bone Miner Res. 2014;29(10): 2161–81.
43. Hind K, Burrows M.Weight-bearing exercise and bone mineral accrual in children and adolescents: areview of controlled trials. Bone. 2007;40(1):14–27.
44. Field AE, GordonCM, Pierce LM, Ramappa A, Kocher MS. Prospective study of physical activity andrisk of developing a stress fracture among preadolescent and adolescent girls.Arch Pediatr Adolesc Med. 2011; 165(8):723–8.
45. Tenforde AS,Fredericson M. Influence of sports participation on bone health in the youngathlete: a review of the literature. PM R. 2011;3(9):861–7.
46. Specker B, ThiexNW, Sudhagoni RG. Does exercise influence pediatric bone? A systematic review.Clin Orthop Relat Res. 2015;473(11):3658–72.
47. Dubnov-Raz G, AzarM, Reuveny R, Katz U, Weintraub M, Constantini NW. Changes in fitness areassociated with changes in body composition and bone health in children aftercancer. Acta Paediatr. 2015;104(10):1055–61.
48. Hough JP, Boyd RN,Keating JL. Systematic review of interventions for low bone mineral density inchildren with cerebral palsy. Pediatrics. 2010;125(3):e670–8.
49. Munns CF, Shaw N,Kiely M, Specker BL, Thacher TD, Ozono K, et al. Global consensusrecommendations on prevention and Management of Nutritional Rickets. Horm ResPaediatr. 2016;85(2):83–106.
50. Holmlund-Suila E,Koskivirta P, Metso T, Andersson S, Makitie O, Viljakainen HT. Vitamin Ddeficiency in children with a chronic illness-seasonal and agerelated variationsin serum 25-hydroxy vitamin D concentrations. PLoS One. 2013;8(4):e60856.
51. Misra M, Pacaud D,Petryk A, Collett-Solberg P, Kappy M. Drug, et al. vitamin D deficiency inchildren and its management: review of current knowledge and recommendations.Pediatrics. 2008;122(2):398–417.
52. Saraff V, Högler W.Endocrinology and adolescence: osteoporosis in children: diagnosis andmanagement. Eur J Endocrinol. 2015;173(6):R185–97.
53. Rauchenzauner M,Schmid A, Heinz-Erian P, Kapelari K, Falkensammer G, Griesmacher A, et al. Sex-and age-specific reference curves for serum markers of bone turnover in healthychildren from 2 months to 18 years. J Clin Endocrinol Metab. 2007;92(2):443–9.
54. Szulc P, Seeman E,Delmas PD. Biochemical measurements of bone turnover in children andadolescents. Osteoporos Int. 2000;11(4):281–94.
55. Yang L, Grey V.Pediatric reference intervals for bone markers. Clin Biochem. 2006;39(6):561–8.
56. Eapen E, Grey V,Don-Wauchope A, Atkinson SA. Bone health in childhood: usefulness ofbiochemical biomarkers. EJIFCC. 2008;19(2):123–36.
57. Jurimae J.Interpretation and application of bone turnover markers in children andadolescents. Curr Opin Pediatr. 2010;22(4):494–500.
58. Michalus I,Chlebna-Sokol D, Rusinska A, Jakubowska-Pietkiewicz E, Kulinska-Szukalska K.Evaluation of bone mineral density and bone metabolism in children withmultiple bone fractures. Ortop Traumatol Rehabil. 2008;10(6):602–12.
59. Warden SJ, Hill KM,Ferira AJ, Laing EM, Martin BR, Hausman DB, et al. Racial differences incortical bone and their relationship to biochemical variables in black andwhite children in the early stages of puberty. Osteoporos Int. 2013;24(6):1869–79.
60. Manjon Llorente G,Fernandez-Espuelas C, Gonzalez Lopez JM, Ruiz-Echarri MP, Baldellou VA. Normalvalues of bone turnover markers in childhood. An Pediatr (Barc). 2004;60(4):330–6.
61. Fischer D-C,Mischek A, Wolf S, Rahn A, Salweski B, Kundt G, et al. Paediatric referencevalues for the C-terminal fragment of fibroblast-growth factor-23, sclerostin,bone-specific alkaline phosphatase and isoform 5b of tartrateresistant acidphosphatase. Ann Clin Biochem. 2012;49:546–53.
62. Crabtree NJ, HoglerW, Cooper MS, Shaw NJ. Diagnostic evaluation of bone densitometric sizeadjustment techniques in children with and without low trauma fractures.Osteoporos Int. 2013;24(7):2015–24.
63. Clark EM, Ness AR,Bishop NJ, Tobias JH. Association between bone mass and fractures in children:a prospective cohort study. J Bone Miner Res. 2006;21(9):1489–95.
64. Schousboe JT,Shepherd JA, Bilezikian JP, Baim S. Executive summary of the 2013 InternationalSociety for Clinical Densitometry Position Development Conference on bonedensitometry. J Clin Densitom. 2013;16(4):455–66.
65. Adiotomre E,Summers L, Allison A, Walters SJ, Digby M, Broadley P, et al. Diagnosticaccuracy of DXA compared to conventional spine radiographs for the detection ofvertebral fractures in children. Eur Radiol. 2017;27(5):2188–99.
66. Binkovitz LA,Henwood MJ. Pediatric DXA: technique and interpretation. Pediatr Radiol.2007;37(1):21–31.
67. Leonard MB, FeldmanHI, Zemel BS, Berlin JA, Barden EM, Stallings VA. Evaluation of low densityspine software for the assessment of bone mineral density in children. J BoneMiner Res. 1998;13(11):1687–90.
68. Zemel BS, KalkwarfHJ, Gilsanz V, Lappe JM, Oberfield S, Shepherd JA, et al. Revised referencecurves for bone mineral content and areal bone mineral density according to ageand sex for black and non-black children: results of the bone mineral densityin childhood study. J Clin Endocrinol Metab. 2011;96(10):3160–9.
69. Zemel BS, LeonardMB, Kelly A, Lappe JM, Gilsanz V, Oberfield S, et al. Height adjustment inassessing dual energy x-ray absorptiometry measurements of bone mass anddensity in children. J Clin Endocrinol Metab. 2010;95(3):1265–73.
70. LeBlanc CMA, Ma J,Taljaard M, Roth J, Scuccimarri R, Miettunen P, et al. Incident vertebralfractures and risk factors in the first three years following glucocorticoidinitiation among pediatric patients with rheumatic disorders. J Bone Miner Res.2015;30(9):1667–75.
71. Phan V,Blydt-Hansen T, Feber J, Alos N, Arora S, Atkinson S, et al. Skeletal findingsin the first 12 months following initiation of glucocorticoid therapy for pediatricnephrotic syndrome. Osteoporos Int. 2014;25(2):627–37.
72. Makitie O, DoriaAS, Henriques F, Cole WG, Compeyrot S, Silverman E, et al. Radiographicvertebral morphology: a diagnostic tool in pediatric osteoporosis. J Pediatr.2005;146(3):395–401.
73. Mäyränpää MK,Helenius I, Valta H, Mäyränpää MI, Toiviainen-Salo S, Mäkitie O. Bonedensitometry in the diagnosis of vertebral fractures in children: accuracy ofvertebral fracture assessment. Bone. 2007;41(3):353–9.
74. Bianchi ML, LeonardMB, Bechtold S, Hogler W, Mughal MZ, Schonau E, et al. Bone health in childrenand adolescents with chronic diseases that may affect the skeleton: the 2013ISCD pediatric official positions. J Clin Densitom. 2014;17(2):281–94.
75. Shepherd JA, WangL, Fan B, Gilsanz V, Kalkwarf HJ, Lappe J, et al. Optimal monitoring timeinterval between DXA measures in children. J Bone Miner Res. 2011;26(11):2745–52.
76. Abrams SA. Buildingbones in babies: can and should we exceed the human milk-fed infant’s rate of bone calcium accretion? Nutr Rev. 2006; 64(11):487–94.
77. Oen K, Malleson PN,Cabral DA, Rosenberg AM, Petty RE, Cheang M. Disease course and outcome ofjuvenile rheumatoid arthritis in a multicenter cohort. J Rheumatol.2002;29(9):1989–99.
78. Lien G, Flato B,Haugen M, Vinje O, Sorskaar D, Dale K, et al. Frequency of osteopenia inadolescents with early-onset juvenile idiopathic arthritis: a long-term outcomestudy of one hundred five patients. Arthritis Rheum. 2003;48(8):2214–23.
79. Huber AM, GabouryI, Cabral DA, Lang B, Ni A, Stephure D, et al. Prevalent vertebral fracturesamong children initiating glucocorticoid therapy for the treatment of rheumaticdisorders. Arthritis Care Res (Hoboken). 2010;62(4): 516–26.
80. Winzenberg TM,Powell S, Shaw KA, Jones G. Vitamin D supplementation for improving bonemineral density in children. Cochrane Database Syst Rev. 2010;10:CD006944.
81. Winzenberg T,Powell S, Shaw KA, Jones G. Effects of vitamin D supplementation on bonedensity in healthy children: systematic review and meta-analysis. BMJ.2011;342:c7254.
82. Lovell DJ, Glass D,Ranz J, Kramer S, Huang B, Sierra RI, et al. A randomized controlled trial ofcalcium supplementation to increase bone mineral density in children withjuvenile rheumatoid arthritis. Arthritis Rheum. 2006; 54(7):2235–42.
83. Jekovec-Vrhovsek M,Kocijancic A, Prezelj J. Effect of vitamin D and calcium on bone mineraldensity in children with CP and epilepsy in full-time care. Dev Med ChildNeurol. 2000;42(6):403–5.
84. Kim MJ, Kim S-N,Lee I-S, Chung S, Lee J, Yang Y, et al. Effects of bisphosphonates to treatosteoporosis in children with cerebral palsy: a meta-analysis. J PediatrEndocrinol Metab. 2015;28(11–12):1343–50.
85. Ozel S, Switzer L,Macintosh A, Fehlings D. Informing evidence-based clinical practice guidelinesfor children with cerebral palsy at risk of osteoporosis: an update. Dev MedChild Neurol. 2016;58(9):918–23.
86. Bryan ML,Worthington MA, Parsons K. Treatment of osteoporosis/ osteopenia in pediatricleukemia and lymphoma. Ann Pharmacother. 2009; 43(4):714–20.
87. Ward L, Tricco AC,Phuong P, Cranney A, Barrowman N, Gaboury I, et al. Bisphosphonate therapy forchildren and adolescents with secondary osteoporosis. Cochrane Database SystRev. 2007;4:CD005324.
88. Thornton J,Ashcroft DM, Mughal MZ, Elliott RA, O’Neill TW, Symmons D. Systematic review of effectivenessof bisphosphonates in treatment of low bone mineral density and fragilityfractures in juvenile idiopathic arthritis. Arch Dis Child. 2006;91(9):753–61.
89. Ooi HL, Briody J,Biggin A, Cowell CT, Munns CF. Intravenous zoledronic acid given every 6 monthsin childhood osteoporosis. Horm Res Paediatr. 2013;80(3):179–84.
90. Simm PJ, JohannesenJ, Briody J, McQuade M, Hsu B, Bridge C, et al. Zoledronic acid improves bonemineral density, reduces bone turnover and improves skeletal architecture over2 years of treatment in children with secondary osteoporosis. Bone.2011;49(5):939–43.
91. Thornton J, AshcroftD, O’Neill T, Elliott R, Adams J, Roberts C, et al. A systematic review of theeffectiveness of strategies for reducing fracture risk in children withjuvenile idiopathic arthritis with additional data on longterm risk of fractureand cost of disease management. Health Technol Assess. 2008;12(3):iii – ix, xi – xiv, 1–208.
92. Bishop N, BraillonP, Burnham J, Cimaz R, Davies J, Fewtrell M, et al. Dualenergy X-rayaborptiometry assessment in children and adolescents with diseases that mayaffect the skeleton: the 2007 ISCD pediatric official positions. J ClinDensitom. 2008;11(1):29–42.
93. Hansen KE, KlekerB, Safdar N, Bartels CM. A systematic review and metaanalysis ofglucocorticoid-induced osteoporosis in children. Semin Arthritis Rheum.2014;44(1):47–54.
94. Bachrach LK, GordonCM. Bone densitometry in children and adolescents. Pediatrics.2016;138(4):e20162398.
95. Jayasena A,Atapattu N, Lekamwasam S. Treatment of glucocorticoidinduced low bone mineraldensity in children: a systematic review. Int J Rheum Dis. 2015;18(3):287–93.
96. Bell JM, ShieldsMD, Watters J, Hamilton A, Beringer T, Elliott M, et al. Interventions toprevent and treat corticosteroid-induced osteoporosis and prevent osteoporoticfractures in Duchenne muscular dystrophy. Cochrane Database Syst Rev.2017;1:CD010899.
97. Gregson RK, Rao R,Murrills AJ, Taylor PA, Warner JO. Effect of inhaled corticosteroids on bonemineral density in childhood asthma: comparison of fluticasone propionate withbeclomethasone dipropionate. Osteoporos Int. 1998;8(5):418–22.
98. Altintas DU,Karakoc GB, Can S, Yilmaz M, Kendirli SG. The effects of long term use ofinhaled corticosteroids on linear growth, adrenal function and bone mineraldensity in children. Allergol Immunopathol (Madr). 2005;33(4):204–9.
99. Buckley L, GuyattG, Fink HA, Cannon M, Grossman J, Hansen KE, et al. 2017 American College ofRheumatology Guideline for the prevention and treatment ofglucocorticoid-induced osteoporosis. Arthritis Rheumatol (Hoboken, NJ).2017;69(8):1521–37.
100. Marrani E, GianiT, Simonini G, Cimaz R. Pediatric osteoporosis: diagnosis and treatmentconsiderations. Drugs. 2017;77(6):679–95.
101. Sermet-Gaudelus I,Bianchi ML, Garabedian M, Aris RM, Morton A, Hardin DS, et al. European cysticfibrosis bone mineralisation guidelines. J Cyst Fibros. 2011;10(Suppl 2):S16–23.
102. Hollander MC, SageJM, Greenler AJ, Pendl J, Avcin T, Espada G, et al. International consensus forprovisions of quality-driven care in childhoodonset systemic lupuserythematosus. Arthritis Care Res (Hoboken). 2013; 65(9):1416–23.
103. Martinez Suarez V,Moreno Villares JM, Dalmau Serra J. Comité de Nutrición de la Sociedad Españolade Pediatría. Recommended intake of calcium and vitamin D: positioning of theNutrition Committee of the AEP. An Pediatr (Barc). 2012;77(1):57.e1–8.
104. Ebeling PR, Daly RM,Kerr DA, Kimlin MG. Building healthy bones throughout life: anevidence-informed strategy to prevent osteoporosis in Australia. Med J Aust.2013;199(S7):S1–S46.
105. Bolland MJ,Avenell A, Baron JA, Grey A, MacLennan GS, Gamble GD, et al. Effect of calciumsupplements on risk of myocardial infarction and cardiovascular events:meta-analysis. BMJ. 2010;341:c3691.
106. Winzenberg TM,Shaw K, Fryer J, Jones G. Calcium supplementation for improving bone mineraldensity in children. Cochrane Database Syst Rev. 2006;2:CD005119.
107. Vasikaran S,Eastell R, Bruyere O, Foldes AJ, Garnero P, Griesmacher A, et al. Markers ofbone turnover for the prediction of fracture risk and monitoring ofosteoporosis treatment: a need for international reference standards. OsteoporosInt. 2011;22(2):391–420.
108. Bauer D, Krege J,Lane N, Leary E, Libanati C, Miller P, et al. National Bone Health AllianceBone Turnover Marker Project: current practices and the need for USharmonization, standardization, and common reference ranges. Osteoporos Int.2012;23(10):2425–33.
109. Vasikaran SD,Chubb SA, Schneider HG. Towards optimising the provision of laboratory servicesfor bone turnover markers. Pathology. 2014;46(4):267–73.
110. Mora S, PrinsterC, Proverbio MC, Bellini A, de Poli SC, Weber G, et al. Urinary markers of boneturnover in healthy children and adolescents: agerelated changes and effect ofpuberty. Calcif Tissue Int. 1998;63(5):369–74.
111. Lambert HL,Eastell R, Karnik K, Russell JM, Barker ME. Calcium supplementation and bonemineral accretion in adolescent girls: an 18-mo randomized controlled trialwith 2-y follow-up. Am J Clin Nutr. 2008;87(2):455–62.
112. Glendenning P,Chubb SAP, Vasikaran S. Clinical utility of bone turnover markers in themanagement of common metabolic bone diseases in adults. Clin Chim Acta.2018;481:161–70.
113. Huang Y, Eapen E,Steele S, Grey V. Establishment of reference intervals for bone markers inchildren and adolescents. Clin Biochem. 2011; 44(10–11):771–8.
114. Di Iorgi N, MarucaK, Patti G, Mora S. Update on bone density measurements and theirinterpretation in children and adolescents. Best Pract Res Clin EndocrinolMetab. 2018;32(4):477–98.
115. Bachrach LK, WardLM. Clinical review 1: bisphosphonate use in childhood osteoporosis. J ClinEndocrinol Metab. 2009;94(2):400–9.
116. Simm PJ, Biggin A,Zacharin MR, Rodda CP, Tham E, Siafarikas A, et al. Consensus guidelines on theuse of bisphosphonate therapy in children and adolescents. J Paediatr ChildHealth. 2018;54(3):223–33.
117. Land C, Rauch F,Munns CF, Sahebjam S, Glorieux FH. Vertebral morphometry in children andadolescents with osteogenesis imperfecta: effect of intravenous pamidronatetreatment. Bone. 2006;39(4):901–6.
118. Van Staa TP,Leufkens HGM, Cooper C. The epidemiology of corticosteroidinduced osteoporosis:a meta-analysis. Osteoporos Int. 2002;13(10):777–87.
119. Reid IR, Heap SW.Determinants of vertebral mineral density in patients receiving long-termglucocorticoid therapy. Arch Intern Med. 1990;150(12): 2545–8.
120. Canalis E,Mazziotti G, Giustina A, Bilezikian JP. Glucocorticoid-induced osteoporosis:pathophysiology and therapy. Osteoporos Int. 2007;18(10): 1319–28.
121. Perez Edo L,Alonso Ruiz A, Roig Vilaseca D, Garcia Vadillo A, Guañabens Gay N, Peris P, etal. 2011 up-date of the consensus statement of the Spanish Society ofRheumatology on osteoporosis. Reumatol Clin. 2011;7(6):357–79.
122. Sharma PK,Malhotra S, Pandhi P, Kumar N. Effect of inhaled steroids on bone mineraldensity: a meta-analysis. J Clin Pharmacol. 2003;43(2):193–7.
Springer Nature remainsneutral with regard to jurisdictional claims in published maps andinstitutional affiliations.
内分泌代谢病疾病 @CK医学科普
内分泌代谢病知识架构 @CK医学科普
内分泌代谢病分级诊疗 @CK医学科普
CK注:本公众号为什么重视指南或共识的推广?
慢性疾病和常见病会有大量的临床研究证据,临床决策应尽量利用有价值、高强度的证据。一个好的指南或者共识,会按照一定的标准汇聚证据,会有多个该领域内的专家共同讨论,这样可以极大的避免个人经验中的偏见,得到相对客观的、更有利于患者的诊治方案。结合指南或共识的个人诊治经验可能更有效。
对于少见病和罕见病,共识的地位更加突出。这些疾病患者在诊治时会有自发的簇集效应,尤其在目前信息传递和搜索都非常便捷的情况下更是如此。具有特定罕见病诊治经验的专家并不多,需要大量搜索文献以指导诊治,因此罕见病相关共识对于临床可遇而不可求的某些场景更为弥足珍贵。
PS:想入专业群的内分泌专科医生可以加微信CKKK1977;仅限内分泌专科医生;加微信请标明身份:XX医院-科室-姓名-职称,否则拒绝加群,入群后也请将群内昵称改为:XX医院-科室-姓名。专业群仅限内分泌专科医生交流学习,暂不对其他科室人员或患者开放。
其实能忍受上面如此枯燥的专科内容并且看到这个“PS”的,基本只剩下内分泌的专科医生了 ,但是,如果你是非内分泌专科医生,竟然也对这些内容如此感兴趣以至于看到了这两段PS的内容,甚至还想加群,那就按照PS中的步骤来吧,欢迎你
,但是,如果你是非内分泌专科医生,竟然也对这些内容如此感兴趣以至于看到了这两段PS的内容,甚至还想加群,那就按照PS中的步骤来吧,欢迎你
