目录
一、血糖仪发展历程
1、全球糖尿病背景与诊断标准
2、血糖仪技术代际演进
第一代:水洗比色法(1979,拜耳)
第二代:擦血式(1983-1990)
第三代:免擦比色法(1987-1996)
第四代:电化学法(主流技术)
第五代:微创多部位采血(2001,TheraSense)
3、关键技术原理详解
4、未来趋势
二、无创血糖监测-背景
三、无创血糖监测-技术分类
四、无创血糖监测-技术分析
1、血液替代物法
(1)技术分类与生理学基础
(2)核心技术与产品分析
2.1 汗液监测技术
2.2 泪液监测技术
2.3 唾液监测技术
(3)已上市产品深度解析
(4)关键技术瓶颈
(5)未来突破方向
2、光谱法
(1)光谱法技术分类与原理
1.1 拉曼光谱法
1.2 近红外光谱法(NIR)
1.3 中红外与光学相干断层(OCT)
(2)代表产品与性能对比
(3)介电谱技术原理
(4)技术瓶颈与突破方向
(5)未来技术融合趋势
3、能量代谢守恒法
(1)技术原理:代谢热整合模型
(2)代表产品与技术对比
(3)误差根源与临床限制
(4)技术突破方向
(5)总结:代谢热法的价值与挑战
4、无创血糖监测系统举例
六、总结展望
1、全球糖尿病背景与诊断标准
-
流行病学数据(2015年):
-
全球患者:4.15亿 → 每11人中有1例
-
中国患者:2040年预计达1.51亿(IDF预测)
-
-
糖尿病本质:
-
慢性代谢疾病 → 胰岛功能减退+胰岛素抵抗
-
-
诊断金标准(WHO 2009):
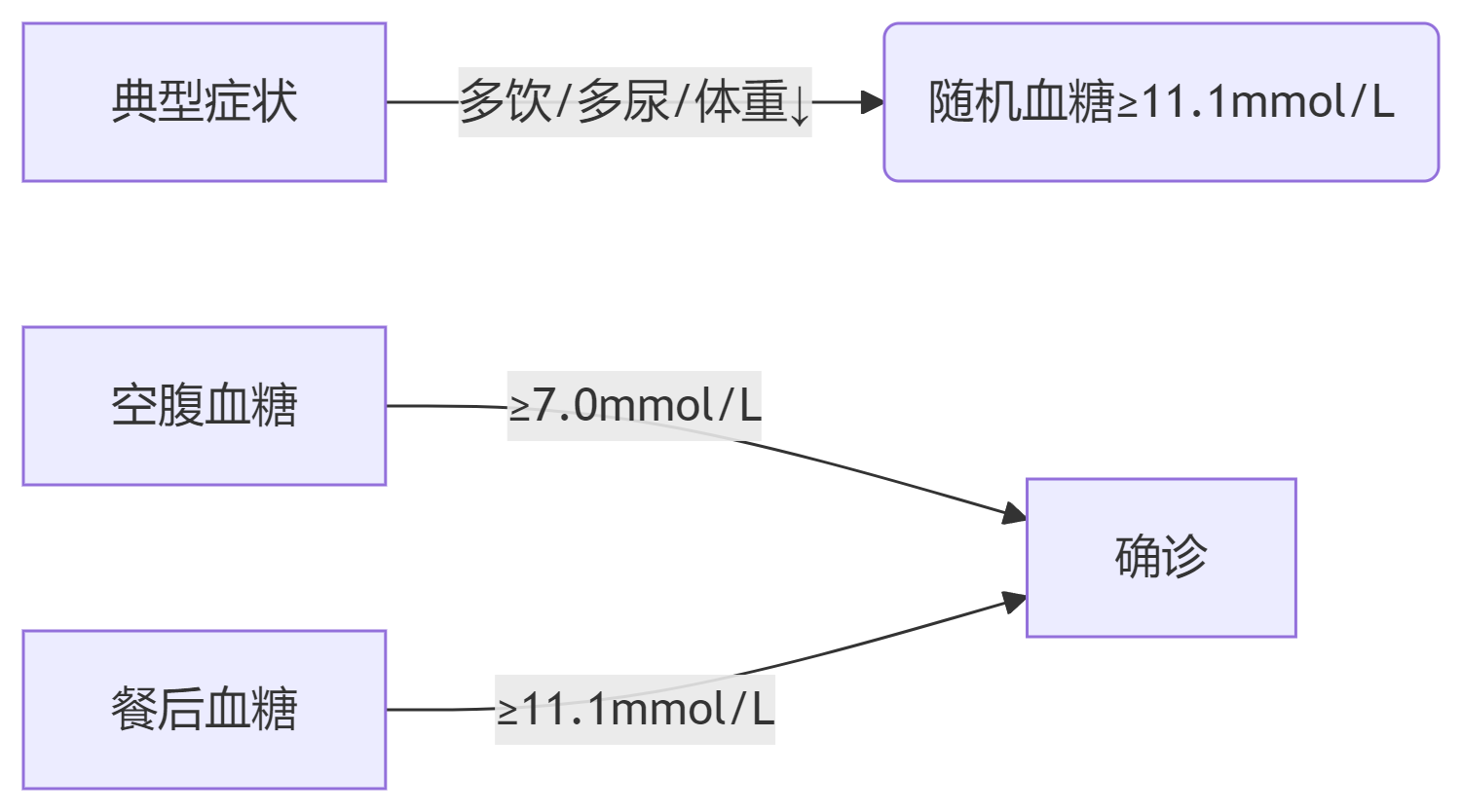
2、血糖仪技术代际演进
第一代:水洗比色法(1979,拜耳)
-
操作流程:
滴血→等待1分钟→冲洗血迹→比色卡对照 -
技术缺陷:
-
红细胞渗透干扰显色
-
改良版涂乙基纤维素仍存比色模糊(误差>15%)
-
第二代:擦血式(1983-1990)
第三代:免擦比色法(1987-1996)
-
技术升级:
试纸酶层固化 → 直接显色读数(无需擦拭红细胞) -
市场洗牌:
-
强生One Touch系列(1987)取代罗氏成美国霸主
-
罗氏反击:Accutrend Mini(1993)主打小型化
-
第四代:电化学法(主流技术)
-
核心创新:
三电极体系实现精准电流检测┌───────────────┐ │ 工作电极(WE) → 葡萄糖氧化反应 │ │ 参比电极(RE) → 电位基准锚定 │ │ 对电极(CE) → 闭合电流回路 │ └───────────────┘
-
优势:
-
体积缩小50% → 便携性↑
-
反应时间<5秒
-
误差率降至±5%
-
第五代:微创多部位采血(2001,TheraSense)
-
革命性突破:
-
库仑电量法:通过电解消耗电量反推血糖浓度
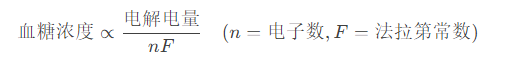
-
采血量0.3μL(传统1-3μL)
-
六部位采血:手指/手掌/四肢(FDA唯一认证)
-
-
“速加”技术:
Y型加样区 → 0.05秒快速虹吸收样
库仑电量法(第五代核心)
-
电解反应:

-
电量检测:
-
恒定电压下电解至电流归零
-
消耗电量
-
-
浓度计算:
(M:葡萄糖摩尔质量,V:血样体积)
误差控制:
-
电流效率100%:避免副反应干扰
-
温度补偿:酶活性受温度影响
-
无创技术:
-
光学传感器(红外/拉曼光谱)
-
组织液监测(微针透皮)
-
-
连续血糖监测(CGM):
-
雅培Freestyle Libre(14天实时监测)
-
-
AI融合:
-
血糖预测算法 + 胰岛素泵闭环控制
-
中国机遇:三诺生物等企业正突破电化学传感器芯片技术,抢占千亿级市场。
- 我国能够规律、规范地进行自我血糖监测的患者所占比例低,其中有 35.4%的患者从未进行自我血糖监测。
- 血糖采集过程中疼痛感带来的畏惧抵触心理。
- 实时监测患者的血糖浓度,能够让医生准确及时地了解患者的病情,从 而降低糖尿病患者其它并发症发生的几率。
- 可以降低医疗成本,良好经济效益。
- 避免因采血带来的环境污染,杜绝了传染病的发生,保持良好的医疗环境。
- 无创血糖已成为血糖检测领域一颗炙手可热的新星。
- 无创血糖的出现顺应了患者和医生的诉求。
- 血液替代物
- 光谱测量法
- 拉曼光谱法
- 光声光谱法
- 中红外光谱法
- 近红外光谱法
- 能量代谢守恒法
- 超声法、荧光法、电磁法、阻抗法 (电子皮肤)
(1)技术分类与生理学基础
浓度差异:体液葡萄糖浓度仅为血液的1/10~1/50,需超高灵敏度传感器
(2)核心技术与产品分析
2.1 汗液监测技术
-
原理:
葡萄糖经汗腺扩散至表皮 → 电化学/比色法检测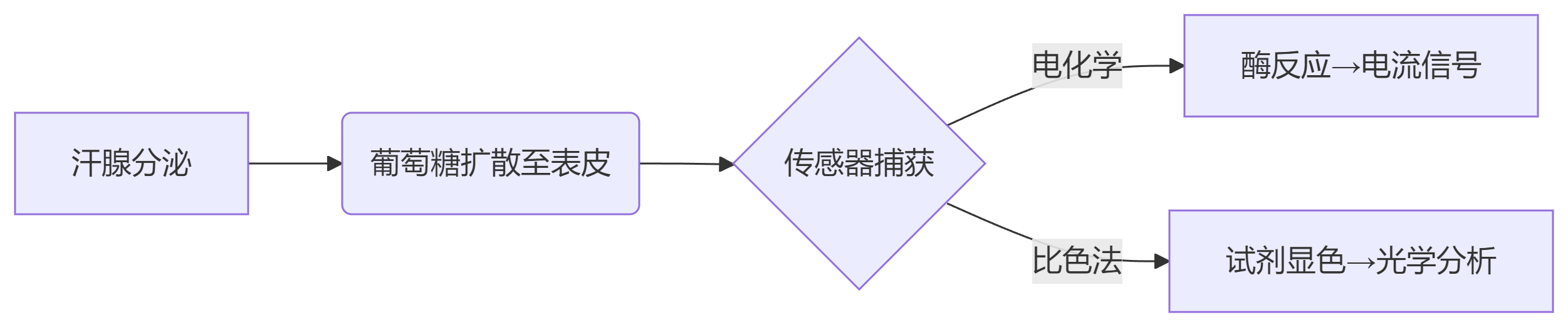
-
代表产品:
-
石墨烯电子纹身:柔性电极实时监测(加州大学圣地亚哥分校)
-
比色贴片:试剂遇汗变色 → 手机拍照分析(韩国KAIST)
-
-
瓶颈:
-
运动后乳酸干扰
-
汗液蒸发导致浓度失真
-
2.2 泪液监测技术
-
原理:
隐形眼镜集成三电极系统:组件 功能 工作电极(WE) 葡萄糖氧化酶催化产生H₂O₂ 对电极(CE) 闭合电路 参比电极(RE) 电位基准 微型天线 无线传输数据 -
代表产品:
谷歌智能隐形眼镜(已终止)-
突破:0.3mm微孔采泪 + 超薄电路
-
失败原因:
-
左右眼泪液浓度差异>15%
-
角膜刺激投诉率23%
-
-
2.3 唾液监测技术
-
原理:
口腔护具式传感器设计:┌──────────────┐ │ 生物酶层 → 葡萄糖→葡萄糖酸 │ │ 电子层 → 电流信号→蓝牙传输 │ └──────────────┘
-
产品原型:
-
日本东芝口护套:集成酶电极于磨牙区
-
美国PennState护齿:光学荧光法检测
-
-
干扰源:
-
食物残渣(尤其糖类)
-
口腔pH波动(咖啡/酒类影响)
-
(3)已上市产品深度解析
精度标准:FDA要求MARD(平均相对误差)<13.2% → 仅微针产品达标
(4)关键技术瓶颈
生理学限制
-
滞后效应:组织液葡萄糖滞后血液10-45分钟 → 延误低血糖干预
-
个体差异:
-
汗腺密度(200-600个/cm²)影响采样一致性
-
泪液分泌量(0.5-2.2μL/min)导致数据断层
-
工程挑战
(5)未来突破方向
-
多模态融合:
-
汗液+皮温+心率 → 机器学习补偿滞后(苹果手表专利)
-
-
纳米技术:
-
等离子体共振传感器:检测唾液葡萄糖灵敏度达0.1μM(MIT研发中)
-
-
闭环系统:

-
新型生物标志物:
-
丙酮呼气:糖尿病酮症早期预警
-
皮肤糖基化终产物(AGEs):荧光光谱无创检测
-
中国市场机遇:三诺生物布局汗液贴片,2025年目标MARD<10%
根据葡萄糖分子对光子的性质, 如旋光、反射、吸收和散射等, 这些方法可以通过改变光的偏振方向(a)、光路(b)、光强度(c) 和波长(d),利用偏振、红外吸收光谱、拉曼光谱等技术检测葡萄糖浓度。
(1)光谱法技术分类与原理
1.1 拉曼光谱法
1.2 近红外光谱法(NIR)
-
物理基础:
-
葡萄糖在950nm/1050nm/1550nm处有特征吸收
-
遵循朗伯-比尔定律:
(A:吸光度,ε:摩尔吸光系数,c:浓度,d:光程)
-
-
探测器类型:
类型 原理 优势 光电探测器 直接测量透射/反射光强 响应快(ms级) 热探测器 光热转换→热电堆输出电压 抗电磁干扰(图D)
1.3 中红外与光学相干断层(OCT)
-
中红外:检测C-O键伸缩振动(9.6μm) → 特异性高但穿透深度仅0.1mm
-
OCT技术(图b):
迈克尔逊干涉仪 → 通过散射光延时反演组织糖化程度
(2)代表产品与性能对比
*注:HG1-c的克拉克误差网格92%位于A/B区(临床可接受)*
(3)介电谱技术原理
-
物理基础:
血糖浓度↑ → 血液介电常数(ε')↓ + 电导率(σ)↑ -
频率响应特性:
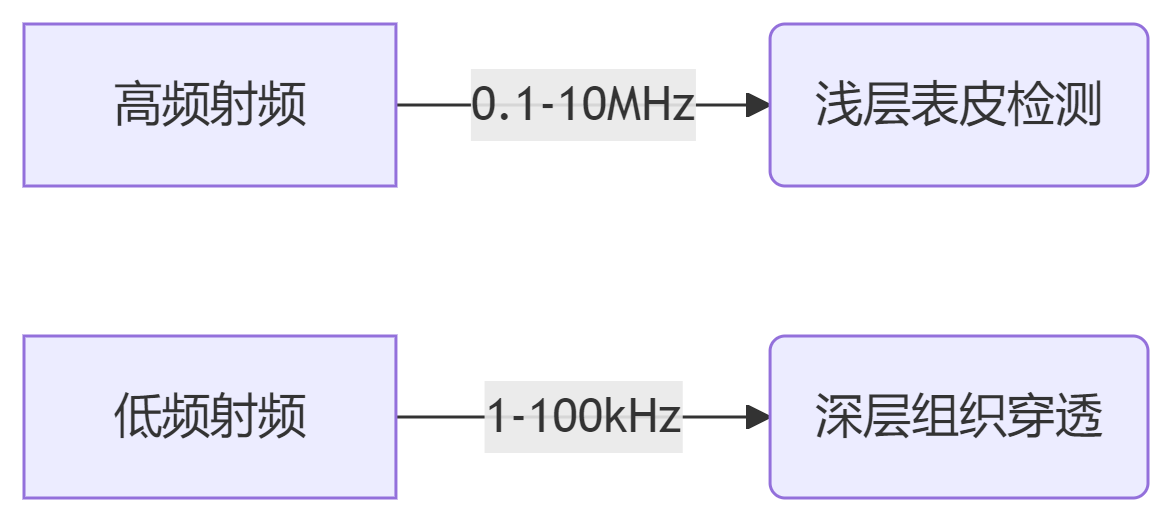
-
传感器设计(图示):
-
叉指电极阵列 → 测量复阻抗(Z = Z' + jZ'')
-
损耗角正切:tanδ = ε′/ε′′ ∝ 血糖浓度
-
(4)技术瓶颈与突破方向
光谱法共性难题
介电谱法特有挑战
-
温度敏感性:体温波动1℃ → 介电常数偏移2%
→ 解决方案:集成微型热敏电阻实时补偿 -
汗液电解质干扰:Na⁺/Cl⁻ 改变表皮电导率
→ 突破:多层电极隔离表皮信号(MIT专利)
(5)未来技术融合趋势
-
多模态传感器阵列:
┌─────────────┐ │ 拉曼光谱 → 分子指纹 │ │ 近红外 → 深层组织│ │ 介电谱 → 电特性 │ └─────────────┘
-
AI驱动校准:
-
CNN算法融合个人生理参数(BMI/皮厚/年龄)
-
动态减少校准频率(Dexcom G7降至每48小时1次)
-
-
柔性光电集成:
-
石墨烯透明电极 + 量子点激光器 → 可穿戴贴片
-
商业预测:2025年光谱法市场规模将达$24亿(复合增长率17.2%),但突破FDA精度门槛仍需解决滞后效应和运动伪影两大难题。
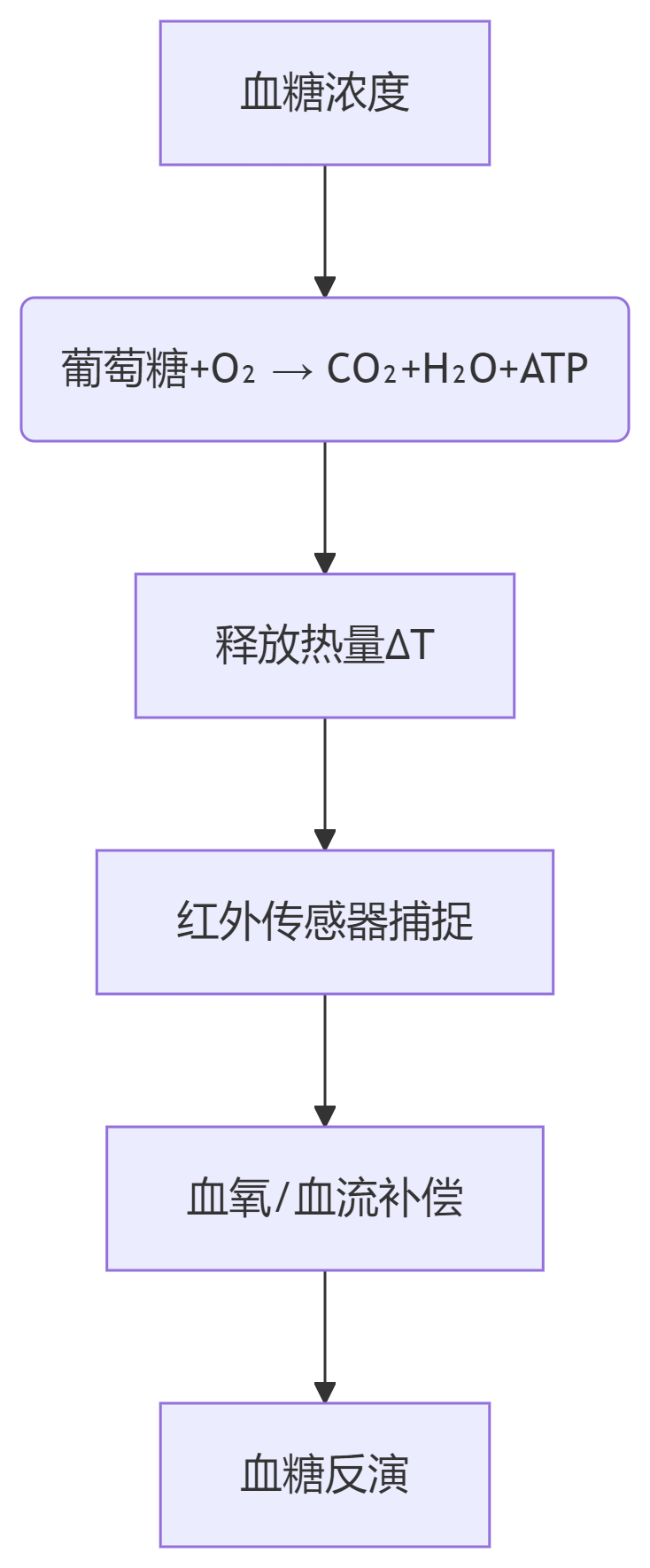
(1)技术原理:代谢热整合模型
核心公式:

-
生理学基础:
葡萄糖氧化产能 → 局部组织产热量 ↑ → 红外传感器检测
(2)代表产品与技术对比
超声+电导+热容
温度+红外+血氧+光学
GlucoTrack三模态原理:
-
超声模块:
-
血糖浓度↑ → 耳垂组织声速↑(+0.8m/s per 1mmol/L)
-
-
电导模块:
-
血糖↑ → 组织电导率↓(电解质稀释效应)
-
-
热容模块:
-
血糖↑ → 单位血流量产热量↑
-
(3)误差根源与临床限制
代谢热法的固有缺陷
GlucoTrack的临床验证问题
-
相关系数0.4:远低于FDA要求的0.9(Dexcom G6=0.92)
-
温度敏感性:
温度(℃) | MARD(%) ---------|--------- 25 | 38.2 27 | 25.0 29 | 26.1 31 | 41.5
(4)技术突破方向
传感器升级
-
解决方案:
-
微型化热电堆阵列(精度0.01℃) → 捕捉微区产热
-
多普勒血流雷达(60GHz) → 实时补偿血流量变化
-
-
进展:MIT研发皮下植入式微热电偶,动物实验MARD=12.3%
算法模型优化
-
机器学习补偿:
血糖=α⋅ΔT+β⋅血氧+γ⋅心率+δ⋅皮电+ϵ血糖=α⋅ΔT+β⋅血氧+γ⋅心率+δ⋅皮电+ϵ
-
输入参数扩展至12维生理信号
-
清华团队CNN模型将运动干扰误差降至18%
-
动态校准机制
-
双模式设计:

-
临界点:血糖变化率>2mmol/L/min时触发
-
(5)总结:代谢热法的价值与挑战
-
独特优势:
无需光学窗口 → 适用于黑色素皮肤人群(光谱法盲区) -
核心矛盾:
代谢信号弱(μW级) vs 环境干扰强(mW级) -
商业化前景:
短期难替代主流技术,但在居家筛查场景(如U糖未获认证版)存在下沉市场空间 -
终极目标:
与可穿戴设备(智能手表)融合 → 连续代谢当量监测
突破路径:高灵敏度热电材料(如Sb₂Te₃/Bi₂Te₃) + 联邦学习个人代谢模型,有望5年内将MARD压缩至15%以内。
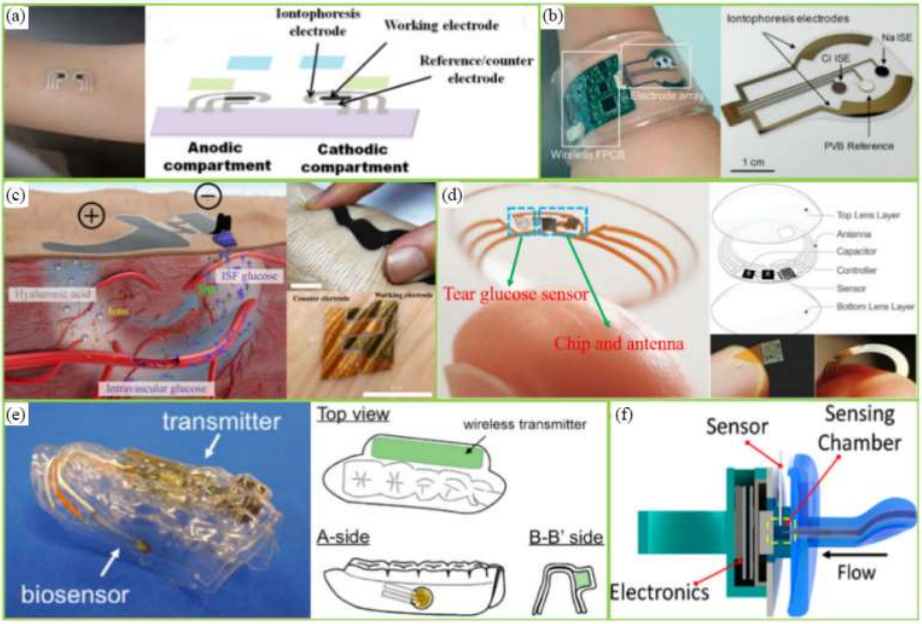
- (a)应用于手臂的纹身传感器;
- (b)可贴式汗液传感器;
- (c)ETCS示意图:包括透明质酸 (HA)渗透、葡萄糖回流和葡萄糖向外转运;
- (d)由谷歌和诺华共同设计的泪液葡萄糖传 感器;
- (e)护口器(唾液)生物传感器示意图;
- (f) 基于唾液的生物传感器结构
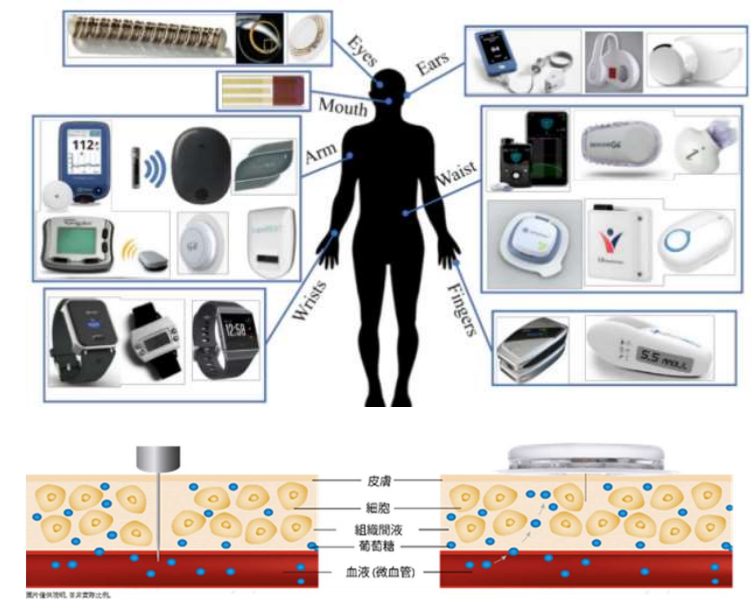
在过去的几十年里,已经推出了各种用于血糖监测的产品,包括可穿戴设备 和非侵入性检测设备。下图显示了市场上出现的各部位相关的监测产品(包括 停产产品)。
- 目前尚未出现精确度和及时性都满足标准的无创血糖产品
- 一方面是传感器的灵敏度、信噪比达不到要求,且信号易受其他因素干扰
- 另一方面,人体生理背景复杂多变,个体之间存在种种差异,测量部位的不同都会影响无创血糖的测量结果
- 基于这些局限,现有的产品大多只能作为血糖数值异常的预警设备
- 尽管无创血糖的前景诱人、市场广阔,但距离它真正可以造福于广大糖友的那一天,仍然有漫长的一段道路。
