医疗器械主要产品:
无源医疗器械:无电源能源供应的医疗器械,可通过人体或重力产生的能量发挥功能。
- I类,II类消费类:避孕,创口贴、伤口敷料;
- 手术工具:吻合器,缝补材料和黏合材料,手术刀等;
- 其他综合类:呼麻-口罩。过滤器,注输、透析,妇科、生殖、妊娠,康复器械;
- 体外诊断试剂:
- 口腔科器械、耗材;
- 眼科:角膜,人工晶体,眼内冲洗灌注液,手术用物质;
- 骨科:人工关节,脊柱修复,人工骨、骨水泥,创伤类骨钉骨板等连接固定器材;
- 其他植入物:心血管,神经内、外科,医美、整形、外科
医疗器械行业壁垒:
◆技术壁垒:多学科交叉整合、技术密集。技术平台和大规模临床数据积累需要时间
◆人才壁垒:研发、技术、临床使用、注册、质量、管理及营销等具有明显行业特色
◆渠道壁垒:医疗机构对安全性要求高,质量、价格、服务质量、品牌信任度至关重要
◆市场准入壁垒
·国家对医疗器械企业设立、产品注册、生产与销售有严格的要求和审查
·产品出口一般需要取得欧盟的CE认证或者美国FDA许可
国家药品监督管理局
- 1998年SDA
- 2000年版《条例》规定医疗器械由其管理,同年组建直属于国务院领导的SFDA
- 2008年3月改为卫生部管理
- 2013年,(国发(2013)14号),成立国家食品药品监督管理总局(FDA),为国务院直属机构
- 2018年并入新成立的国家市场监督管理总局(NMPA) ,卫检委同年一同监督
主要职责:贯彻实施国家医疗器械产业规划和政策,负责药品、化妆品、医疗器械的注册并实施监督管理。
相关内设机构:医疗器械注册管理局,医疗器械监管司
- 注册管理司机构设综合处、注册一处、注册二处、研究督察处等。
- 监管司机构设综合处、生产监管处、流通监管处、监测评价处等。
技术支撑部门与机构:医疗器械检测中心、技术审评中心、药品不良反应监测中心、标准管理中心等。
具体机构主要包括:
- 1、中国食品药品检定研究:暨国家药监局医疗器械标准管理中心,是囯家局直属事业单位,下设医疗器械标准研究所
- 2、医疗器械质量监督检验中心:安全有效性评价。注册检验、生物学评价检测。相关国家标准的技术审核、修订或起草
- 3、医疗器械技术审评中心:对医疗器械技术审评
- 4、国家药品监督管理局药品评价中心:也称国家药品不良反应监测中心,下设医疗器械监测与评价处负责医疗器械监管
- 5、医疗器械标准化技术委员:负责全国医疗器械标准化工作的技术指导和协调
美国医疗器械监管:最早立法管理医疗器械的国家
- 监管模式的科学性和系统性被大多数国家和地区认可
- 医疗器械管理和监督机构由商务部(DC)、FDA以及医疗卫生工业制造商协会(HIMA)共同承担,相互合作。根据1938年的《联邦食品、药品和化妆品法》FDA是监管的主要机构
- FDA中由器械和辐射健康中心(CDRH)及FDA监管事务办公室(ORA)负责医疗器械
- 1976年FDA颁布的《医疗器械修正案》捋医疗器械分为3类
- l类产品(占47%左右)实行一般管控
- ll类产品(占46%左右)实行特殊控制
- lll类产品(占7%左右)实行的是上市前许可(pre- market approva,PMA)
分类标准基于医疗器械的复杂性和风险特征,以lll类产品最复杂、风险最高
欧盟医疗器械监管:CE认证是欧盟的产品安全认证。外来医疗器械需满足的CE指令有:有缘植入性医疗器械指令、医疗器械指令、体外诊断器械指令。
CE认证要求
1、收集与认证产品有关的欧盟技术法规和欧盟(EN)标准,通过消化、吸收、纳入企业产品标准
2、按照产品标准生产,把上述技术法规和EN标准要求贯彻到产品的设计开发和生产制造的全过程
3、按照ISO9000+ISO13485标准建立和维护质量体系,并取得ISO9000+ISO13485认证
有如下几种类型的CE证书:
(1) Declaration of conformity/ Declaration of compliance《符合性声明书》,是自我声明书
(2) Certificate of compliance/ Certificate of compliance《符合性证书》,为第三方机构或测试认证机构)颁发的符合性声明,同时,企业也要签署《符合性声明书》
(3) EC Attestation of conformity《欧盟标准符合性证明书》,可用作清关,为一次性证书
日本医疗器械监管
归口管理
通产省、厚生省、医疗器械工业协会。厚生省全权负责医疗器械的监督管理,厚生省药物局根据《药事法》进行具体的行政管理。
行业分类:制造业、贩卖业、制造贩卖业
产品分类
- l类:一般器械,须获得地方政府的入市销售许可,不需要厚生省批准或对入市的管理规定。
- ll类:控制类器械,须由第三方认证。
- lll和lV类:严格控制类器械,受严格管理,须获得厚生省入市销售许可
行业许可:制造业生产许可、贩卖业许可、制造贩卖业许可、修理业许可
产品管理:承认审查制度,根据产品的危险等级,分别采取产品申报登记、产品第三方认证、厚生劳动大臣审查承认等不同管理等级
过程管理:按不同等级体现在QMS、GDP、GVP、广告规定方面,非常注重临床研究规范和不良事件报告体系建设。
生产企业按照《医疗器械生产质量管理体系》建立健全质量管理体系,规定了如下内容:
- 机构与人员:组织机构图明确各部门的职责和权限,明确质量管理职能
- 厂房与设施:合理设计、布局和使用保证符合生产要求
- 设备:生产设备、工艺装备等确保有效运行。检验仪器、设备和计量器具满足使用要求
- 文件管理:建立健全包括质量方针和质量目标、质检和记录以及法规要求的其他文件
- 设计开发:建立控制程序并形成文件对设计和开发过程实施策划和控制
- 采购:建立控制程序,确保采购物品符合规定要求及法律法规规定和囯家强制性标准
- 生产管理:保证产品符合强制性标准和经注册或者备案的产品技术要求。编制工艺规程、SOP等,根据生产工艺特点对环境进行监测,并保存记录
- 质量控制:建立质量控制程序,规定产品检验部门、人员、操作等要求,并规定检验仪器和设备的使用、校准等要求,以及产品放行的程序
- 销售和售后服务:建立销售记录并可追溯。顾客反馈处理程序及信息有跟踪分析
- 不合格品控制:建立不合格品控制程序,规定控制的部门和人员的职责与权限,对不合格品标识、记录、隔离、评审并采取相应的处置措施
- 不良事件监测、分析和改进:指定相关部门负责接收、调查、评价和处理顾客投诉,并保持相关记录。建立不良事件监测制度,开展监测和再评价工作,并保持相关记录
2019年全球医疗器械市场规模4500亿美元,五年年均增长率超5%,
全球医疗器械行业主要分布
- 以欧美发达国家为中心的、以高科技为主的新型医疗器械产业链,产品包括医用介入治疗器械、身体检测与扫描仪器等,国外大型企业垄断了全球绝大多数市场;
- 劳动密集且技术含量不高的传统型医疗器械,逐渐从欧美发达国家向劳动力成本比较低的发展中国家转移,如一次性注射器等,亚洲的典型承接国有中国和印度。
各地区发展特点:
◆美国是最大市场和制造国,占全球医疗器械市场40%。拥有强大研发实力,技术水平世界领先。
◆欧渊是全球第二大市场和制造地区,占全球医疗器械市场30%。德、法、英是欧洲医疗器械的主要制造国。法国也是欧洲主要医疗器械出口国
◆中国已成为全球医疗器械重要生产基地,占全球医疗器械市场14%市场份额,在多种中低端医疗器械产品领域,产量居世界第一。
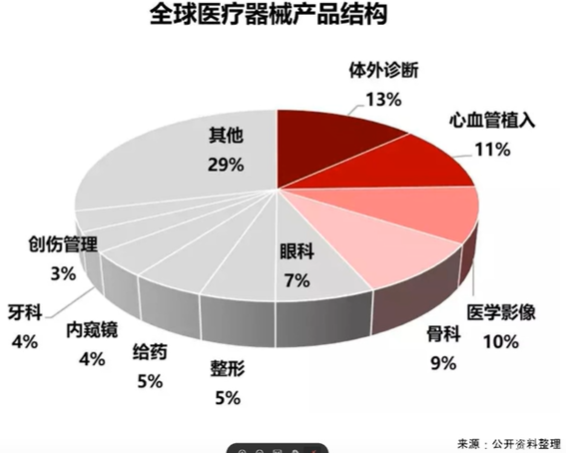
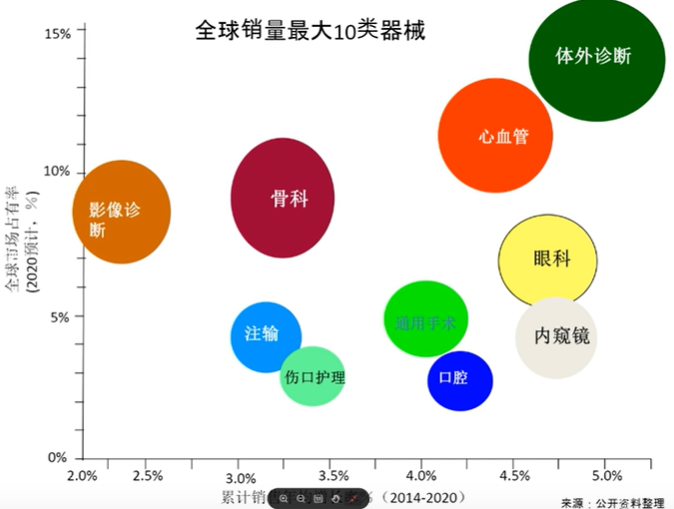
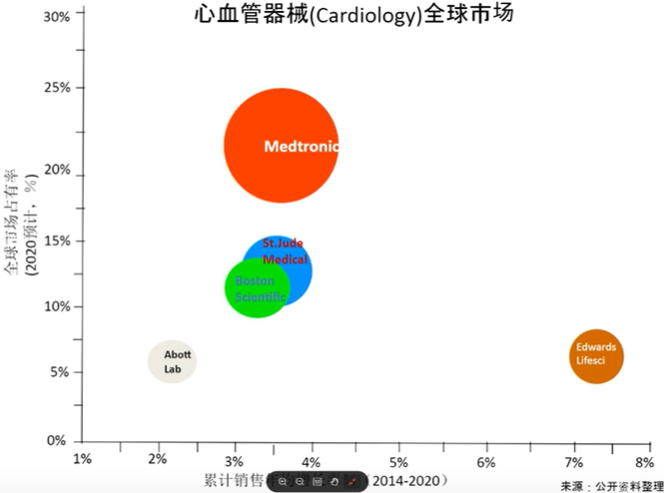
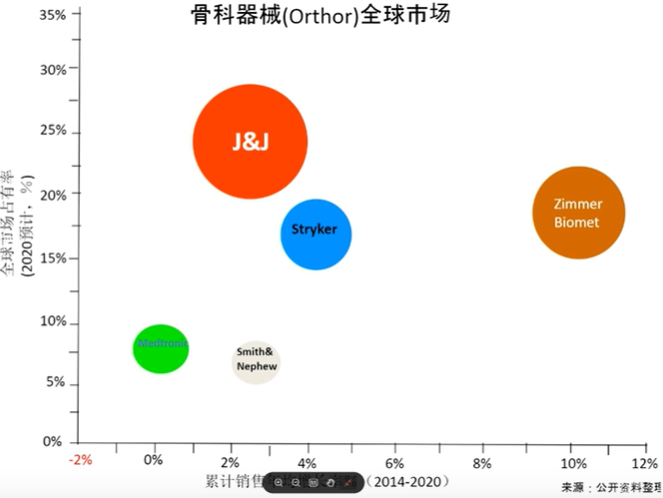
全球医疗器械技术热点:
- 影像诊断( Diagnostic Imaging)
- 远程医疗( Telemedicine)
- 分子诊断( Molecular Diagnostics)
- 助行器械( Mobility Aids)
- 微创手术 (Minimally Invasive Surgery)
- 微流体与微机电系统( Micro- Fluidics and mems)
- 无创监护( Non-Invasive Monitoring)
- 生物材料(Bio- Materials)
- 生物植入技术( Bio-Implants)
- 药物输送(Drug Delivery)
近几年火爆的医疗机器人、可穿戴医疗器械等一般包含以上多项核心技术。
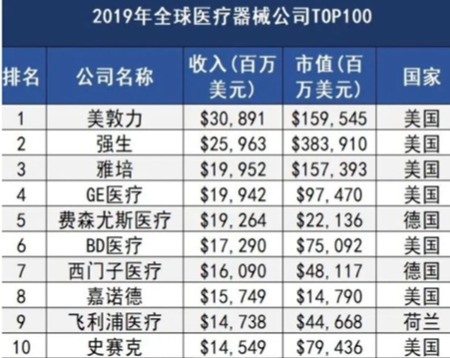
全球十大医疗器械企业:第三方QMED发布的《2019年医疗器械企业百强榜单》
并购:总体规模495亿美元,史塞克和波士顿科学活跃度超过美敦力。
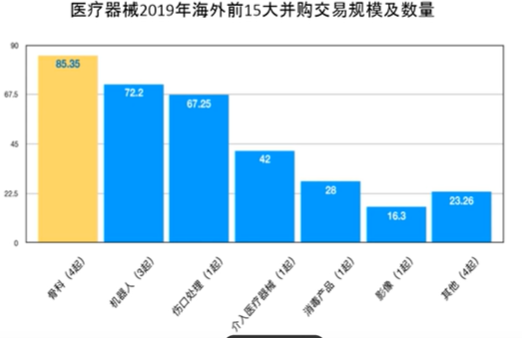

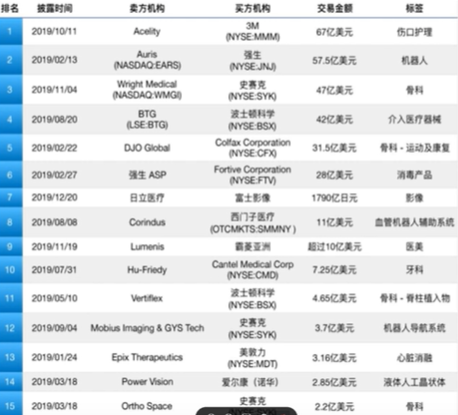
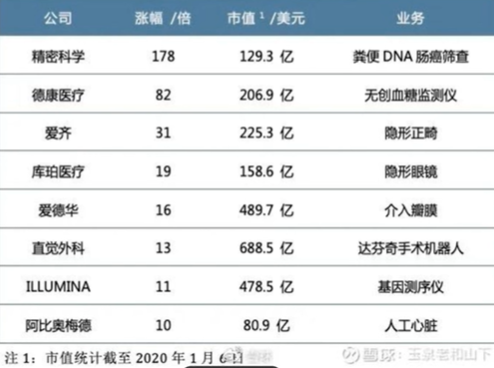
海外前15大并购,来源浩悦资本 美股过去十年诞生14支10被医药股,8支为医疗器械。
美国医疗器械市场:40%,慢性病和老年人口为主要市场驱动力,美敦力,强生,雅培占全球1/5市场份额。罗氏、雅培、丹纳赫、西门子医疗,IVD行业四大巨头占据全球近一半份额。根据OEC统计,出口220亿美元国家依次为荷兰、中国、德国、日本,进口150亿美元国家依次为德国、墨西哥、日本、中国。
来自中国的医疗器械进口额保持良好增长势头,10%+。
欧盟医疗器械市场:第二大,市场三成,德法英意瑞占欧洲市场3/4。准入门槛CE同FDA的510(K)条例市场准入速度比美国快些。质量保证体系执行更为严格的EN46001(见MDD附录)。
进入欧盟市场的方式:
◆获得著名医院的信任
首先攻下欧洲著名医院,赢得大医院的医生信任,欧洲中小医院才会逐步信任并采购你的产品
◆找可靠的总代理商
无法与西门子、罗氏等大公司竞争时,只能依赖当地可靠的总代理商,他们与当地医院的采购负责人有深厚的合作基础。
◆高值产品先做临床试验
高值产品最好先在主要国家如德、法、英、意和瑞士等发达国家开展临床试验,欧洲医生普遍认为欧洲的医疗水平是全球最高的,大多不很相信外国医院,尤其是中国、印度和巴西等发展中国家医院的临床试验结果。
◆小产品找分销商
低值耗材值类或手术台、轮椅等技术含量不高的产品,可直接交欧洲分销商销售,双方共赢。
日本医疗器械市场 机械、光学、电子和材料工业强国,医疗器械工业门类全,生产大部分品类,共15大类。
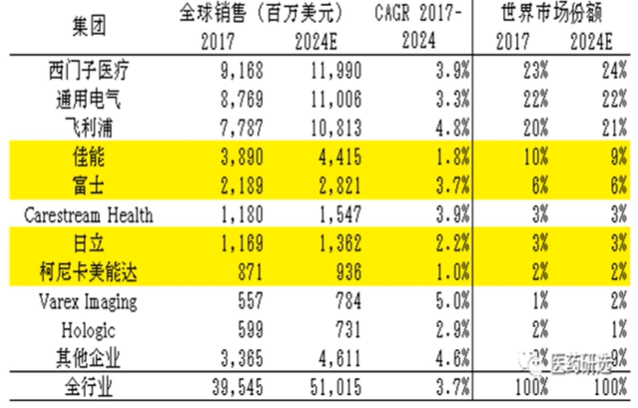
我国医疗器械市场
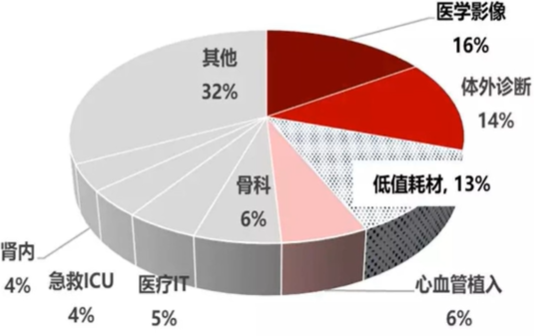
械药比:全球平均1:1.4,发达国家1:1,我国1:4
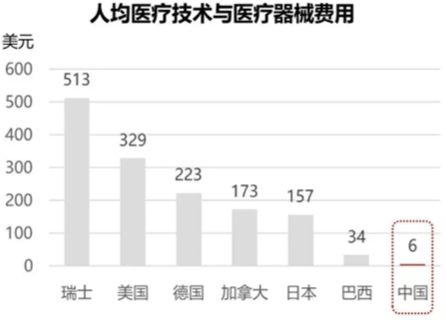
医疗器械国内发展:
- 企业多、规模小
目前生产企业18000家
规模小、产业集中度低、生产技术水平偏低
研发投入不足
国际竞争力不足
- 研发能力不足,高端靠进口,低端竞争恶性
创新转化率不高:新产品销售收入年均增长32%,但低于新产品开发经费36%的平均增速
高端器械还是依赖进口: PET. MRI,CTB超,人工关节等
大型设备毎年市场规模近两百亿元,大部分进口
- 中、低端产品关键霁部件仍依赖进口。
刚需行业、市场潜力大
大健康产业的重要细分行业
政策支持国产设备,去年贸易战、今年疫情更显国产设备的价格优势是主要的市场增长点
跨行业、高科技、资金密集型
2019年医疗器械相关政策:
- 医疗器械实名制,医用耗材统一编码;
- 带量采购:推行的4+7带量采购和扩围,推动3+5带量采购;
- DRG(Diagnosis Related Groups,按疾病诊断相关分组):医保不再纵容大处方,取消耗材加成,耗材、检验检查由收入来源变成成本
- 平台型企业:有完整解决方案,通过成本费用平摊、产品多元化、规模效应、总收入体量大更具优势
- 创新型企业:加快国产替代,具备核心技术和产品实力的公司可以大幅提升市占率
- 头部企业:在“通缩”控费背景下,品种单一的中小企业风险更高,企业经并购退出接受度迅速提升,市场环境有利干有资金的头部企业通过并购拓展产品布局和市场
带量采购、DRG有利于:
医疗器械注册人制:MAH制度利好医疗器械CDMO/CMO
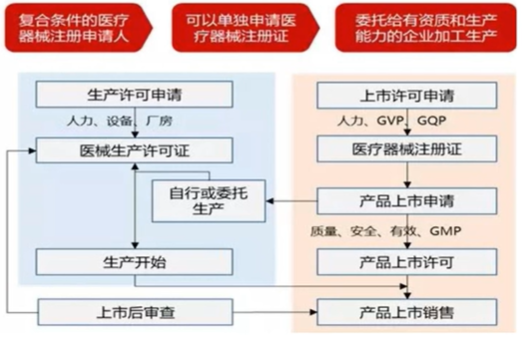
创新医疗器械特别审批程序相比于普通三类缩短83天,
中国近年医疗器械创新关键词:
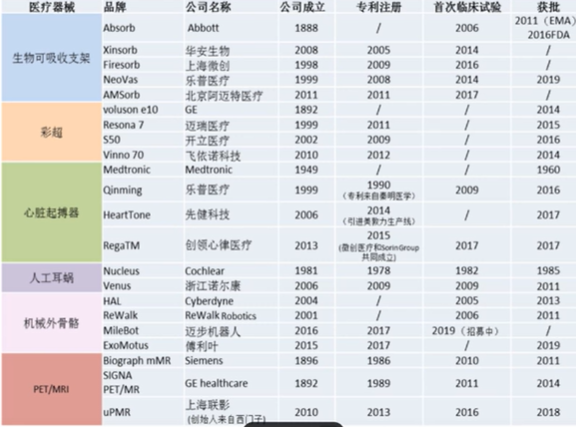
中国医疗器械未来十年
一、进口替代:
◆产业结构升级
结构性差距
生产企业90%以上为中小型企业
◆械药比、上市公司比例失衡
◆招标控费促进口替代
二、配套机制
◆政策:密集出台和落实,良好的法规环境
◆人才:国內院校生物工程学系崛起,海外人才的回归、引进
◆资本市场:科创板的推出,并购活动兴起
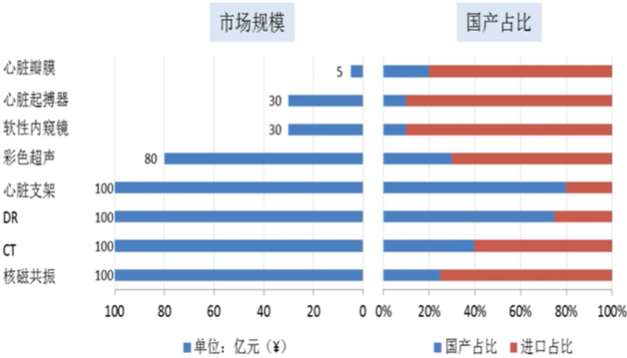
国产心血管支架4年完成进口替代。2004年前,国内冠脉支架市场,强生、美敦力、波士顿科学等多家跨国巨头占市场份额95%以上。
- 2004-2005年微创医疗、乐普医疗先后上市国产药物洗脱冠脉支架;
- 2006-2008年国产支架市场占有率分别由59%增长至70%;
- 2017年,国产品牌乐普、微创和吉威分别占据心脏支架市场24%、23%和20%的份额,共计占有67%的市场份额巳经占据2/3的市场份额。

进口替换机会:
血液净化耗材:外资70%,我国透析市场非常巨大;
神经外科耗材:除人工硬脑(脊)膜市场完成替代外其他细分为外资主导;
伤口管理耗材:敷料、缝针、缝线等,不可吸收材料市场为外产把持如强盛的进口缝线、巴德的疝补片、美敦力的止血夹等,
人工关节
ECMO( Extracorporeal Membrane Oxygenation)全称“体外膜肺氧合”,音译“叶克膜”,俗称“人工肺”,对重症心肺功能衰竭患者提供持续的体外呼吸与循环,以维持患者生命,号称救治新冠肺炎重症病人的”终极救命神器”。目前全球只有几家企业能够生产,我国目前还没国产。
结构包括血管内插管、连接管、动力泵(人工心脏)、氧合器(人工肺)、供氧管、监测系统等,最核心的部分是膜肺和血泵,分别起人工肺和人工心脏作用,对重症心肺功能衰竭患者进行长时间心肺支持。
近日,在广东省医疗器械质量监督检验所召开国家局体外循环器械重点验室专题工作会议,研究开展ECMo标准和技术研究,为企业ECMo研发提供技术支持,推进ECMo国产化进程,填补产品国内空白。
我国中小医疗器械企业现状:
- 现有生产企业1.8万家,85%为中小型,年销售额不到3000万元
- 年均增长率20%,中低端医疗器械增长率30%
- 80%的CT、超声波仪器、磁共振设备、心电图机、中高档监视仪、高档生理记录仪等被GE医疗、飞利浦、东芝、西门子、奥林巴斯、史赛克等跨国公司垄断
- 国内企业产品主要集中在按摩器具、血压仪等低附加值品类
- 一方面要抵御国外公司和国内大企业的挤压,另一方面还要应对医改带来的政策变化
- 生存第一、短期现金流为王
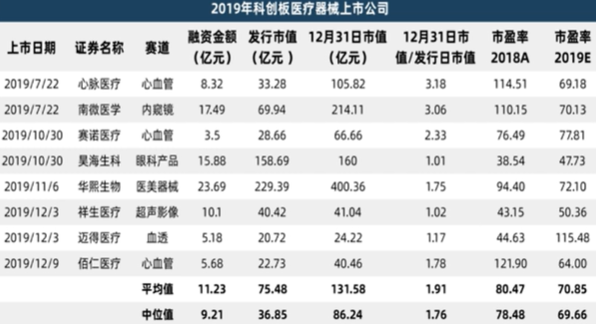
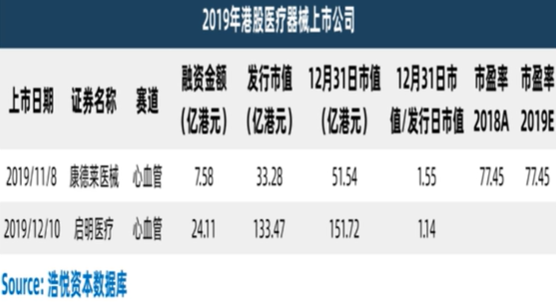
2019年有8家医疗器械公司在科创板上市,覆盖心血管、医学影像、内窥镜等多个赛道 2019年有2家医疗器械公司在港股上市,均在心血管领域。
参考来源:【医疗器械】第一集:医疗器械那些事儿_哔哩哔哩 (゜-゜)つロ 干杯~-bilibili 干货满满滴
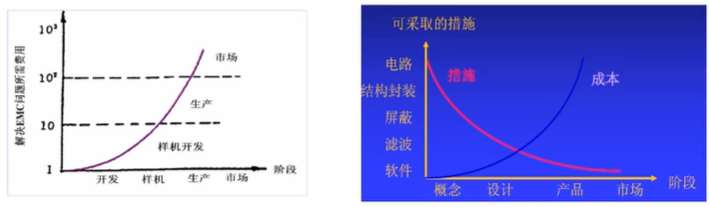
医疗器械EMC相关政策 食药监办械[2012]151号
2014年1月1日,首次申报注册的III类医用电气设备在注册申报时提交EMC检测报告;
2015年1月1日,首次申报注册的I类、II类医用电气设备在注册申报时提交EMC检测报告。
在重新注册时再提交符合电磁兼容标准要求的相应检测报告。
EMC常见问题:送检环节屡次EMC不合格,监督抽验不合格被罚款公示影响招投标,研发前期配件选购有问题导致的EMC不合格。
提高EMC自检能力:
人-接受相关EMC培训,分析资料[标准法规、测试数据、研发资料等];物-检测设备替代法或非标法
eg:可用于辐射和传导发射的自检搭配,频谱仪+电流钳或频谱仪+近场探头[d电场探头,磁场探头]

医疗器械法律法规
口罩:普通,防护Respirator,医用
N95口罩常规时期如何在美上市
NIOSH将口罩分为9类别:N95,N99,N100R95,R99,R100P95,P99,P100
[P-防护非油性悬浮颗粒,无时限;R-防护非油性悬浮颗粒及汗油性悬浮颗粒,限时8H;P-防护非油性悬浮颗粒及汗油性悬浮颗粒,无时限;95,99,100表示最低过滤效率,100为99.97%]
申请流程:
1、申请三位编码的企业代码[适用于第一次申请或2年内未申请]
2、递交申请资料和检测样品
申请资料包括但不仅限于:产品信息,自测数据,质量保证手册,产品质量控制计划等;
NIOSH安排认可实验室对样品按照STP进行检测;
NIOSH审核递交文件并安排工厂认可检查(1-2天);
NIOSH批准
时间:√申请企业代码:1个月 √审核资料(检测)时间:3到4个月
费用:√审核费:200美元 √发证费:100美元 √现场审核费
√初次申请:√美国境内:2500美金 √美国境外:5000-7500美金 检测费:基于不同检测项目报价
非医用防护口罩如何在美国上市
根据 NIOSH于2020年4月24日公布的 NIOSH Conformity Assessment Letter to Manufacturers,所有首次申请的海外企业为最低优先级别,无法给出审核的时间表。
不接受耳挂式防护口罩的申请。
不回复任何通过公共邮箱发放的申请,比如vip.126.com,qq.com等[企业邮箱]
对于美国境内企业,NIOSH在开发虚拟现场审核的流程。
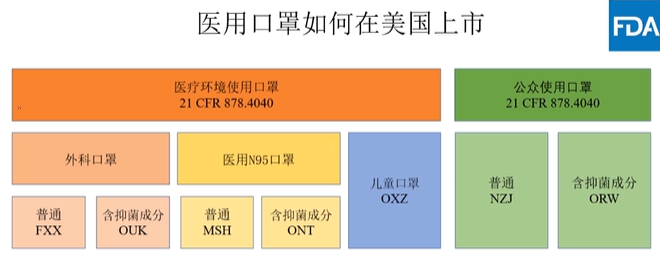
可以510(k)豁免的N95口罩的说明书中不得宣称以下信息:
用于防止特定的疾病或感染(包括但不限于耐甲氧西林金黄色葡萄球菌(MRSA),流感或H1N1);
过滤病毒或者细菌(例如过滤95%的细菌);
具体抗菌抗病毒功能
低变应原性(例如,对于适用于皮肤敏感的用户);
过滤手术烟雾或烟气
可以510k)豁免的N95口罩不可以含有以下技术特性:
抗菌涂料
与产品的呼吸防护特性无关的旨在改变产品性能的涂层
药物输送系统
包含有纳米晶技术的颗粒,纤维,电线,管子,抗菌涂层
该N95口罩是与另一种FDA管制产品的组合
可以510(k)豁免的N95口罩必须获得了 NIOSH的N95认证
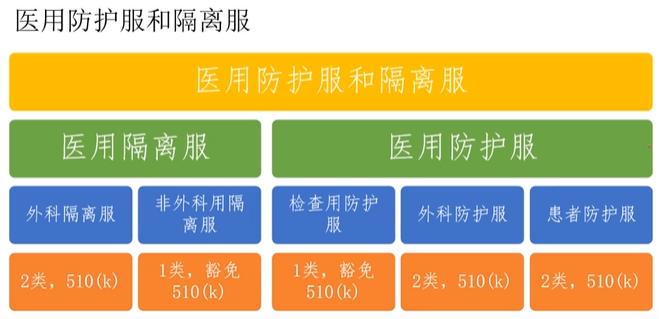
防护服
- 工业用防护服
- 非外科用隔离服:达到 ANSI/AAMI PB70 1级或2级
- 外科隔离服:达到 ANSI/AAMI PB70 3级或4级,并可在无菌环境中使用
工业用防护服
- 非外科用隔离服:达到ANSI/ AAMI PB70 1级或2级
非无菌的可用于医院中与疑似新冠病毒患者的常规接触
无菌的可用于医用中进行低感染风险的手术或介入治疗
- 外科隔离服:达到ANSI/ AAMI PB70 3级或4级,并可在无菌环境中使用
用于高感染风险的手术或介入治疗如新冠病毒相关
体温计
- 红外体温计分类:临床用电子体温计,2类,510(k)
- 水银体温计分类:临床水银体温计,2类,510(k)
- 其他类型电子体温计:临床用电子体温计,2类,510(k)
FDA没有家用的概念,只有处方和非处方的区别。
工业用途测温计在美国如何上市
受美国FDA的CDRH部门管理,和医疗器械在一个部门
红外测温计需要按照FCC要求进行测试
红外测温计需要向美国FDA提交FC报告,取得FCC编号
时间约1个月
呼吸机
- 呼吸机(有创和无创,持续、非持续)是2类,但是高频呼吸机是3类
- 持续呼吸机面罩也是2类
监护仪
- 生命体征监护(不建议给药量,也不能自动给药)都是2类,但不能和美国已经合法分销的产品有显著差异
- 建议给药量或可以自动给药的生命体征监护仪( Vital Sign):3类
- 多参监护仪:2类
- 有发明创造的, De novo或PMA
新冠病毒检测相关体外诊断试剂
- PCR测试设备是2类,510(k),没有EUA途径
- 试剂(PCR或血清法)没有分类,目前只有EUA这一个途径
- 咽拭子:1类
- 病毒管:2类,510(k),没有EUA途径
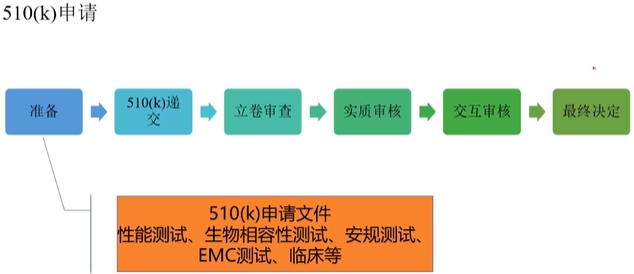
510(k)
510(k)的有效期
只要符合以下条件,一次申请终身有效,没有年费
- 产品没有发生FDA规定的重大变更;
- FDA没有将产品升为3类;
- 没有发生严重的不良事件导致FDA取消这个510(k)。
510(k)申请周期及费用
- 申请时间:6-8个月
- 2020财政年度(2019.10.1-2020.9.30)510(k)申请审核费:
- 标准收费:11594美元
- 小企业收费:2899美元
小企业资质申请:√要求:年销售额小于1亿美元(所有关联企业) √时间:最长60天;
美国FDA工厂注册和产品列示
- 针对所有类别的医疗器械企业和产品,包括510(k)豁免
- 场所注册 Establishment Registration:需列明场所的类别;
- 医疗器械列示 Medical Device Listing
所有根据法规要求向FDA进行注册的医疗器械工厂都必须向FDA确认他们进行商业分销的医疗器械。这个过程称之为医疗器械列示。
- 生产企业、出口商和经销商的场所注册必须至少和一个产品列示同时提交。
工厂注册和产品列示
- 财政年度(每年10.1-次年9.30)
- 2020财政年度工厂注册年费:5236美元;
- 没有小企业优惠;
- 付费需要邓白氏代码,免费申请需要约30天;
- 注册费可以允许由其他企业代理支付;
- 海外企业需要指定美国代理人,没有规定统收费标准。
红外体温计、有无线传输功能、蓝牙传输功能的医疗器械在美国上市的额外要求
- 受美国FDA的CDRH部门管理,和医疗器械在一个部门
- 无线传输、蓝牙传输等功能需要按照FCC要求进行测试
- 需要向美国FDA提交FCC报告,取得FCC编号
- 时间约1个月
紧急使用授权[EUA]
在联邦视频、药品和化妆品法案(FD&C Act)第564部分规定,FDA专员可以在紧急情况下且没有充足的已经批准的或者可以获得替代品时,允许使用未经批准的医疗产品或已经获批产品的未经批准用途用于诊断、治疗或预防严重或威胁生命的疾病。
EUA的时效? 仅在紧急时期有效,由FDA决定,会发布正式公告。目前新冠病毒的紧急时期从2020年2月4日开始。
FDA历史上一共启动了6次EUA;
- √2013年H7N9禽流感;
- √2013年MERS(中东呼吸综合征)
- √2014年埃博拉
- √2015年肠病毒(EV-D68)
- √2016年寨卡病毒
- √2020年新冠病毒。
前5次EUA都仅限于病毒的体外诊断试剂
哪些产品可以申请EUA
- 所有产品都可以申请EUA吗? 不是。FDA会根据具体情况,随时调整可以申请EUA的产品清单
- EUA批准后的有效期有多长? 直到FDA宣布EUA时期结束
- EUA结束后,EUA批准的产品应该怎么办? FDA还没想好,等到宣布EUA结束时候才知道。可能立即停止销售,也可能给在美国境内还未售出的产品一个比较短的宽限期(应该不会超过3个
- 根据FDA要求不需要FDA审核的产品可以随便进入美国市场吗? 错!必须满足FDA公布的此类产品EUA指南中规定的标准、验证确认要求并且标签标识符合美国FDA21 CFR Part801要求以及EUA指南的特殊要求。
新冠病毒体外诊断试剂/试剂盒的EUA
- 适用范围
- 分子诊断法
- 抗原探测诊断
- 血清学诊断
- 政策:接受紧急投权使用(EM申请。
- 请尽量不要在申请EUA的阶段有特别创新点。
- 需要严格遵循FDA的模板,不用提交模板未要求资料,不要缺项,临床数据统计严格按照要求实施
- 模板要求与NMPA要求非常接近。

口罩的EUA 范围
- 适用于医疗用途的口罩和防护口罩
- 不适用于非医疗用途的口罩和防护口罩
- 预期用于预防疾病的口罩属于医疗用途的口罩
- 含任何药物、生物制剂、或抗菌/抗病毒成分的口罩,无论用途,都是医用口罩,但是不可以申请EUA

呼吸机(包括呼吸麻醉机) 范围
- 适用于应急使用授权的呼吸类设备指向具有呼吸衰竭或呼吸不足情况的病人提供通气和呼吸支持的设备,包括但不限于医院用连续呼吸机,家用连续呼吸机,应急使用呼吸机等
- 仅适用于FDA分类为2类的呼吸机
政策
1.FDA仍然建议医疗机构使用己获得FDA许可的传统/全功能的呼吸机;
2.对于已经获得FDA许可上市的呼吸设备,在紧急使用期间,FDA将允许其在适应症,宣称功能,硬件或软件等各方面的有限变更,而不需要对变更递交510(k)申请
3.接受紧急授权,申请人应当向FDA提供基础信息
非侵入远程监护系统 政策
为了应对新冠疫情,对于已经获得FDA许可上市的非侵入远程监护系统,在应急使用期间,FDA将允许其在适应症,宣称功能,硬件或软件等各方面的有限的变更,而不需要对变更递交510(k)申请。此类设备不能申请紧急使用授权(EUA)。
如何申请EUA
- FDA不对EUA收取申请费,但是EUA完成后的场所注册还是正常收费的;
- 每类产品的EUA,FDA分别分配了一个受理渠道,不可以混淆;
- 所有的EUA都要满足FDA关于产品标识要求、医疗器械报告要求、注册列示要求、额外的针对EUA的提示信、部分产品还需要在公司网站上进行额外公示
- 根据FDA的要求,根据产品的风险和特性,还可能需要提交性能测试报告、生物学评价测试、有效期验证方案、稳定性验证方案、临床试验方案等

在FDA网站查看信息,无证书。
