生理信号监测技术多年来取得了巨大进步,对医学诊断和个人医疗保健产生了重大影响,从早期生物电势传感技术的基本进展[1–3],到最近利用手持设备和家用电器中广泛可用的传感技术扩展生理感知范围的最新进展[4–7]。互补金属氧化物半导体技术和电路技术推动了创新性生理传感设备的发展与小型化,在确保通过模拟和数字信号处理方法获得有效医学信息的同时,提升了性能、降低了功耗和成本。这些集成电路发展使得脑信号的可靠测量成为可能,并催生了多种用于临床治疗与诊断的新仪器。
半导体技术的创新使得患者即使在家中也能实现可移动连续时间监测。通过现代集成电路技术实现的这种普适监测,能够推动个性化医疗和预防性医学的发展,以应对因老龄化人口这一当前人口趋势所导致的医疗成本不断上涨问题。患者支持传感器与系统不仅
扩展了现代诊断的能力和准确性,还改善了患者日常生活。
图 2.1 显示了一个用于ECoG信号监测的通用集成电路的主要功能组件,包括模拟前端(AFE)、模拟信号处理器(ASP)、模数转换器(ADC)、数字信号处理器(DSP)、射频(RF)通信和电源管理。本章重点调研这些组件中的AFE、ASP和ADC,它们在低噪声、低功耗的定制集成电路中实现,并针对感兴趣的生理变量的信号条件和范围进行了优化。首先,对电极‐体界面有扎实而全面的理解,对于准确可靠的ECoG感知和信号采集至关重要。
2.2.1 生理要求
前端模拟电路(AFE)、应用信号处理(ASP)和模数转换器(ADC)的主要设计要求由生理信号和人体‐电极接口的特性决定。脑电图(EEG)、心电图(ECG)、肌电图(EMG)和皮层脑电图(ECoG)等生物电位是由发电细胞群产生的电流通过容积传导形成的。脑电图(EEG)是由大脑中大量神经元集体活动所诱发的电位。
心电图(ECG)源自心肌细胞的动作电位,肌电图(EMG)则来自骨骼肌细胞的收缩。各种其他生物电位(如眼电图(EOG)、视网膜电图(ERG)、胃电图(EGG)等)也源于大量发电细胞或离子分布的集体效应。
如图2.2所示,皮层脑电图信号的频率范围非常低,通常低于1千赫兹。当使用表面电极测量时,其幅度非常低,范围从几十到几百微伏。由于皮层脑电图信号可低至1赫兹以下,因此在记录这些信号时会面临电极偏移电压的挑战,该偏移电压可能高达100毫伏,并随时间缓慢变化。此外,如果应用要求在低频(< 1赫兹)下具有低噪声,则需要抑制 1/f噪声。同时,应充分抑制来自电源和其他无关生物电位的共模干扰。
2.2.2 设计因素、相互关系和权衡
设计中用于量化性能和成本的多个因素、它们之间的相互关系以及文献中的典型范围总结于表1.1中。其中一些关系,例如噪声、功耗、带宽、增益和动态范围之间的关系,通常基于基本的物理和信息理论原理而被充分理解,例如功耗通常与带宽呈线性关系,但需考虑噪声因素。其他关系,例如输入阻抗与运动伪影抑制之间的关系,则特定于电极接口处的生理信号和环境因素。这些因素之间的各种交织关系必须在电极、电路和架构层面的设计权衡中进行协同优化。因此,需要深入理解连接这些因素并驱动权衡的基本原理。下文将详细阐述利用低功耗CMOS集成电路及系统特性的具体权衡和架构设计拓扑。
在CMOS工艺中制造的NMOS和PMOS场效应晶体管的横截面,(B) 它们的原理图符号,以及(C) 当体与源极相连、漏极电压偏置在饱和区时,漏极电流ID的对数随栅源电压的变化关系。)
图 2.3(A) 展示了在集成电路CMOS工艺中制造的NMOS和P沟道MOS场效应晶体管的横截面。它们均有四个端子:栅极(G)、源极(S)、漏极(D)和体极(B)。其电路符号如图 2.3(B) 所示。MOS场效应晶体管的工作可分为两种模式,依据栅极与源极之间的电压,分别为强反型和弱反型(或亚阈值)工作模式,如图 2.3(C) 所示。
与模拟CMOS电路设计中的常规做法相反,CMOS器件的弱反型(亚阈值)工作区域已被证明是低功耗生物医学电路设计的理想工作区。在传统设计中,尤其是对于高速应用,弱反型操作被视为截止区的一种非理想特性区,其电流被称为漏电流。近年来,弱反型变得越来越重要,因为其低功耗和低带宽特性非常适合生物医学及其他低功耗传感器应用,这得益于优异的跨导效率。此外,采用深亚微米技术在弱反型下工作的晶体管不会受到许多影响阈上强反型区的工艺相关问题的困扰,例如电子和空穴迁移率中速度饱和引起的增益限制效应[10]。
弱反型下的晶体管模型方程比强反型下更简单、更直观,且具有更宽的缩放范围。工作在弱反型下的晶体管中,电子能量完全基于玻尔兹曼分布,与工艺技术无关。流经晶体管沟道的漏极电流不是通过漂移,而是通过扩散产生,并随栅极电压指数式地变化。因此,弱反型操作特别适合用于实现对数线性电路和对数域滤波器。
弱反型区的漏极电流 $i_{DS}$、跨导 $g_m$ 和单位增益频率 $f_t$ 遵循 [11]:
$$
i_{DS} = i_{DS0} frac{W}{L} e^{v_{GS}/(nV_t)}(1 – e^{-v_{DS}/V_t}), quad (2.1)
$$
$$
g_m = frac{I_{DS}}{nV_t}, quad (2.2)
$$
$$
f_t = frac{I_{DS}}{2pi nV_t(C_{gs} + C_{gd} + C_{gb})} propto I_{DS}. quad (2.3)
$$
由于跨导与漏极电流成正比,单位增益频率也是如此。因此,电流与带宽之间的权衡非常直接:电流越大,带宽越宽。
饱和区和弱反型下的热噪声与漏极电流成正比,如下所示[12]:
$$
overline{i^2_{n,th}} = 2qI_{DS}Delta f, quad (2.4)
$$
其中 $Delta f$ 是信号带宽。相对噪声功率(信噪比的倒数)与漏极电流成反比:
$$
frac{overline{i^2_{n,th}}}{I_{DS}^2} = frac{2qDelta f}{I_{DS}}. quad (2.5)
$$
因此,在弱反型区,信噪比与偏置电流呈线性正比关系。对于大多数信号带宽较窄的生物医学应用而言,工作在弱反型区的电路即使采用较低的电流,仍能在最高能效下提供足够大的信噪比。
闪烁噪声,也称为1/f噪声或粉红噪声,在低频时也是一个重要的噪声源。已知在Si/SiO2界面附近的陷阱中载流子的随机捕获以及一些其他机制是1/f噪声[13,14]的主要来源。
$$
overline{i^2_{n,f}} = frac{g_m^2 K}{C_{ox} W L} cdot frac{1}{f} Delta f, quad (2.6)
$$
其中K是与工艺相关的常数,W和L分别为MOS晶体管的宽度和长度,$C_{ox}$为栅极氧化物电容。已知PMOS晶体管的1/f噪声小于NMOS晶体管,因此在生物传感中用于低噪声、低频应用的前端放大器输入差分对时,应选用PMOS晶体管。增大MOS器件尺寸也可使1/f噪声随面积成反比地降低。
1/f噪声拐点频率 $f_c$ 是表征在整个频谱范围内1/f噪声相对于热噪声比例的重要指标。1/f噪声拐点 $f_c$ 定义为1/f噪声与热噪声幅值相等时的频率,在弱反型条件下由下式给出:
$$
overline{i^2_{n,th}} = overline{i^2_{n,f}}, quad (2.7)
$$
$$
2nkTg_mDelta f = frac{g_m^2 K}{C_{ox} W L} cdot frac{1}{f} Delta f, quad (2.8)
$$
$$
f_c = frac{K}{C_{ox} W L g_m} cdot frac{1}{2nkT}. quad (2.9)
$$
1/f噪声拐点可能因工艺制造质量的不同而从几百赫兹到几兆赫兹不等。此外,它还取决于偏置电流:偏置电流越低,1/f噪声拐点就越低,因此1/f噪声对总噪声的相对贡献也就越小。
对于脑电图(EEG)采集等低噪声生物医学应用,斩波稳定技术被广泛用于进一步降低1/f噪声。为了有效发挥作用,斩波频率需明显高于1/f噪声拐点频率,在这些应用中通常介于100赫兹至10千赫之间。其他技术如自动归零和相关双采样也可用于降低1/f噪声。
在生物医学电路设计中,需要仔细考虑MOS晶体管中的三种电流,如下所述。这三种电流如图2.3(A)中的亚阈值电流$I_{sub}$、栅极漏电流$I_g$以及p‐n结反向偏置漏电流$I_{np}$[15]所示。
在可穿戴生理监测系统的设计中,最具挑战性的部分之一是仪表放大器(IA)的实现,这些仪表放大器从电极获取生物信号,并进行模拟信号处理与调理。仪表放大器需满足第2.2.2节中前述几乎所有具有挑战性的设计规格。
经典的三运放仪表放大器足以实现高输入阻抗、高共模抑制比和足够的增益。然而,由于使用了三个放大器,它消耗较大的功耗和面积[16]。对于微功率生物电势采集前端,图 2.4(A)(类似于[17])和 (B)(类似于[18])所示的结构被广泛使用。交流耦合输入电容器 $C_C$ 阻断电极偏移电压。由于在集成 CMOS工艺中电容器具有良好的匹配性能,增益可以被精确控制。一个大电阻 $R_f$,通常通过伪电阻或开关电容电路(第2.6.2节)实现,用于建立放大器输入节点的直流偏置,并与 $C_f$ 共同实现高通滤波。电容值的失配会导致共模抑制比下降。该架构可达到的实际共模抑制比约为60至70 dB。此外,$C_C$ 决定了输入阻抗。因此,在设置 $C_C$ 的值时,需要同时考虑共模抑制比和输入阻抗。
仪表放大器的传递函数如下[17]:
$$
A_v(s) = -frac{C_C}{C_f} cdot frac{1 – sC_f/g_m}{(1 + 1/sR_f C_f)} cdot frac{1}{(1 + s(C_C + C_L + C_C C_L / C_f)/g_m)}, quad (2.10)
$$
其中$g_m$是运算跨导放大器的跨导。其通带增益由电容器$C_C$与电容器$C_f$的比值决定。高通截止频率$f_{HP}$由下式给出
$$
f_{HP} = frac{1}{2pi R_f C_f}. quad (2.11)
$$
低通截止频率 $f_{LP}$ 可通过负载电容 $C_L$ 进行控制,并近似由以下公式给出
$$
f_{LP} approx frac{g_m C_f}{2pi C_C C_L}, quad (2.12)
$$
当$C_L gg C_f$且$C_C/C_f gg 1$时。$g_m/C_f$处的右半平面零点可以通过在$C_f$上串联一个$1/g_m$电阻来消除。但在许多情况下可以忽略该零点,因为它所处的频率远高于生物医学应用的感兴趣频率范围。
单级仪表放大器的主要噪声来源是运算跨导放大器(OTA)和反馈电阻 $R_f$。由这些源引起的输入参考噪声分别如下所示:
$$
sqrt{overline{v^2_{ni,Rf}}} = sqrt{frac{4kT}{R_f}} cdot frac{1}{sqrt{2pi f C_{in}}}, quad (2.13)
$$
$$
sqrt{overline{v^2_{ni,amp}}} = sqrt{overline{v^2_{ni,system}}} cdot left(frac{C_f + C_{in} + C_C}{C_C}
ight), quad (2.14)
$$
其中 $C_{in}$ 表示运算跨导放大器输入节点处的寄生电容 $V_{IN+}$和 $V_{IN-}$[16]。在感兴趣的低频范围内,$R_f$产生的噪声可能占主导地位。因此,为了减小$R_f$[19]的噪声贡献,需要满足以下条件:
$$
frac{C_L}{C_C} gg frac{2}{3} frac{f_{LP}}{f_{HP}}. quad (2.15)
$$
在实际电路中,运算跨导放大器的噪声远大于$R_f$[19]的噪声。
作为低噪声和低电源电流前端仪表放大器设计的基准,噪声效率因子(NEF)用于比较电流‐噪声性能:
$$
NEF = frac{V_{rms,in}}{sqrt{2I_{tot}/pi V_t cdot 4kT cdot BW}}, quad (2.16)
$$
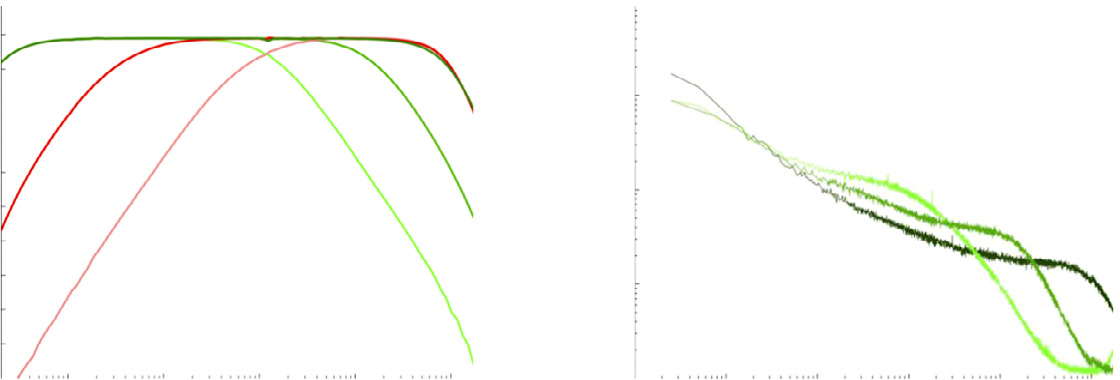
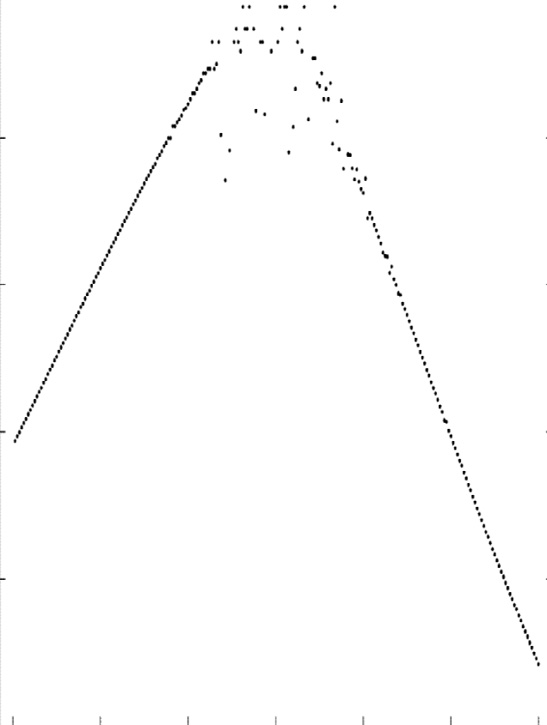
其中 $V_{rms}$为总输入参考噪声,$I_{tot}$为系统的总电流消耗,$V_t$为热电压,BW为系统 −3‐dB带宽[20]。NEF对应于在相同噪声水平下,相对于单个双极结型晶体管配合理想恒流负载的归一化供电电流,定义了理论极限(NEF = 1)。实际上,采用输入差分对的差分仪表放大器在相同跨导下需要两倍的供电电流,因此NEF值大于2。最先进的仪表放大器通常具有2.5至10的NEF。最近,已展示出采用电流复用技术提升输入级跨导的仪表放大器,其实现的NEF低于 2[21–24]。作为参考,图1.6[25,17,18,26–37]展示了最先进的仪表放大器测得的NEF及性能。
尽管NEF被广泛用于对仪表放大器进行基准测试,但NEF实际上只是带宽、噪声和电流这三个性能指标之间的权衡,而忽略了共模抑制比、输入阻抗、功耗、输入动态范围等许多其他关键性能因素。改进后的NEF指标,其一是用功耗替代电流[38],另一个是包含功耗消耗和动态范围[39],已被提出作为更全面的神经电子接口替代方案。
运算跨导放大器(OTA)是仪表放大器中的最重要模块,如图 2.4(A)(单端)和(B)(全差分)所示。在多种放大器中,最常用的两种放大器——对称 OTA(或电流镜OTA)和折叠共源共栅OTA——如图 2.5[17,33]所示。两者均为单级放大器,因为它们在 $V_{OUT}$处仅有一个高阻抗节点。这两种放大器的增益等于输入对管的跨导与输出阻抗的乘积。全差分放大器(此处未显示)通常需要共模反馈,设计上更为复杂,但相比单端方案具有更优的共模抑制比和电源抑制比。
对称OTA。(B) 折叠共源共栅OTA。)
2.5.1 噪声‐功耗权衡
生物医学应用的前端放大器噪声至关重要。在给定跨导$g_{m1}$的情况下,对于 M1–M2, $g_{m3}$ (对应M3–M6 )和$g_{m7}$ (对应M7–M8, )时,图2.5中各放大器的输入参考热噪声分别如下所示[17]:
$$
overline{v^2_{ni,sym}} = frac{16kT}{3g_{m1}}left(frac{3}{4}n + frac{2g_{m3}}{g_{m1}} + frac{g_{m7}}{g_{m1}}
ight)Delta f, quad (2.17)
$$
$$
overline{v^2_{ni,folded}} = frac{16kT}{3g_{m1}}left(frac{3}{4}n + frac{g_{m3}}{g_{m1}} + frac{g_{m7}}{g_{m1}}
ight)Delta f quad (2.18)
$$
其中$n$取决于耗尽层电容与氧化物电容之间的电容比,该值通常介于1.2至1.8之间。在这些公式中,假设M1和M2工作在弱反型区,而其他晶体管工作在强反型区。共源共栅MOSFETs在噪声方面的贡献可忽略不计。这些公式明确表明,为了获得良好的噪声性能,$g_{m1}$应尽可能大。在给定偏置电流的情况下,输入对晶体管(M1和M2)应在弱反型区工作,以实现更高的$g_m/I_D$效率。相反,M3–M8需要工作在强反型区,以获得更低的$g_m$。由于近似认为$g_{m1}$远大于$g_{m3}$和$g_{m7}$,输入参考噪声被简化为
$$
overline{v^2_{ni,sym}} sim overline{v^2_{ni,folded}} sim frac{4nkT}{g_{m1}}Delta f = frac{4n^2kTV_t}{I_1}Delta f propto frac{1}{ ext{current}}. quad (2.19)
$$
通过合理设计放大器的尺寸,电路设计人员唯一可以调控的因素就是电流。因此,功耗与噪声之间的权衡关系十分直接:电流越大,噪声越低。在对功耗有更严格限制的情况下,折叠式放大器优于前述两种放大器,因为它只有两个支路。然而,其输出摆幅范围远小于前述两种放大器。
2.5.2 The $g_m/I_D$ 设计方法
The $g_m/I_D$ 设计方法对于低功耗和低噪声设计非常实用。$g_m/I_D$ 跨导效率表示晶体管在较低电流下实现更高增益的效率;如图 2.6(A) 所示,弱反型下的$g_m/I_D$ 大于强反型下的值。这意味着晶体管在弱反型下工作更高效。
如图 2.6(B) 所示,通过调整器件尺寸以获得期望的跨导效率,可以调控给定偏置电流下晶体管的工作区。但应注意,为获得更高跨导效率而增大器件尺寸会占用更大的面积,从而引入更大的寄生电容。
2.5.3 稳定性
负反馈几乎被用于所有放大器中,以获得精确的增益,该增益由线性无源元件的反馈比决定,而不受开环增益的影响,同时还能展宽带宽并增强噪声抑制。然而,高增益系统中的反馈可能会受到不稳定性因素的影响,需要仔细进行设计考虑。用于生物医学应用的仪表放大器不需要很宽的带宽,因为感兴趣频率范围较低,通常小于1千赫兹。然而,由于低功耗的限制,典型电流仅为几十到几百纳安,晶体管通常尺寸较大,以实现更好的匹配和低噪声性能,这导致电导较低而寄生电容较大,可能恶化稳定性。
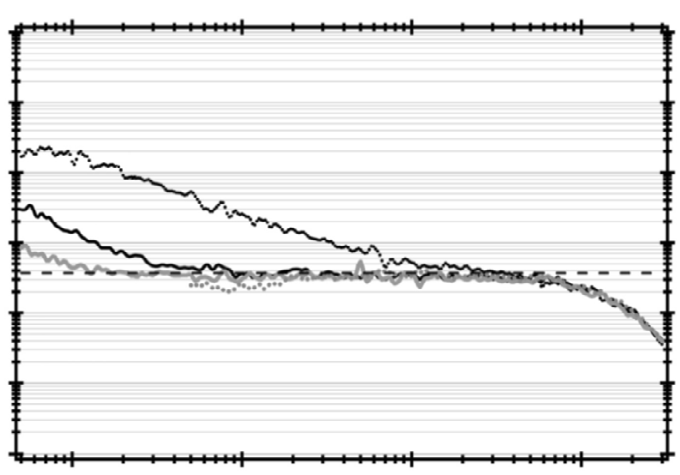
图 2.7 显示了放大器的开环伯德图。由于如上所述,$V_{OUT}$是唯一的高阻抗节点,因此位于 $V_{OUT}$处的极点位于非常低的频率。反馈建立了如图 2.7中虚线所示的闭环增益。反馈的闭环增益与放大器的开环增益的交点决定了单位环路增益频率$f_K$。相位裕度由以下公式给出:
$$
ext{Phase Margin} = 90 – an^{-1} frac{f_K}{f_{p2}}, quad (2.20)
$$
其中$f_{p2}$是第二个极点频率。因此,第二个极点的位置对相位裕度至关重要。如果图M3–M8 2.5(A)–(B)中的器件假设具有相同的过驱动电压,则 $V_3$节点由于器件尺寸较大而具有更大的栅极电容,并可能产生第二个极点。然而,由于存在双信号路径,该极点之后总会跟随一个零点,因此不会严重影响相位裕度。此外,在全差分放大器中,$V_3$节点处不会产生极点‐零点对。由于 $V_2$节点处的结电容较大,该处的极点可能低于极点‐零点对,M1和M2,的尺寸设计适用于大输入对跨导和低 1/f噪声。在某些情况下,这可能会产生双峰,导致相对较长的稳定时间,但对于包括皮层脑电图记录在内的许多生物医学应用而言,仍在可接受范围内。
2.6.1 失调和1/f噪声抵消技术
自动归零开关电容技术用于消除1/f噪声以及放大器的失调[40]。然而,在自动归零后,采样电容器上的复位开关断开会引入显著的奈奎斯特‐约翰逊噪声(kT/C噪声)[41,42]以及随机电荷注入,从而污染采样信号。仅1–10 pF电容的kT/C噪声就约为几十微伏。为解决前端模拟电路输入端的这一噪声问题,可采用信号折叠和数字辅助信号拼接技术,从而放宽电压动态范围的要求[43]。相反,几乎所有仪表放大器都采用斩波稳定技术来消除1/f噪声。
斩波调制技术广泛应用于抑制1/f噪声及其他低频噪声,例如爆米花噪声、电压偏移和漂移。该技术特别适用于对相对较弱的生物电位(如皮层脑电图和脑电图)进行高灵敏度采集,这类应用要求极低的输入参考噪声。放大器所用斩波调制技术的基本原理已被深入研究[40,44–46],如图2.8所示。低频带限输入信号 $V_{in}$在放大器前端通过一个方波斩波信号进行调制。由此产生的信号波形 $V_a$被移至斩波频率$f_{ch}$处,从而使干扰源不在信号频带内。经过放大后,再使用相同的斩波信号进行解调,放大的输入信号分量被移回直流基带频率处的 $V_b$,而干扰源则被移至信号频带之外的$f_{ch}$处。所有不希望存在的干扰源及其谐波均通过低通滤波器滤除,理想的输入信号最终在输出端 $V_{out}$处恢复。
残余失调主要由输入斩波调制器的非理想性引起。输入斩波器中时钟馈通和电荷注入的失配会产生开关瞬态尖峰,这些尖峰在输出斩波器处被解调为残余输出失调。为了最小化失调,首先需要仔细设计和布局。连续[25,29,31,33]或数字[26]直流伺服环可以减小残余失调,并缓解由于放大器带宽有限所导致的信号失真问题。此外,还可以应用滤波技术[30,47,48]。
输出纹波由放大器的输入失调引起,并且由于失调也会被放大,可能导致放大器输出饱和。该纹波可以通过连续纹波抑制环路[31]和数字前台校准[26]来减小。
2.6.2 用于亚赫兹高通截止的伪电阻
在典型的生物医学传感器中,高通截止频率需要远低于1赫兹,这要求达到TΩ范围的超高压电阻。使用片上电容器和多晶硅电阻实现亚赫兹时间常数,在集成实现中会占用不切实际的大面积。
最常用的解决方案是将1–10 pF电容器与基于P沟道MOS的MOS‐双极型伪电阻组合,如图2.9(A)–(F)[49,17]所示。其中最基本的拓扑结构是一个P沟道MOS,其栅极和体端相连,如图2.9(A)[49]所示。该P沟道MOS伪电阻在正向($V_A>V_B$)结合了一个p‐n结,在反向($V_A<V_B$)结合了一个二极管连接方式的亚阈值P沟道金属氧化物半导体。由于存在源极‐体连接,栅极连接的漏极端子无泄漏,理想情况下可连接至OTA的浮空输入等对泄漏敏感的一侧。单个MOS‐双极型伪电阻的测量电阻如图2.9(I)[17]所示。另一种配置是将P沟道MOS的栅极连接至偏置电压
图 2.9(E)中,通过栅极电压实现可控电阻[18,52–54,39]。然而,图 2.9(A)–(E)中的基于PMOS的伪电阻在跨电压偏离零点时,其电阻值急剧下降,导致信号相关失真并限制了电压动态范围[32]。图 2.9(F)中的伪电阻具有更平衡的电阻特性,线性范围更宽,可达数百毫伏。通过使用辅助放大器,可实现更宽的线性范围[55]。
然而,标准的MOS‐双极型伪电阻除了可能对光和电磁干扰敏感外,还会受到工艺、电压和温度(PVT)变化的影响,从而导致截止频率的变化。开关电容可用于实现片上对PVT不敏感的高电阻,如图2.9(G)[29]所示。在此拓扑结构中,开关频率$f_s$和中间的电容器精确地决定了电阻值,为$1/f_sC$。图2.9(H)中的开关电容电阻通过在开关电容电路中利用电荷共享实现十倍的电阻增加,缓解了可制造性和干扰问题[33]。
2.6.3 共模抑制比增强技术
共模干扰对生物医学信号传感系统来说是一个棘手的挑战。这种干扰的主要来源是电力线,它们会以电的方式耦合到人体。为了确保高信号质量,系统需要具有高的共模抑制比,以抑制共模干扰。
差分信号线之间以及各通道之间的精确元件匹配是实现高共模抑制比的最基本要求。良好的匹配涉及从精心布局到智能架构设计选择的各种技术。
2.6.3.1 驱动右腿技术
右腿驱动技术通过放置在右腿上的附加电极将放大后的输入共模电压反馈至人体,用于心电图测量。这种负反馈降低了反馈环路的阻抗,从而按反馈环路增益的倍数衰减传感器输入端的共模干扰电压[56,57]。通过右腿驱动负反馈,电极阻抗和共模电压均被降低,降低倍数等于右腿驱动环路增益。因此,为了获得更高的增益,可以采用开环右腿驱动放大器[58]。数字辅助右腿驱动电路在电源频率处提供更大的增益以实现更高的抑制能力,而在其他频率处则保持较低增益以确保稳定性[59]。在干电极应用中,将共模反馈连接到有源电极上各个放大器的负输入端,也能提高共模抑制比,并确保稳定性不受电极阻抗变化的影响[26]。
2.6.3.2 输入阻抗提升技术
电极阻抗的变化和失配也会降低共模抑制比,减小信号幅度,并使系统更容易受到运动伪影的影响。因此,生物电位传感器的输入阻抗应远高于电极阻抗以及人体与电极之间的界面阻抗。通过正反馈可对交流耦合输入电容进行自举,从而提升输入阻抗[60,26,34],使输入阻抗达到GΩ量级。为了进一步将输入阻抗提升至TΩ级别,可以采用带有有源屏蔽的单位增益放大器,对输入晶体管的电容及其他所有寄生电容[61]进行自举。
本章首先介绍了可靠皮层脑电图信号采集的系统要求。随后,我们回顾了用于皮层脑图信号感知的低功耗集成电路设计的基本原理,例如亚阈值和$g_m/I_D$设计方法。先进诸如伪电阻、斩波、驱动右腿电路和阻抗自举等技术也已涵盖。
