2025年11月14日至11月20日,动脉智库重点整理了医疗器械产品国内外获批资讯及数据,涉及6个器械获FDA批准,3个器械获欧盟及其它批准,1个器械获NMPA创新产品批准,另有435个器械获NMPA批准注册文件。
海外获批
一、FDA
1. 血糖监测系统研发商Dexcom智能基础系统搭配15天CGM传感器获FDA批准,优化2型糖尿病胰岛素剂量
2025年11月20日,美国食品药品监督管理局(FDA)已批准Dexcom智能基础系统,该系统旨在为2型糖尿病患者优化基础胰岛素剂量。该技术通过个性化建议改善糖尿病管理,并配备使用寿命达15天的持续血糖监测(CGM)传感器。Dexcom智能基础系统通过数据驱动的个性化方案提升基础胰岛素剂量精准度。该系统整合先进CGM技术,可长期持续监测血糖水平,从而实现更精确的胰岛素给药调整。此项突破性进展聚焦于实时监测支持的个性化治疗策略,标志着糖尿病护理领域的重要进步。
2. 泰利福Hem-o-lok PurplePlus获FDA批准上市
泰利福宣布其新版Hem-o-lok——Hem-o-lok PurplePlus获FDA批准上市。该结扎夹为大外科手术中重要止血产品,是闭合7mm以上血管最安全有效的方式,自上市以来已成为闭合大血管金标准,虽专利到期后国内多家企业仿制,但原版设计仍堪称完美。随着医疗技术发展,泰利福对其进行升级,推出Hem-o-lok PurplePlus,其主体结构与上一代基本一致,细节优化,采用交错齿形、三点固定和柔性铰链设计,有效防止滑移、降低滑脱风险并简化操作流程。该产品优势在于能与5mm施夹器配套使用,入路尺寸缩减四倍,且能闭合2-13mm血管和组织,减少临床库存。
3. 拓普康获得FDA 510(k)许可并推出OMNIA,一款全自动的四合一预测试系统
2025年11月19日,拓普康医疗公司宣布获得FDA 510(k)许可,并在美国推出了OMNIA,一款全自动的四合一预检测系统。这款紧凑型设备将客观验光、角膜曲率测量、眼压测量和角膜厚度测量集成在一个平台上,使眼科护理专业人员能够以最少的操作员培训获得一致的测量结果。据拓普康医疗首席执行官兼总裁阿里·塔弗雷什介绍,OMNIA提供快速、可靠的数据,缩短了数据收集时间,提高了临床精确度,并增加了与患者的互动时间。OMNIA专为诊所和高流量医疗机构设计,通过将四项必要测试整合到一台仪器中简化了预检测流程,减少了测试时间和患者等待时间,同时节省了设备空间。该设备配备了360度旋转触摸屏,便于灵活设置和患者定位,其DICOM兼容性确保与电子病历系统和数字化实践管理工具无缝集成。
4. 捷迈邦美升级版膝关节机器人获批FDA
骨科巨头捷迈邦美宣布其膝关节置换手术机器人平台Rosa Knee的升级版——Rosa Knee with OptimiZe技术,获美国FDA批准用于机器人辅助全膝关节置换。OptimiZe版本重点放在三个方向:强调“个体化”,为术者提供定制手术规划与界面;提升“精准与可重复性”,细化假体定位等工具;优化“人机交互与工作流”,减少术中干扰和操作负担。此次获批是捷迈邦美扩展手术机器人产品组合的重要动作,被视为骨科机器人“智能化迭代”的关键里程碑。OptimiZe核心是对四个关键环节系统升级,其中OptimiZe Planning是升级核心,可减少规划时间,结构化术者策略,实时更新规划过程,让经验被“结构化”和“可复制化”。
5. Meduloc宣布自主研发的Meduloc system获FDA批准上市
Meduloc宣布自主研发的Meduloc system获FDA批准上市,为标准骨折领域带来全新固定技术,用于治疗小型长骨骨折。该系统由柔性镍钛合金制备的Y型植入物和接骨螺钉组成,设计简洁独特,提供旋转及长度稳定性,使医生能避开关节囊入路,帮助患者实现早期活动、减少并发症、降低手术复杂性并加速康复。其适用于成人和儿童多种骨折类型,仅三种尺寸就能满足所有临床需求,减轻医院库存压力。Meduloc system优势明显,可为骨折部位提供旋转稳定性,可精确匹配患者解剖结构,且通过微创入路保护关节和软组织,无需二次手术。Meduloc将发布美国市场商业计划,拓展合作网络以支持技术推广。
6. Integra LifeSciences超声抽吸系统FDA批准用于心脏手术
FDA批准Integra LifeSciences的CUSA Clarity超声手术抽吸系统扩展适应症,用于心脏手术特定领域,标志着该系统从神经外科等传统应用向心血管手术拓展,或提升瓣膜置换和修复手术的安全性和效率。超声吸引器装置利用超声波振动高精度去除软组织,在神经外科等精细手术中价值突出。CUSA Clarity系统是CUSA平台最新迭代,有超40年临床应用历史,最早于1978年就有相关神经外科肿瘤切除的同行评议临床出版物。其开发历经多次FDA 510(k)申请,2016年初上市,2020年获批用于神经外科特定适应症,此次心脏手术适应症研发源于临床需求,2020年提交申请,2025年11月获批。
二、欧盟及其它
1. 国际化加速进行,德晋医疗DragonFly™破局阿根廷与越南
德晋医疗核心产品DragonFly™经导管二尖瓣夹系统获阿根廷与越南上市批准,此前已获中国药监局批准、欧盟MDR认证及多国和地区监管机构批准,国际化加速。其成功进入国际市场,在于解决临床核心难点,可视化与刻度化操作系统缩短学习曲线,保障手术效率与成功率;瓣膜夹自由角度锁定搭配中央封堵网,兼顾即刻张力与远期稳定。这些优势获国际认可,在PCR London Valves 2025上,专家专题演讲其最新临床成果,引发关注。阿根廷Marcelo Aguero教授肯定其临床实用性,王建安院士称其治疗有效终点成果显著,超八成患者无需二次治疗,无严重不良事件。
2. 赛诺医疗冠脉球囊产品在海外获得注册证
赛诺医疗11月18日公布,公司于2024年11月向巴西国家卫生监督局(ANVISA)递交了SC HONKYTONKTM冠脉球囊扩张导管的注册申报资料,近日收到ANVISA通知,该资料已获批准,意味着赛诺医疗的这款冠脉球囊产品成功在海外获得注册证。SC HONKYTONKTM冠脉球囊扩张导管适用于对冠状动脉的狭窄节段或搭桥狭窄部位进行球囊导管扩张,以改善心肌灌注,此次获批有助于公司进一步拓展海外市场,提升国际竞争力。
3. 图迈®机器人的影像系统组件DFVision® 3D荧光电子内窥镜获得欧盟CE认证
图迈®多孔腔镜手术机器人(简称图迈®机器人)的影像系统组件DFVision® 3D荧光电子内窥镜获得欧盟CE认证,标志着国产手术机器人在自主创新实力方面再次获得国际权威监管机构的认可。凭借多模态荧光功能,该系统可在八种不同荧光显示模式之间实时切换,在全科室高难度复杂手术中提供更高的肿瘤识别精度与更清晰的术野成像,帮助外科医生精准辨识病灶、血管结构与组织灌注,提高手术安全性与操作效率,显著改善手术效果和患者预后。这一突破将加速图迈®机器人在欧洲及其他国家高端市场的商业化步伐,推动“中国创造”在全球高端手术机器人领域持续崛起。图迈®机器人荧光成像系统支持8种不同荧光显示模式实时切换,并保持焦面同步与画面一致,使术者在同一画面中既能观察荧光信号,又能清晰看到非荧光组织细节,突破了传统黑白荧光成像下无法直接操作的限制,实现在一个画面中完成组织辨认、病灶识别、切除及残留确认,无需术中频繁切换,大幅提升手术效率与便利性,同时增强手术的安全性与精准性。
国内获批
一、创新器械获批
1. 一次性使用压力监测心脏脉冲电场消融导管获批上市
2025年11月20日,国家药品监督管理局批准了上海微创电生理医疗科技股份有限公司的一次性使用压力监测心脏脉冲电场消融导管注册申请。该产品由导管和连接尾线组成,基于应变片原理的压力传感器设计,结合脉冲电场技术、磁场定位技术、盐水灌注技术,与心脏脉冲电场消融设备配合使用,可用于房室结折返性心动过速和房室折返性心动过速的治疗;与三维心脏电生理标测系统配合使用,可提供导管在心内的位置信息以及进行导管头端和心壁之间触点压力的实时测量。该产品为室上性心动过速治疗提供了更多选择。
二、NMPA最新获批器械产品明细
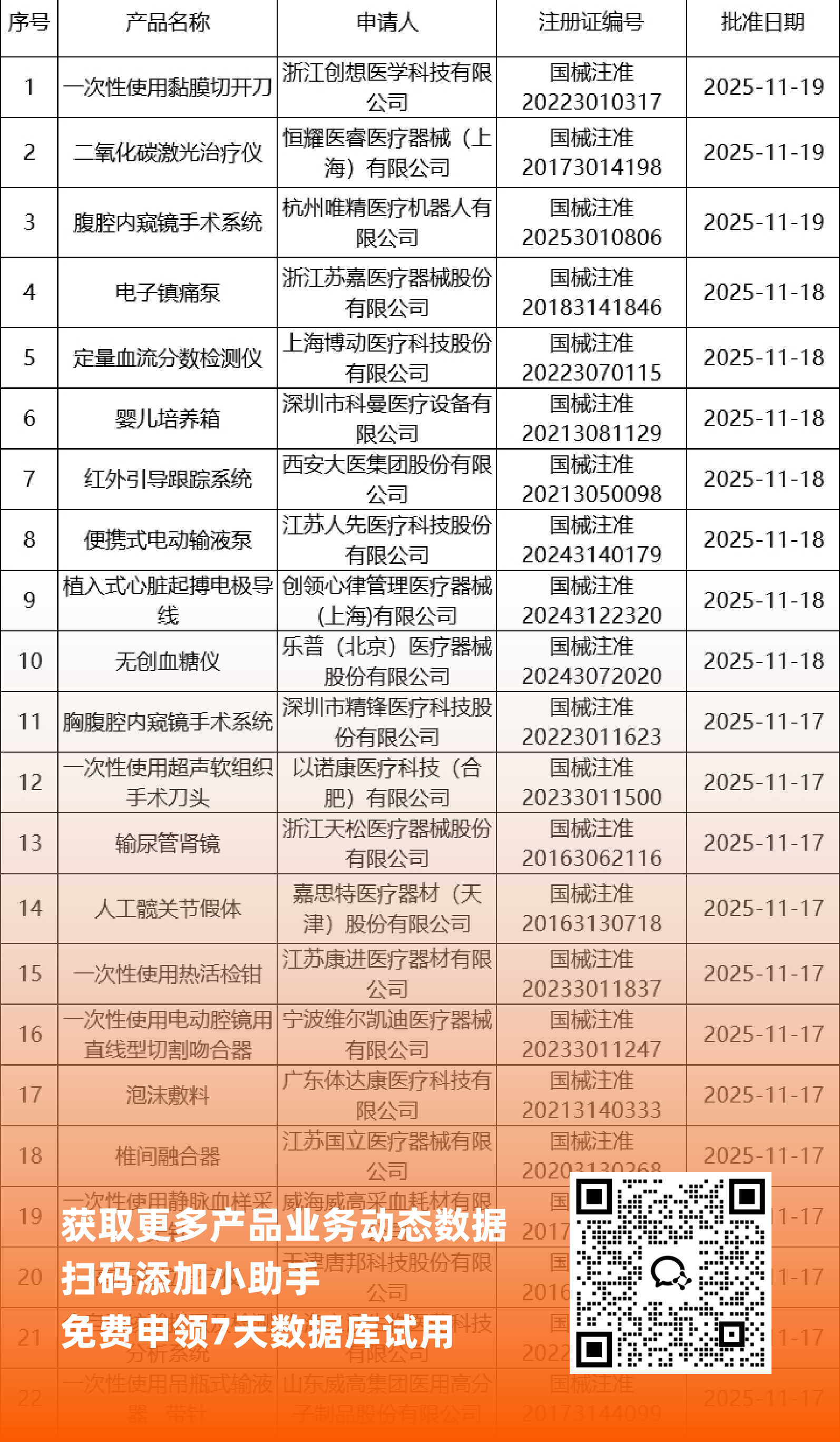
*声明:
1.文中所有相关数据和事件信息均来自于公开渠道,包含媒体报道,企业官网,工商信息等,可能出现遗漏或错误;
2.动脉智库仅进行数据梳理和呈现,不提供任何形式的投资建议、见解或立场;
3.如需对数据纠错或进行其他相关反馈,欢迎扫描二维码联系小助手处理。
