解答:
解:(1)Fe3+有强氧化性,能把金属铜氧化成铜离子,自身被还原成 Fe2+,反应方程式为2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)设计成原电池时,负极上发生氧化反应,正极上发生还原反应,该电池反应中三价铁离子得电子发生还原反应,所以正极上的电极反应式为Fe3++e–=Fe2+(或2Fe3++2e–=2Fe2+),铜失电子发生氧化反应,所以负极上的电极反应式为Cu=2Cu2++2e–(或Cu-2e–=Cu2+);
电池反应中发生氧化反应的金属作负极,所以铜作负极,不如负极活泼的金属或导电的非金属作正极,可选石墨作正极,发生还原反应的电解质溶液作原电池的电解质溶液,所以该原电池图为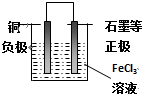 ,
,
故答案为: ;2Fe3++2e–=2Fe2+;Cu-2e–=Cu2+;
;2Fe3++2e–=2Fe2+;Cu-2e–=Cu2+;
(3)①碱性溶液中负极反应为2H2-4e–+4OH–=4H2O,正极反应为O2+4e–+2H2O=4OH–,电池总反应都为2H2+O2=2H2O,溶液体积增大,OH–浓度减小,则pH减小,
故答案为:2H2-4e–+4OH–=4H2O;O2+4e–+2H2O=4OH–;减小;
②反应Ⅰ中Li元素化合价升高,被氧化,Li为还原剂,n(Li)==1mol,由方程式可知7g Li可吸收标况下H20.5mol,标准状况下的体积为11.2L,转移电子1mol,
故答案为:Li;11.2;1.
解答:
解:(1)Fe3+有强氧化性,能把金属铜氧化成铜离子,自身被还原成 Fe2+,反应方程式为2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)设计成原电池时,负极上发生氧化反应,正极上发生还原反应,该电池反应中三价铁离子得电子发生还原反应,所以正极上的电极反应式为Fe3++e–=Fe2+(或2Fe3++2e–=2Fe2+),铜失电子发生氧化反应,所以负极上的电极反应式为Cu=2Cu2++2e–(或Cu-2e–=Cu2+);
电池反应中发生氧化反应的金属作负极,所以铜作负极,不如负极活泼的金属或导电的非金属作正极,可选石墨作正极,发生还原反应的电解质溶液作原电池的电解质溶液,所以该原电池图为 ,
,
故答案为: ;2Fe3++2e–=2Fe2+;Cu-2e–=Cu2+;
;2Fe3++2e–=2Fe2+;Cu-2e–=Cu2+;
(3)①碱性溶液中负极反应为2H2-4e–+4OH–=4H2O,正极反应为O2+4e–+2H2O=4OH–,电池总反应都为2H2+O2=2H2O,溶液体积增大,OH–浓度减小,则pH减小,
故答案为:2H2-4e–+4OH–=4H2O;O2+4e–+2H2O=4OH–;减小;
②反应Ⅰ中Li元素化合价升高,被氧化,Li为还原剂,n(Li)==1mol,由方程式可知7g Li可吸收标况下H20.5mol,标准状况下的体积为11.2L,转移电子1mol,
故答案为:Li;11.2;1.
