三维打印(3DP)是一种极具颠覆性的技术,有望改变制药、处方和药品生产的方式。由于其低成本、多样性、便携性和简便性,熔融沉积成型(FDM)非常适用于数字健康领域的多种药物应用。通过结合数字技术和基因组技术,FDM能够从具有独特形状、尺寸和剂量的三维模型远程制造药物递送系统,从而更好地控制药物的释放特性及其生物利用度。这一系统有望加速数字医疗革命,实现按需为每位患者量身定制药品。迄今为止,多种FDM三维打印的医疗产品(如植入物)已实现商业化并用于临床。然而,在制药领域仍存在一定的监管障碍。本文综述了FDM技术在医学和药物研究中的最新进展,包括其在个性化治疗以及数字健康网络互联方面的应用,并探讨了当前面临的主要挑战,重点分析了推动该技术在药房和医院中集成所需的未来发展方向。
关键词
:熔融沉积成型、材料挤出、个性化药物、熔融丝线制造、以患者为中心的药物、数字化药房
三维打印(3DP)作为一项新兴且革命性的制造工具,在许多行业中获得了快速发展。这种增材制造系统正在迅速改变产品的设计和生产方式:通过使用三维计算机模型,可在自动化条件下逐层创建定制化的物体。因此,该技术能够弥合想象世界与现实世界之间的差距。目前市面上已有多种3D打印技术,但在所有系统中,熔融沉积成型(FDM)是制药领域内研究最为广泛的3D打印技术(Alhnan 等,2016;Alomari 等,2015;Awad 等,2018;Goole 和 Amighi,2016;Norman 等,2017;Trenfield 等,2018;Zema 等,2017)。因此,我们预计FDM非常适用于数字健康的实施。
熔融沉积成型3D打印(FDM 3DP)是材料挤出技术的一个分支,是一种应用广泛的先进技术,目前其应用范围涵盖航空、汽车、医学、牙科、艺术、珠宝和鞋类(Barnatt,2016)。在制药领域,预计FDM的采用将在药物设计、制剂和生产领域引发范式转变(Berman,2012)。特别是,熔融沉积成型3D打印可作为数字健康领域的一种制造工具,用于远程制造和配药个性化制剂,其剂量、形状和尺寸均可根据患者需求进行优化。这些优势为治疗过程提供了灵活性和自主性,有望提升治疗效果和用药依从性。本综述概述了
材料挤出是一种热过程;其基本原理是通过喷嘴选择性地挤出熔融材料,生成精细的半固态细丝,这些细丝在成型板上固化以形成三维物体。该技术所使用的材料包括热塑性塑料、粘土、蜡、凝胶和膏体。因此,材料挤出是一个广义术语,涵盖了其他一些重要技术,包括熔融沉积成型和半固态挤出。尽管材料挤出和熔融沉积成型这两个术语经常被互换使用,但熔融沉积成型仅涉及热塑性材料(麦克梅因斯,2005年)。
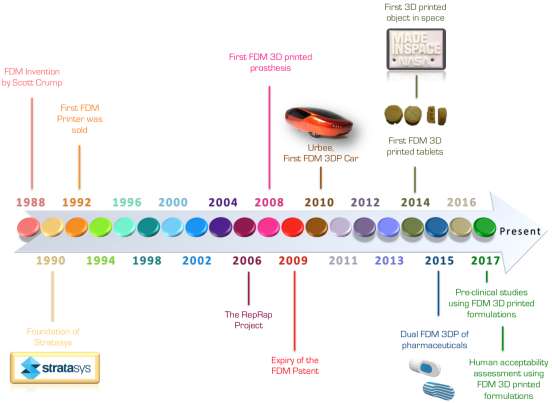
FDM技术,也称为熔丝制造(FFF),最初由斯科特·克朗普于1988年提出,当时他尝试使用简单的热熔胶枪为女儿制作一个玩具(On3DPrinting.com,2013)。他将传统的胶棒替换为聚乙烯和石蜡的混合物,并用它逐层构建玩具。随后,这一想法得到扩展,开发出了该工艺的自动化版本。1989年,克朗普和他的妻子申请了该技术专利,并共同创立了自己的公司斯特拉塔西斯,以实现产品的商业化(Crump,1992;Stratasys,2017a)。该技术被命名为并注册为FDM®。图1概述了FDM过程中当前进展的时间线。
与其他三维打印技术一样,熔融沉积成型法 遵循“三维打印的三个D”(Trenfield 等,2018):(a)设计:使用计算机辅助设计(CAD)软件设计一个三维形状。该形状在数字上被分割为水平层,然后以立体光刻(.stl文件)格式加载到打印机软件中(斯特拉塔西斯,2017a);(b)开发:开发出合适的热塑性载药丝材,然后送入打印机,在特定温度下通过金属喷嘴熔化并挤出(麦克梅因斯,2005)。大多数打印机允许用户选择打印头温度,因此熔融沉积成型打印机可用于打印不同的聚合物和聚合物共混物;(c)分配:挤出的丝材随后被沉积在打印机的平坦基底上,即成型板或平台。打印头按光栅模式移动,形成物体的第一层。每完成一层后,平台会下降,为沉积新的一层留出足够的空间。随着丝材冷却,其与前一层粘合。该过程不断重复,直至物体完成(图2)。打印物体的分辨率取决于挤出丝材的厚度,通常在商用打印机中为 100 μm。

通过简单更换所打印的聚合物,熔融沉积成型(FDM)能够制造出具有独特特性的复杂物体,例如高强度机械性能和耐热性。在医学领域,外科医生已探索利用该技术打印专为患者定制的解剖导板和器官模型,以训练应对复杂手术(Maxey,2013)。通过集成电子传感器,这些模型可对外科技术进行定量分析(例如手术持续时间和成功率),因此被称为“智能外科辅助工具”(Qiu 等,2018)。此外,基于通过成熟的成像技术(如计算机断层扫描(CT)或磁共振成像(MRI))获取的人体数据构建的器官模型,也可用于测试,这一过程称为生物建模。例如,基于患者气管CT扫描数据采用FDM 3D打印的诱导口(IP)模型,被证明优于药典用诱导口,能更深入地支持对加压定量吸入器的体外评估(Berkenfeld 等,2018)。然而,与其他3D打印技术(如立体光刻(SLA))相比,FDM器官模型在体外评估中的应用较为有限;立体光刻已被用于打印气道模型以进行吸气流模拟(Collier 等,2018),或打印鼻腔模型以预测雾化器药物沉积情况(Warnken 等,2018)。这主要是由于FDM打印机分辨率有限,导致打印精度较低,或在制作复杂模型时需要使用支撑材料。
此外,已开发出定制骨样铸件作为先进疗法的一种形式(卡拉萨欣,2013)。这些功能性装置利用低强度脉冲超声(LIPUS)来刺激骨愈合。这会在骨折骨骼的细胞上产生机械应力,使其愈合时间最多缩短38%。此外,熔融沉积成型已广泛用于设计患者特异性医疗器械,包括假体(纳亚克等,2016)和植入物(亚努什等,2015),其中此类装置的定制化是一种必要要求(例如用于重建和整形手术的植入物(何等,2006))。其中一个示例是制造能够响应温度和压力的功能化耳部假体(苏亚斯特‐戈麦斯等,2016)。这种智能设备有可能利用机械应力和温度变化来产生电势,从而使听力障碍患者能够响应声音。
此外,熔融沉积成型3D打印可应用于骨组织工程,其中支架已显示出能够承受高强度的机械应变,同时保持较高的组织生长(金等,2006)。2017年,美国食品药品监督管理局(FDA)发布了关于“增材制造医疗器械的技术考量”的指导文件,概述了其对使用3D打印技术进行医疗器械制造的期望(美国食品药品监督管理局,2017)。迄今为止,仅有少数熔融沉积成型打印的医疗植入物(如颅骨板或髋关节)实现了商业化,但均未负载药物。
通常,由热塑性材料制成的丝材被用作熔融沉积成型(FDM)打印机的原料。热塑性塑料的例子包括聚乳酸(PLA)、丙烯腈‐丁二烯‐苯乙烯共聚物(ABS)、聚乙烯醇(PVA)和聚碳酸酯(PC)。然而,这些商业化丝材均不被认为适合用于人体。因此,在药物研究中,FDM所用的原料是通过一种称为热熔挤出(HME)的过程制备的(Sandler 等,2014)。热熔挤出(HME)在制药行业中被广泛用于生产可安全摄入人体的聚合物固体分散体,以提高难溶性药物的溶解度(Miller 等,2007)。挤出过程的第一步是制备粉末混合物。将所需量的聚合物、药物和/或辅料精确称重并混合。所得均质混合物随后倒入料斗中,流入挤出机机筒。该粉末随后受到高温和压力的共同作用而熔化。在旋转螺杆的作用下,熔融材料被推入金属喷嘴,并形成连续的丝状 filament。所得丝材被沉积到收集盘上,使其冷却。然后将丝材密封在适当的包装中,并储存在真空干燥器中以去除残留水分。
药物可通过两种方法整合到丝材中:一种是在挤出过程之前将其掺入粉末混合物中,另一种是通过
将挤出的丝材浸渍于合适的含药溶液中,迫使药物被动扩散进入丝材。已有若干尝试使用被动扩散法对药物进行浸渍(Goyanes 等,2014;Goyanes 等,2015a;Skowyra等人,2015)。然而,该方法的主要缺点是载药量有限(<2 %)。相比之下,热熔挤出可掺入大量药物,提供更高的剂量灵活性(Verstraete 等,2018)。此外,它还可被调整以生成适用于多种活性成分的标准配方,无需改变整个组成。因此,可利用具有相同辅料的丝材来整合不同的药物(例如 5‐氨基水杨酸(5‐ASA)、卡托普利、茶碱和泼尼松龙)(Sadia 等,2016)。因此,将热熔挤出与熔融沉积成型3D打印结合被认为是提高载药量的一种更有效的替代方案。
如表1所示,挤出丝材若要适用于熔融沉积成型打印,应具备某些特性(Aho 等,2015;Fuenmayor 等,2018;纳赛雷丁等人,2018)。例如,丝材直径需在1.75 – 3.00 ± 0.05 毫米范围内,才能顺利装入打印头(Melocchi 等,2015)。然而,某些聚合物在加热时容易膨胀或收缩,因此选择合适的喷嘴尺寸至关重要。此外,直径的均匀性对于确保稳定的打印过程也十分关键,因为不规则性可能导致打印不一致并引发打印失败。因此,使用润滑剂(如硬脂酸镁)可能有助于减少丝材之间的摩擦
挤出物和挤出机螺杆,使丝材能够更稳定地从喷嘴中挤出(贝克等人,2017;戈亚内斯等人,2017a)。
丝材的刚度与脆性之间的平衡对打印至关重要(科特和奎多巴赫,2018b)。这主要是因为过高的刚度会阻碍丝材在卷轴上的正常弯曲,从而限制其使用。因此,需要对聚合物共混物进行改性。另一方面,过高的脆性会阻止丝材被正确装入打印机的 熔化器,或导致其在打印过程中断裂,在某些情况下甚至可能导致喷嘴堵塞。在这种情况下,添加增塑剂有助于降低聚合物的玻璃化转变温度(Tg),并使丝材更具柔性。然而,选择合适类型和用量的增塑剂至关重要。这主要是因为过度的柔韧性会使丝材变得过软,在熔化器内部弯曲并造成堵塞。因此,近期的研究致力于利用验证方法评估丝材的机械性能,以预测其可打印性(Fuenmayor 等,2018;纳赛雷丁等人,2018)。
已对熔融沉积成型在制造多种药品(Cunha‐Filho 等人,2017)方面的潜力进行了广泛研究,包括片剂(Goyanes 等,2015a;Zhao 等,2018),后者也被称为“打印片” (戈亚内斯等人,2017a)、胶囊(Maroni 等,2017; Melocchi 等,2018;Smith 等,2018)、微珠和导管(Weisman 等, 2015)、口服分散膜(Ehtezazi 等,2018;Jamróz 等,2017a)、局部敷用面膜(Goyanes 等,2016)、透皮微针(Luzuriaga 等,2018)、阴道环 (Fu 等,2018)、宫内节育器(IUD)以及皮下植入装置(Genina 等, 2016;Holländer 等,2016)。熔融沉积成型在制药领域广泛应用的主要动因总结于表2。
4.1. 药物递送的多功能平台
人类之间的巨大差异影响着药物在体内的作用方式。由于人体的复杂性,包括年龄、性别、疾病/健康状态以及人类基因在内的多种因素都会影响药物的药代动力学(PK)和药效学(PD)行为(Abuhelwa 等,2017;Ashiru 等,2008; de la Cruz‐Moreno 等,2017;Fadda 等,2010;Freire 等,2011; Hatton 等,2018;Hens 等,2017;Hens 等,2018;Jamei 等,2009; Leong 等,2002;Liu 等,2009;Merchant 等,2016;Nicolas 等,2009; Sadée 和 Dai,2005;Smart 等,2014;Taherali 等,2018;Varum 等, 2013;Wang 等,2015)。因此,不同个体可能需要不同的剂量方案或剂型,而这些并不总是容易获得(Sahlgren 等,2017)。研究表明,在临床试验的早期阶段,大多数药物的成功率较低(Wong 等,2018),给制药行业带来了巨大的经济负担。自2015年精准医疗计划提出以来,治疗个性化受到了广泛关注(Collins 和 Varmus,2015)。因此,制药研究人员一直致力于寻找一个单一平台能够根据患者的需要、偏好和个体特征定制药物(美国食品药品监督管理局,2013)。由于其独特的特性和多功能性,熔融沉积成型3D打印可轻松适应制造几乎任何所需具有特定释放曲线的剂型(Awad 等,2018;Kadry 等, 2018;Tagami 等,2018;Trenfield 等,2018)。这些打印药物的特点是具有精确的空间
药物和辅料的分布,这是大多数其他制造方法无法实现的(Goyanes 等, 2015d)。
FDM技术由于可使用多种聚合物基质,有望对药物递送系统进行编程,以靶向人体特定区域。因此,FDM 3DP可被描述为一种“灵活‐剂量分配器” (Pietrzak 等人,2015),能够在无需额外加工(如包衣)的情况下(Goyanes 等人,2015b),制造出具有不同剂量和从速释(Jamróz 等人, 2017b;Solanki 等人,2018)到缓释(Verstraete 等,2018)乃至修饰释放 (Goyanes 等人,2017a)等多种释放曲线的剂型。因此,该技术为药物装置的工程化提供了更为精密的方法。
2014年,首次尝试采用熔融沉积成型3D打印技术制备口服药物制剂(Goyanes 等,2014)。该研究表明,打印参数是决定药物释放曲线的主要因素。其中一个例子是内部结构或填充率,即3D打印片剂外层壳体内部的填充百分比。含有较少填充材料的片剂表现出更快的药物释放,而具有较高填充材料的片剂则呈现延长的释放曲线。这主要归因于与聚合物密度相关的不同溶胀比。有趣的是,在较低填充率(<20%)时,3D打印片剂的整体密度降低,从而增强其浮力。这种漂浮效应可用于延长其在体内的滞留时间
胃部区域,延长药物释放,这种现象被称为胃滞留(柴等人,2017)。这一发现对于弱碱性药物尤其重要,因为它将提高其生物利用度。然而,这高度依赖于患者饮食和胃中胃液的量,因此在临床中可能会出现性能的高变异性。
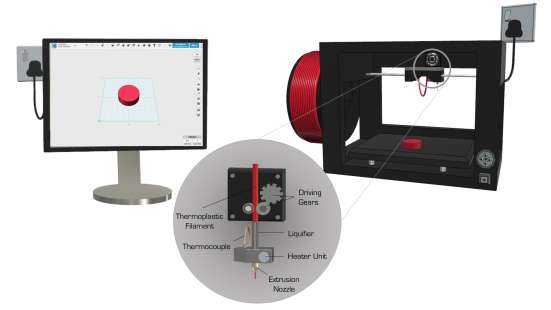
此外,研究人员探索了带通道装置以最大化速释制剂的药物释放(图3A)(萨迪亚等人,2018)。通过控制通道的不同参数(如宽度、长度和结构),可调节药物释放以满足所需的规格。此类复杂几何结构使用传统制造工艺难以生产。类似地,通过制造含有内部间隙的胶囊片(称为间隙片),可促进速释片的破碎,从而无需添加崩解剂(图3B)(阿拉法特等人,2018b)。同样,还制备了具有控释特性和不同密度的3D打印网络(科特和奎多巴赫,2018a)。
胃部区域,延长药物释放,这种现象被称为胃滞留(柴等人,2017)。这一发现对于弱碱性药物尤其重要,因为它将提高其生物利用度。然而,这高度依赖于患者饮食和胃中胃液的量,因此在临床中可能会出现性能的高变异性。
此外,研究人员探索了带通道装置以最大化速释制剂的药物释放(图3A)(萨迪亚等人,2018)。通过控制通道的不同参数(如宽度、长度和结构),可调节药物释放以满足所需的规格。此类复杂几何结构使用传统制造工艺难以生产。类似地,通过制造含有内部间隙的胶囊片(称为间隙片),可促进速释片的破碎,从而无需添加崩解剂(图3B)(阿拉法特等人,2018b)。同样,还制备了具有控释特性和不同密度的3D打印网络(科特和奎多巴赫,2018a)。
质量可通过改变3D打印片剂的大小来控制,也可用于控制药物释放(Skowyra等人,2015)。结果表明,由于较小的片剂具有更高的表面积与质量比,其药物释放速度更快。同样,3D打印片剂的几何形状变化也被发现会影响药物释放。
行为(Goyanes 等,2015c)。研究评估了五种不同形状,包括立方体、金字塔、圆柱体、球体和环面。体外溶出研究表明,片剂的表面积与体积之比改变了药物完全释放所需的时间。因此,药物释放最快的是金字塔形片剂,而最慢的是圆柱体片剂。有利的是,所有3D打印片剂均表现出良好的重量和剂量准确性。
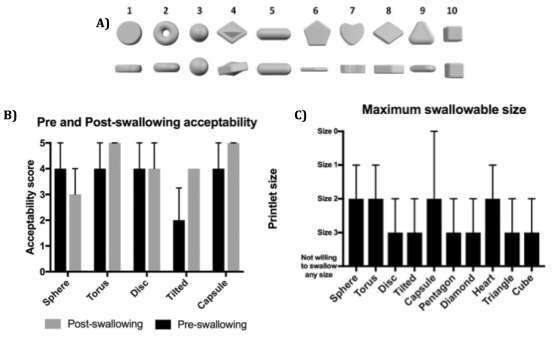
事实上,尽管经常被忽视,但药物的形状、大小和颜色可能是影响治疗方案效果的重要因素。一项开放标签、随机化患者可接受性研究显示,患者更倾向于吞咽某些形状的药物,从而影响其服药依从性(Goyanes 等,2017b)(图 4A)。结果表明,环面形状在操作便捷性和吞咽方面最受青睐(图4B)。而倾斜的菱形在吞咽偏好方面得分最低。这种对吞咽困难的感知可能源于该形状边缘的尖锐程度。然而有趣的是,球体片剂比菱形片剂更难吞咽。此外,研究结果还显示,尺寸2和尺寸3的片剂最受患者欢迎(图4C)。在颜色方面,大多数患者认为添加着色剂会使片剂更具吸引力。这一点在面对特定年龄群体(如儿科和老年科患者)时可能是一个主要因素,这些群体通常存在药物可接受性差的问题。
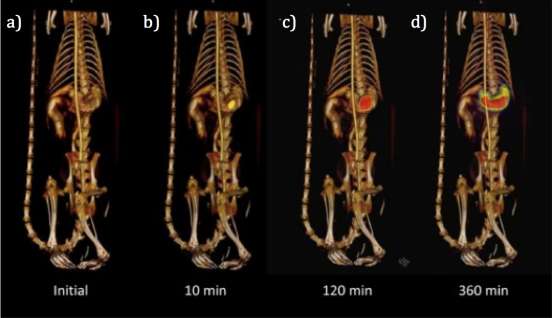
与传统生产方法不同,熔融沉积成型3D打印(FDM 3DP)可通过改变三维结构,立即调整剂型以适应各种测试需求。因此,这可被视为一项重要的临床益处,有助于加快药物研发过程,推动其迅速进入临床前和临床阶段。尽管大多数关于3D打印药物的研究仍集中在体外测试上,但近年来已有研究开始使用动物模型(Arafat等人,2018a;柴等人,2017;Genina等人,2017;戈亚内斯等人,2018)。由于熔融沉积成型适应过程简单,3D打印片剂可轻松修改以适用于特定的动物模型。例如,9号空心胶囊经过专门设计用于大鼠给药(戈亚内斯等人,2018)。测试结果显示,每种制剂表现出不同的崩解时间,这与聚合物的性质有关。有趣的是,保持完整的胶囊未显示出任何示踪剂释放或胃排空迹象(图5)。这一发现非常重要,表明尽管9号胶囊通常被宣传为适用于大鼠给药,但其实际应用仅限于速释应用。对于缓释或控释制剂而言,使用9号胶囊所得的结果可能具有误导性,因为这些胶囊无法从胃部区域排出,在大鼠体内可能表现为胃滞留制剂。这一发现凸显了制剂研究人员常犯的一个错误:在制剂测试中未能正确选择合适的动物模型(Afonso-Pereira 等,2018; Hatton 等,2015;Schulze 等,2005;Varum 等,2010)。
因此,需要对替代剂型或动物模型进行临床前测试评估。
与其他3D打印技术不同,FDM可以在一次打印中制备包含多种聚合物或活性成分的药物,该过程称为双熔融沉积成型打印。已有研究探讨了采用双FDM打印制备控释系统的适用性,其中制造了不同的排列形式(多层片剂和双室片剂)(Goyanes 等,2015d)。在多层片剂中,每一层含有一种药物,下一层则含有另一种药物。相反,双室片剂在片剂中心含有一种药物,外圈部分含有另一种药物。体外溶出研究表明,多层片剂的药物释放仅取决于聚合物的特性,而双室片剂的药物释放则以外层作为限速步骤。
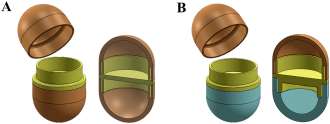
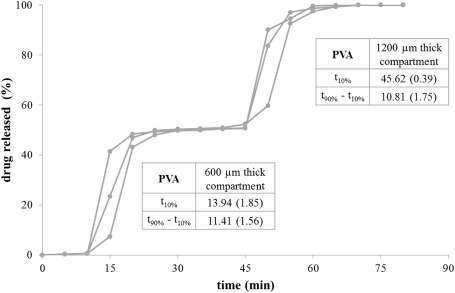
熔融沉积成型3D打印还可用于制造具有明显双室结构的中空胶囊壳( Maroni 等,2017;Melocchi 等,2018)。各个室可采用相同(图6A)或不同的材料和/或厚度进行制造,从而可在不同时间点启动各室的药物释放(图7)。由于这些室被精确密封,因此可以填充粉末甚至液体(Markl 等,2017;Okwuosa 等,2018)。该技术的发展对于创建包含不同药物(例如二甲双胍和格列美脲(Gioumouxouzis 等,2018))或不同剂量药物的个性化药物递送系统具有重要价值。
尤其是因为即使药物在化学上不相容,也可以进行共配方。
4.2. 熔融沉积成型3D打印作为一种数字化工具
数字健康是一个多学科交叉的领域,通过利用从健康信息(如疾病状态和遗传信息)以及通信技术(如计算技术和智能设备)获取的数据,将卫生系统相互连接,以增强治疗效果并提供个性化药物剂型(美国食品药品监督管理局,2018)。可植入或可穿戴传感器可用于远程监测患者的健康/疾病状态( Alhnan 等,2016)。所获得的数据可被分析,从而提供有关治疗需求(如药物、剂量和剂型)的信息。随后可实施FDM 3D打印的3D技术(Trenfield 等,2018)。尽管大多数应用的设计阶段较为简单,但某些患者可能需要更复杂的剂型或医疗器械,这就需要使用3D扫描。3D扫描是一种利用3D扫描仪设备对物体(如其形状、颜色和尺寸)进行分析并收集高精度数据的过程。所收集的数据随后被用于构建数字化3D模型。因此,该技术能够生成几乎任何现实世界物体的模型。
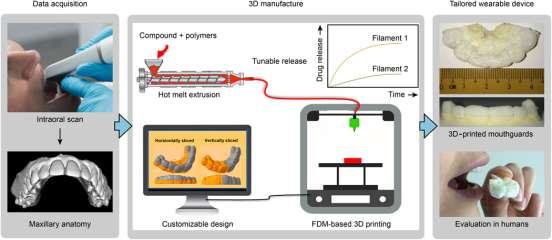
包括身体部位。此类应用已在牙科和听力学领域实现商业化,其中三维打印分别用于大规模定制隐形牙套和助听器(叶,2015)。在制药领域,使用熔融沉积成型技术可以制造适应患者的药物递送装置(图8)(Goyanes 等,2016; 梁等,2018;Muwaffak 等,2017)。这种适应性可增强装置的固定效果,并提供更持久的治疗效果。此外,它们不易引起不适,从而提高患者对药物的依从性。
四维打印(4DP)是一种利用三维打印技术制造能够随时间发生形态变化的物体的新兴技术(蒂比特,2014)。这些智能三维物体被编程为可响应特定刺激,如光、温度、水或pH值,从而引发预设的变化。该编程过程依赖于两个条件:智能材料的使用以及三维结构的智能设计(格拉德曼等人,2016)。通过结合熔融沉积成型3D打印和pH响应性聚合物的基本概念,已成功制备出4D功能系统(纳多戈尔尼等人,2016)。本研究中采用聚(2-乙烯基吡啶)这一pH响应性聚合物作为聚合物主链。在打印完成后,所得到的三维打印结构经过交联和季铵化处理,形成智能水凝胶。这些功能水凝胶表现出可逆的pH介导响应,使其有望应用于流量调节阀和大孔膜。尽管这项发明并未
结合药物后,这项技术或许能为局部药物递送到特定器官带来新的机遇。因此,在研发阶段采用4D打印等先进技术,有望提供更加优化的治疗方案,减少因患者个体间和个体内差异导致的治疗效果差异。最后,FDM 3D打印机的紧凑尺寸和操作便捷性将使得配药阶段可在最近的诊所或医院完成。该数字化框架的采用有望增强医疗系统,提升患者在治疗路径中的自主性,并使药物更加个性化且易于患者获取。
显然,将三维打印技术整合到临床实践中可能会加速数字医疗革命,改变药品为患者设计和处方的方式。然而,与所有进入数字健康领域的新技术一样,其采用往往较为缓慢,并可能伴随诸多挑战。医疗行业以对变革的抵触著称,这很可能是因为既有的监管指南和临床流程已实施多年。尽管这种谨慎态度可以理解,旨在维护患者安全,但往往会阻碍现代技术进步的快速应用。事实上,为了加快三维打印技术在临床实践中的应用,必须建立坚实的证据基础,以证明该技术不仅对患者有益且安全,同时也适用于日常使用该技术的临床医生。
迄今为止,3D打印药物仅在体外或体内动物模型中进行过测试,涉及人体受试者的仅有两项研究:一项为可接受性评估(Goyanes 等,2017b),另一项为评估研究(梁等,2018),这两项研究均采用熔融沉积成型(FDM)技术制备。此外,尽管不同研究已显示出该技术的诸多优势,但尚未有研究将这些数据整合到单一研究中,以证明个性化药物的临床益处和结果。因此,截至目前,该技术所提出的有益特性仍停留在假设阶段,尚无药代动力学/药效学数据表明这些3D打印制剂具有预期更优的药物吸收和胃肠道转运行为。然而,随着该技术的快速发展以及当前使用的丝材均由公认安全(GRAS)的辅料组成,3D打印制剂进入临床试验阶段只是时间问题。尽管如此,要实现这一目标,该技术首先必须能够克服现有突出问题和挑战,从而向“理想3D打印机”现象迈进( Trenfield 等,2018)。
首先,由于该方法包含一个两步热加工过程(挤出和打印),且这两个步骤都涉及高温(最常见为>150°C),药物成分降解的可能性增加(Goyanes 等,2015a)。目前的进展表明,加工温度可降低至40-90°C(Kempin 等,2018; Kollamaram 等,2018)。通过进一步筛选新的辅料
能够进一步降低加工条件,未来熔融沉积成型3D打印有可能在室温下进行打印。
除了高温外,该技术相关的额外热熔挤出步骤也可能耗时,因为丝材并不容易获得,且其可打印性受到多种因素的影响(参见第3节)。因此,FDM技术需要进一步发展,应摒弃对预制成型丝材的需求,转而改进打印机以直接使用原材料(例如颗粒料或粉末)进行打印。目前已有少数FDM打印机采用颗粒料作为起始材料,但该技术仍处于初级阶段,打印机存在多种问题(例如由于冷却时间过长导致的材料成团、层填充不准确以及打印件翘曲)(Whyman 等,2018)。
有利的是,从成本和便携性角度来看,FDM 3D打印机非常适合集成到药房或医院中,用于按需制造个性化剂量。一种 proposed 治疗路径可能包括将患者特定数据通过物理或数字干预(例如智能手机应用程序)发送给医疗从业者进行审查。临床医生随后可以生成电子处方(或“e-处方”),根据患者需求定制,从而设计出相应的制剂并发送至本地FDM打印机进行配药。然而,要实现这一目标,显然需要能够实现不同技术之间跨通信的兼容的软件平台( Brookes, 2017)。此外,
有关数据安全和保护的问题需要被重视,以保护患者的敏感信息。为此,软件开发者、技术创新者、医疗从业者和监管机构之间需要加强沟通,以推动该领域的标准化。
此外,目前商业化的FDM 3D打印机不符合良好生产规范(GMP)的要求,这可能导致3D打印产品对人体服用不安全。因此,需要进行质量控制(QC)测量,以确保符合监管机构制定的政策(Di Prima等人,2016)。首先,对3D打印机进行隔离可以降低产品污染的风险,并可能更好地控制环境条件的变化(Preis等人,2015)。幸运的是,由于熔融沉积成型3D打印片剂已显示出良好的机械性能,因此可能不需要进行脆碎度和硬度等测试。另一方面,尽管理论上3D打印片剂应含有“个性化剂量的药物”;但实际的药物含量必须经过验证。此外,由于FDM和热熔挤出工艺已被证明会改变药物分子的物理状态(例如晶态/非晶态),从而影响其稳定性、溶解度和溶出速率(Murdande等人,2011),因此必须进行分析测定以预测药物性能。
然而,破坏性表征方法,如体外溶出、崩解测试和高效液相色谱(HPLC)
以及紫外-可见分光光度法–在此场景下无法使用。因此,可能需要采用非破坏性方法,例如过程分析技术(PAT),包括近红外(NIR)光谱法(Donoso 和 Ghaly,2005a,b;Donoso 等,2003)或拉曼光谱法(Lee,2009)来替代(Trenfield 等,2018)。此外,改变打印参数(如形状、大小或填充率)也会改变3D打印片剂的整体性能。因此,有必要开发一种能够预测随打印因素变化的药物含量和生物利用度的分析方法。更理想的是,所提出的分析设备或策略应集成于打印机内部(Sandler 和 Preis,2016),以确保批间均匀性并加速最终剂量的配药过程。
三维打印有望在医疗保健领域引发一场数字革命。由于其简便性、多样性和便携性,我们预计熔融沉积成型3D打印可能特别适合应用于数字健康领域。与传统制造技术不同,熔融沉积成型3D打印能够按需生产定制化、面向患者的剂量药物产品,实现精确给药、高重现性和优异的机械性能。此外,还可生产复杂剂型,例如通过容纳多种聚合物基质和活性成分,或通过编程使剂型表现出定制化效果或靶向特定器官。该技术已进一步发展,使其能够与其他技术结合,从而创建更复杂的和“智能” 递送系统。然而,人们普遍认识到,数字健康并不局限于这一种3D打印技术,因为其他3D打印平台也可能证明具有优势。尽管如此,目前所有3D打印技术都受到技术和质量控制障碍的限制,制约了其发展。一旦克服这些障碍,它们的前进和实际应用将成为可能,从而改变制药生产的面貌,并开启数字健康的新时代。
