为什么电极能止血铁及铁的化合物应用广泛.如FeCl3可用作催化剂.印刷电路铜板腐蚀剂和外伤止血剂等. (1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 . 中的反应设计成原电池.请画出原电池的装置图.标出正.负极.并写出电极反应式.指出电解质溶液是 .正极电极反应式为 . (3)写出甲醇(CH3OH)
新闻资讯2026-04-17 13:52:58
【答案】
(1)2Fe3++Cu=2Fe2++Cu2+;(2分)
(2)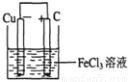 (2分) ;
(2分) ;
FeCl3(1分);
2Fe3++2e—=2Fe2+。(2分)
(3) CH3OH-6e-+8OH-=CO32-+6H2O (3分)
【解析】
试题分析:(1)Fe3+有强氧化性,能把金属铜氧化成铜离子,自身被还原成 Fe2+,反应方程式为2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)设计成原电池时,负极上发生氧化反应,正极上发生还原反应,该电池反应中三价铁离子得电子发生还原反应,所以正极上的电极反应式为Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+),铜失电子发生氧化反应,所以负极上的电极反应式为Cu=2Cu2++2e-(或Cu-2e-=Cu2+);
电池反应中发生氧化反应的金属作负极,所以铜作负极,不如负极活泼的金属或导电的非金属作正极,可选石墨作正极,发生还原反应的电解质溶液作原电池的电解质溶液,所以该原电池图为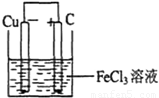 ,故答案为:
,故答案为: ;Cu-2e-=Cu2+;
;Cu-2e-=Cu2+;
Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+)。
(3)甲醇是负极,失去电子,电极式为CH3OH-6e-+8OH-=CO32-+6H2O。
考点:盐和亚铁盐的相互转变 电极反应和电池反应方程式.
点评:本题考查了原电池的工作原理及原电池的设计,难度较大,原电池的设计是学习的重点和难度。